
- •Арилалкиламины и их производные (дигидроксифенилалкиламины, фенилалкиламины)
- •Гидроксифенилалкиламины
- •3. Кислотно-основные свойства:
- •4. Окислительно-восстановительные свойства:
- •5.Комплексообразующие свойства:
- •Физические и физико-химические свойства
- •Гидроксифенилалкиламины Гормоны мозгового слоя надпочечников
- •Получение
- •Химические свойства и особенности строения
- •Вписать продукты растворения ад и над
- •Физические и физико-химические показатели подлинности
- •Чистота
- •279 310 Им λ, нм Количественное определение
- •Хранение
- •Isadrinum – изадрин (изопреналина гидрохлорид)
- •Реакции подлинности
- •6,5 3,56 1,0
- •Чистота
- •Количественное определение
- •Фенилалкиламины ephedrini hydrochloridum – эфедрина гидрохлорид
- •Получение
- •Физические свойства
- •Подлинность Реакции
- •Чистота
- •Количественное определение
Подлинность Реакции
Структуру молекулы эфедрина составляют ароматическое ядро, вторичный спиртовой гидроксил и вторичная алифатическая аминогруппа.
Являясь α-аминоспиртом, эфедрина гидрохлорид обладает слабо выраженными кислотными свойствами, обусловленными подвижностью атома водорода спиртового гидроксила. Соседство спиртового гидроксила с аминогруппой позволяет проводить реакцию комплексообразования.
Реакция комплексообразования с сульфатом меди в щелочной среде. Согласно ФС образуется сине-фиолетовое окрашивание за счёт вторичного спиртового гидроксила и вторичной алифатической аминогруппы.
Образовавшийся комплекс способен переходить в эфирный слой, который приобретает лилово-розовую (красно-фиолетовую) окраску. Водный слой остается синим (ионы меди). Способность комплексной соли эфедрина с ионами меди растворяться в эфире делает эту реакцию специфичной и позволяет отличить от близких по структуре мезатона, адреналина и норадреналина.
![]()
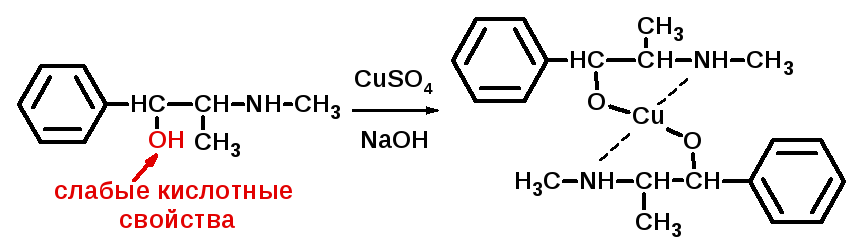
красно-фиолетовое (лилово-розовое)
окрашивание эфира
Эфедрин окисляется в более жёстких условиях и более сильными окислителями (т.к. нет фенольного гидроксила). МФ III на эфедрин даёт реакцию окисления с калия гексациано(III)-ферратом (красной кровяной солью) при нагревании. Окисление идёт за счёт спиртового гидроксила до бензальдегида (запах горького миндаля), при этом расщепляется углерод-углеродная сигма-связь и образуется метилэтиламин (синее окрашивание лакмусовой бумаги):
[O]
+
K3[Fe(CN)6],
t0
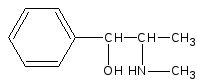
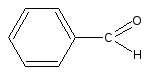
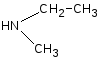
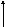
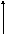
+
метилэтиламин (синее окрашивание
лакмусовой бумаги)
бензальдегид (запах горького миндаля)
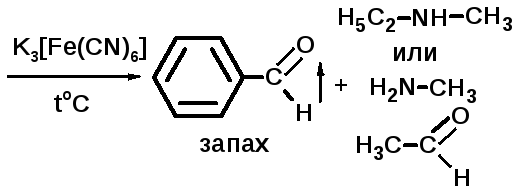
Другие возможные окислители – перманганат калия, йодат калия, нингидрин. С нингидрином в щелочной среде эфедрин образует темно-фиолетовое окрашивание.
Кислотно-основные свойства. Наличие вторичной алифатической аминогруппы определяет основные свойства эфедрина, он образует соли с кислотами и применяется в виде гидрохлорида. Под действием более сильных оснований эфедрина гидрохлорид, как и все соли слабых оснований и сильных кислот, подвергается гидролизу с выделением основания, но основание эфедрина РАСТВОРИМО в воде, поэтому видимых изменений не происходит. Это делает еще более значимым контроль рН (осуществляется потенциометрически).
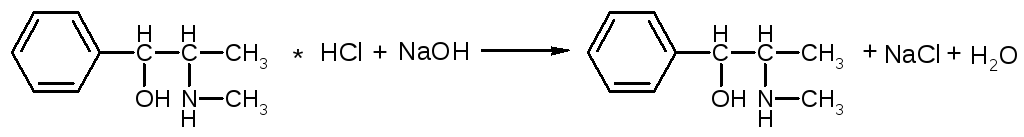
Основание эфедрина растворимо в воде. Контроль процесса гидролиза – измерение рН раствора.
ФС хлорид-ионы доказывают с раствором серебра нитрата.
Физические и физико-химические показатели подлинности
температура плавления
[α]D20 удельное вращение (5% раствора в воде).
УФ-спектр. В диапазоне от 230 до 300 нм имеет набор максимумов (251,257,263 нм) и минимумов (253,361 нм) поглощения каждый из которых обусловлен наличием того или иного структурного фрагмента молекулы.
ИК-спектр.?
