
Строение клетки протистов
.pdf
4.4. ПЛАСТИДЫ
фоторецептор и позволяет клетке осуществлять фототакси сы (детальнее о строении фоторецептора см. стр. 290). Глазки могут располагаться и вне хлоропласта, однако и в этом случа е они находятся у основания жгутика, как у эустигматофитовы х.
4.4.4. Пигменты
Основными пигментами хлоропластов являются хлорофиллы7 à, b è ñ, которые находятся на мембране тилакоидов. Хлорофилл c (или хлорофиллид) встречается в трех формах: c1, c2 è c3. Для разных групп фототрофных протистов характерны определенные наборы хлорофиллов. В хлоропластах зеленых во - дорослей и эвгленовых содержатся хлорофиллы a+b, у красных водорослей – только хлорофилл à, подавляющее большинство остальных фототрофных протистов имеет хлорофиллы a+c.
Вторичные пигменты у водорослей гораздо более многообразны. Они располагаются в пластидах, часто бывают связан ы с основными пигментами, принимая активное участие в фотосинтезе. В больших концентрациях вторичные пигменты могут маскировать зеленый хлорофилл и придавать хлороплас там разнообразную окраску – от желто-зеленой до красновато-ко - ричневой. Все многообразие вторичных пигментов может быт ь распределено по трем группам: фикобилины, каротины и ксан - тофиллы (табл. 6). Фикобилины встречаются только у криптомонад, красных водорослей, глаукофитовых и цианобактерий (прокариоты). Наиболее полный набор их имеется у цианобактерий и родофитовых. У глаукофитовых отсутствует фикоэритрин, а у криптофитовых – аллофикоцианин. Эти пигменты встречаются в двух формах – в виде фикобилисом на поверхности тилакоидов (цианобактерии, красные водоросли и глаукофиты) и в дисперсном состоянии внутри собранных попарн о тилакоидов (криптофитовые).
7Факт обнаружения у красных водорослей хлорофилла d, который вошел в учебную литературу, в дальнейшем не подтвердился. Этот ти п хлорофилла обнаружен пока только у прокариот.
241

242
Таблица 6. Распределение пигментов и запасных питательных веществ у водорослей. (По: Van den Hoek et al., 1995)
|
Cyanobacteria |
Prochlorophyta |
Glaucophyta |
Rhodophyta |
Chrysophyceae |
Xanthophyceae |
Eustigmatophyceae |
Bacillariophyceae |
Raphidophyceae |
Pedinellophyceae |
Phaeophyceae |
Haptophyta |
Cryptophyta |
Dinophyta I |
Dinophyta II |
Euglenoidea |
Chlorarachniophyceae |
СТРОЕНИЕ .4 ГЛАВА |
Хлорофиллы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хлорофилл a |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
+ |
++ |
++ |
КЛЕТКИ |
хлорофилл c1 |
|
|
|
|
++ |
+ |
|
++ |
++ |
|
++ |
++ |
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
хлорофилл b |
|
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
++ |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
ПРОТИСТОВ |
хлорофилл c2 |
|
|
|
|
++ |
+ |
|
++ |
++ |
++1 |
++ |
++ |
++ |
++ |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
хлорофилл c3 |
|
|
|
|
+- |
|
|
++ |
|
|
++ |
|
|
|
|
|
|
|
Фикобилины |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фикоцианин |
++ |
|
++ |
++ |
|
|
|
|
|
|
|
|
++ |
|
|
|
|
|
аллофикоцианин |
++ |
|
++ |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фикоэритрин |
++ |
|
|
++ |
|
|
|
|
|
|
|
|
++ |
|
|
|
|
|
фикобилисомы |
++ |
|
++ |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Каротины |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α-каротин |
|
|
|
++ |
+ |
|
|
|
|
|
|
+ |
++ |
|
+ |
|
|
|
β-каротин |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
++ |
+- |
++ |
+ |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|

|
Ксантофиллы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
зеаксантин |
++ |
++ |
++ |
++ |
|
+ |
|
+- |
|
|
+3 |
|
+- |
|
+ |
|
|
|
+- |
|
+ |
||
|
эхиненон |
++ |
+ |
|
|
|
|
|
|
+ |
|
|
|
|
+ |
|
|
+ |
|
+- |
|
+- |
||
|
кантаксантин |
++ |
|
|
|
|
|
|
+ |
+ |
|
|
|
|
+ |
|
|
+ |
|
|
|
|
||
|
миксоксантофилл |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
осциллаксантин |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лютеин |
|
|
|
+ |
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
+ |
++ |
|
антераксантин |
|
|
|
+- |
|
+ |
|
+ |
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
+ |
|
виолаксантин |
|
|
|
+- |
|
+ |
|
++ |
|
|
+3 |
|
++ |
|
|
|
|
|
|
|
+ |
++ |
|
|
фукоксантин |
|
|
|
|
|
++ |
|
|
++ |
++3 |
++ |
++ |
++ |
|
|
|
|
+ |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
диатоксантин |
|
|
|
|
|
+ |
++ |
|
++ |
|
|
+ |
+ |
++ |
|
|
|
|
+ |
+- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
диадиноксантин |
|
|
|
|
|
+ |
++ |
|
++ |
++ |
+ |
+ |
++ |
|
|
++ |
+ |
+ |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
вошериаксантин |
|
|
|
|
|
|
++ |
++ |
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
гетероксантин |
|
|
|
|
|
|
++ |
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
аллоксантин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
++ |
|
|
|
|
|
|
|
|
перединин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
++ |
|
|
|
|
|
|
неоксантин |
|
|
|
|
|
+ |
+ |
+ |
+ |
+ |
|
+ |
|
|
|
|
|
|
++ |
+ |
++ |
||
|
Запасные питательные вещества |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Цианофицин |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α-1,4-глюканы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Цианофитиновый |
++ |
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
крахмал |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Багрянковый |
|
|
|
++ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
крахмал |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Крахмал |
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
++ |
|
|
|
++ |
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
β-1,3-глюканы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Хризоламинарин |
|
|
|
|
|
++ |
++ |
++ |
|
++ |
|
? |
? |
++ |
++ |
|
|
|
|
|
|
|
|
|
парамилон |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
++4 |
|
|
|
|
|
+ |
? |
|
243 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПЛАСТИДЫ .4.4

ГЛАВА 4. СТРОЕНИЕ КЛЕТКИ ПРОТИСТОВ
Обозначения к таблице 6 (стр. 242-243): ++ - важные пигменты, + - пигмент присутствует, +- - встречается редко, ? - данные отсутствуют, Dinophyta I – типичные динофитовые, Dinophyta II – динофитовые с эукариотичес кими симбионтами (преимущественно бурыми водорослями), Prochloroph yta включают только род Prochloron, который относится в настоящее время к Cyanobacteria. 1 – неизвестно, какой именно хлорофилл ñ, 2 –пигмент, подобный хлорофиллу ñ, обнаружен у 5 видов празинофитовых, 3 - встречается только у морских представителей таксона, 4 – отмечен у Pavlova.
4.4.5. Лейкопласты
Многие протисты, утратившие способность к фотосинтезу, со - хранили пластиды в измененном виде и часть пластидного ге - нома. Такие редуцированные пластиды называют лейкопластами. Наличие в них функционирующей ДНК указывает на то, что она содержит немало генов, которые не связаны напряму ю с биосинтезом белков фотосинтетических реакций.
Лейкопласты характерны для бесцветных (гетеротрофных) хризомонад. Они располагаются обычно в перинуклеарном
Рис. 4.74. Схема строения бесцветного хризофита
Anthophysa vegetans ñ
лейкопластом в перинуклеарном пространстве. (По: Belcher, Swale, 1972.) В лейкопласте (ле) видны глобулы глазка
(г). вз – вздутие в основании короткого жгутика, кж – короткий жгутик, м – митохондрия, пв – пищеварительная вакуоль, пн – перинуклеарное пространство, ож – опушенный жгутик, я – ядро.
244

4.4. ПЛАСТИДЫ
пространстве ядра, ограничены 1–2 мембранами, содержат иногда внутренние мембраны и пигментные гранулы, которые преставляют собой, по-видимому, остатки тилакоидов и глаз - ка (рис. 4.74).
Одним из вариантов лейкопласта следует считать, вероятно, так называемый апикопласт. Эта структура в виде довольно крупной вакуоли с гетерогенным содержимым была обнаружена у спорозоитов споровиков и долгое время не привлекала внимания. Однако сравнительно недавно в ядерной ДНК споровиков был обнаружен ген rbs, кодирующий малую субъединицу этого фермента. Кроме того, более детальные ультраструктурные исследования показали, что в оболочке апикопласта имеется 4 мембраны. Таким образом, предполагается, что апикопласт Apicomplexa – это редуцированный хлоропласт, близкий по последовательности нуклеотидов гена rbsS (малой субъединицы RUBISCO) к хлоропласту зеленых водорослей.
В последнее время, однако, больший вес при выяснении филогении хлоропластов имеют данные по последовательност и нуклеотидов у рибосомальных генов хлоропластной ДНК. Так, секвенирование генов АТФазы показывает, что апикопласт эволюционировал из пластид красных водорослей, а анализ полной последовательности нуклеотидов ДНК апикопласта позволяет предполагать, что он эволюционировал вне линии ра з- вития зеленых пластид и предположительно связан своим происхождением с хлоропластами динофитовых. Это предположение, однако, противоричит тому общеизвестному факту, что обе субъединицы гена rbs находятся в пластидном геноме у всех водорослей, за исключением зеленых, у которых ген ма - лой субъединицы находится в ядерном геноме. Поэтому, если бы апикопласт был связан своим происхождением с хлоропластами динофитовых, то его гены не были бы обнаружены в ядре.
По-видимому, хлоропласт мог редуцироваться во многих группах автотропных протистов и утратил способность к фо тосинтезу. Однако, несмотря на это, его гены все еще необходим ы клетке, т.к. они регулируют такие существенные процессы, как синтез аминокислот и утилизация липидов.
245

ГЛАВА 4. СТРОЕНИЕ КЛЕТКИ ПРОТИСТОВ
4.4.6. Проблема происхождения пластид
Происхождение пластид путем симбиогенеза в настоящее время общепризнано. В литературе идет обсуждение конкрет - ных путей приобретения пластид в той или иной группе авто - трофных эукариот.
На морфологическом уровне первая догадка о приобретении пластид в эволюции путем симбиогенеза возникает при срав - нении ультратонкого строения цианобактерий и хлоропластов красных водорослей (рис. 4.72). Действительно, легко представить, что сине-зеленые водоросли могут быть заглочены эук а- риотным гетеротрофом и перейти к симбиозу, находясь при э том в симбионтофорной вакуоли. Затем цианобактерия утрачивает клеточную стенку, интегрируется в клетке хозяина на биохи - мическом уровне и становится хлоропластом. Таким образом, наружную мембрану хлоропласта красных водорослей можно рассматривать как мембрану симбионтофорной вакуоли, а вн утреннюю мембрану – как бывшую плазмалемму цианобактерии. Внутреннее содержимое цианобактерии и хлоропласта крас ных водорослей почти идентично. Этот путь происхождения плас - тид подтверждается существованием современных глаукофитовых, в цитоплазме которых мы находим цианеллы – цианобактерии, находящиеся на разных стадиях интеграции в клет ку хозяина. На примере цианелл можно буквально проследить эт а- пы редукции клеточной стенки цианобактерий в разных вида х глаукофитовых.
Таким образом эукариоты, по-видимому, приобрели фотосинтезирующий аппарат, содержащий хлорофилл à. Приобретение других хлорофиллов объясняется двумя основными ги - потезами. 1) После обнаружения хлорофилла b у цианобактерии Prochloron (Lewin, 1986) был предложен путь приобретения хлорофилла b путем независимого симбиоза гетеротрофного предка зеленых водорослей и прохлорона. У зеленых водорослей в оболочке хлоропласта имеется всего 2 мембраны, поэтому ве сь процесс мог происходить так же, как у предков красных водо - рослей. Содержащие хлорофилл b эвгленовые водоросли могли получить его вступив в симбиоз с клеткой зеленых водоросл ей
246
4.4. ПЛАСТИДЫ
(вторичный симбиоз). 2) путь приобретения хлорофилла b в результате трансформации хлорофиллов группы à.
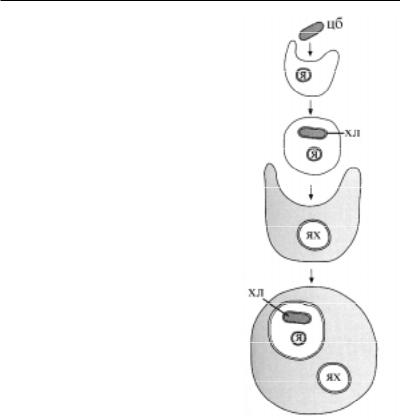
К настоящему времени накопилось достаточно данных, которые показывают, что состав пигментов не является консервативным признаком фототрофных организмов. И у прокариот, и у эукариот обнаружены разные типы хлорофиллов a, b, c1, c2, c3 è äàæå d (у прокариот). С большой долей вероятности предполагается, что возникновение основных пигментов могло происходить независимо в разных группах организмов. Следовательно, сейчас уже нет необходимости в гипотезе о независимом приобретении хлорофилла b путем еще одного акта симбиоза. Поэтому разумно предположить, что первичный симбиоз (приобретение пластид путем симбиоза с цианобактериями) имел место в эволюции лишь однажды и дал начало всему многообразию пластид у современных эукариот (рис. 4.75).
В настоящее время считается, что все современные пластиды происходят от цианобактерий. В литературе приводятся следующие доказательства этой гипотезы. Прежде всего, об этом свидетельствуют морфологи- ческое сходство пластид, типично эубактериальное расположение генов в геноме хлоропластов, молекулярная филогения пластид и сине-
Рис. 4.75. Гипотетическая схема эндосимбиотического происхождения пластид. (По разным авторам). хл – хлоропласт, цб – цианобактерия, я – ядро гетеротрофного протиста, получившего пластиды путем первичного симбиоза
ñцианобактерией, ях – ядро гетеротрофного протиста, получившего пластиды путем вторичного симбиоза
ñэукариотной водорослью.
247

ГЛАВА 4. СТРОЕНИЕ КЛЕТКИ ПРОТИСТОВ
зеленых водорослей на основе генов 16S рРНК и некоторых белков.
Сравнительные исследования пластидного генома у водоро с- лей показывают, что он гораздо меньше бактериального, и большинство генов, отвечающих за синтез специфических белков фотосинтеза, находятся в ядерной ДНК. Таким образом, в процессе становления хлоропластов первоначальные симбионт ы оказывались все более зависимыми от хозяина и постепенно теряли способность жить вне клетки хозяина. К настоящему вр е- мени накопилось немало экспериментальных свидетельств передачи генов из пластид в ядро. Например, уже упоминавшийс я ген rbcS зеленых водорослей находится в ядре, тогда как у других водорослей – в пластидной ДНК; ген tufA, кодирующий фактор элонгации белкового синтеза хлоропластов, у всех в одорослей входит в состав пластидного генома, а у харофитовы х – в состав ядерной ДНК; у Cyanidium caldarium (одноклеточная эукариотная водоросль, близкая к родофитам) ген одной из субъединиц пластидной ДНК-полимеразы локализован в ядре ; а у глаукофита Cyanophora в ядерном геноме находится ген одного из важнейших белков фотосинтетических реакций ферр е- доксин-НАДФ-редуктазы.
Продукты биосинтеза этих генов образуются в цитоплазме и должны быть перенесены в конечном итоге в хлоропласт. Для этого необходимы специальные «направляющие» белки, которые бы транспортировали их из цитоплазмы именно в пластиды, а не в другие органеллы. Таким образом, процесс переноса генов из хлоропластов в ядро требует формирования в проце с- се эволюции дополнительных генов для этих направляющих белков, а также изменения самой системы импорта белков в х лоропласт. В настоящее время известно, что по меньшей мере часть пластидной системы импорта является модификацией систе мы мембранного транспорта цианобактерий.
Цианобактерии довольно часто заселяют цитоплазму эукри - отных клеток в качестве эндобионтов. Они обеспечивают фик - сацию углерода и азота, а также участвуют в метаболизме кл етки. Интересно, что азот-фиксирующие цианобактерии (иногда сильно видоизмененные) встречаются в цитоплазме имеющих
248

4.4. ПЛАСТИДЫ
пластиды клеток, например, диатомовых водорослей. Помимо протистов, цианобактериальные эндобионты найдены в клет - ках губок и некоторых грибов.
Поэтому неудивительно, что существует целый класс пресно - водных протистов (глаукофиты), содержащих в цитоплазме от 2 до нескольких клеток цианобактерий (цианелл). Фактически, цианеллы являются пластидами глаукофитов, однако они сохранили тонкую пептидогликановую клеточную стенку, ха - рактерную для свободноживущих цианобактерий. Строение и биохимические особенности клеточной оболочки цианелл, а также их внутреннее содержимое настолько сходны с этими х а- рактеристиками цианобактерий, что практически не возник а- ет сомнений, что цианеллы были приобретены в результате первичного акта симбиоза гетеротрофных предков глаукофитовых с цианобактериями. В то же время, цианеллы не культивируются отдельно от клетки хозяина, как это показано и для дру - гих пластид, а 90% белков цианелл Cyanophora кодируется в ядре. Таким образом, цианеллы все-таки являются хлоропластами. По ядерно-цитоплазматическим характеристикам глаукофиты близки криптомонадам. Об этом свидетельствуют дан - ные молекулярной филогении по последовательностям нуклеотидов генов 18S рРНК и хитшоковых белков.
По-видимому, в результате первичного эндосимбиоза с цианобактериями были приобретены пластиды глаукофитовыми и красными водорослями, причем, судя по полному отсутствию жгутиков у родофитов, эти события могли произойти независимо. Менее однозначно выглядит гипотеза приобретения пл а- стид таким же образом зелеными водорослями, т.к. их хлоропласты значительно отличаются от цианобактерий. Вполне вероятно, однако, что их пластиды являются производными ц и- анелл глаукофитовых.
4.4.7. Приобретение пластид в результате вторичного эндосимбиоза
Предположение о приобретении пластид в результате вторич- ного эндосимбиоза основано на том, что в оболочке пластид мно-
249

ГЛАВА 4. СТРОЕНИЕ КЛЕТКИ ПРОТИСТОВ
гих водорослей насчитывается более 2 мембран. Такие пластиды называются сложными и они, как было показано в предыдущей главе, характерны для динофитовых и эвгленовых, име - ющих 3 мембраны в оболочке пластиды, а также для всех охрофитов, хлорарахниофитов и криптофитовых, имеющих 4 мембраны. Наружная мембрана таких пластид обычно считается принадлежащей самой клетке, и интерпретируется как мембрана бывшей симбионтофорной вакуоли.
Редкие авторы относят к сложным пластидам также хлоропласты красных и зеленых водорослей, считая их результатом вторичного эндосимбиоза, в процессе эволюции утративших одну или 2 мембраны.
Наиболее веским доказательством приобретения сложных пластид путем эндосимбиоза с эукариотными водорослями считается наличие нуклеоморфа в перипластидном простра н- стве криптофитовых, хлорарахниофитовых и некоторых динофитовых.
Ультраструктурные исследования нуклеоморфа стимулировали его углубленное изучение молекулярными методами. Бы ло показано, что нуклеоморф криптомонад и Chlorarachnion содержит ДНК, организованную в 3 хромосомы. Хромосомы очень короткие (всего 380 000 оснований) и содержат несколько генов, кодирующих рРНК малой субъединицы, сплайсинговые белки, которые обеспечивают процесс считывания ДНК, некоторые рибосомальные белки и протеазы. Наличие этих генов и процесса считывания информации позволило предположить, что нуклеоморф является сильно редуцированным ядром эук а- риотной клетки. Другие гены, необходимые для функционирования пластид, были перенесены в ядро клетки хозяина. Таким образом, синтезируемые в цитоплазме клетки белки пластид должны преодолеть 4 мембраны, чтобы попасть в хлоропласт на место своей окончательной локализации.
Сравнение сиквенсов генов нуклеоморфа, ядра клетки и пластид, а также состав пигментов и морфологические данные показывают, что сложные пластиды хлорарахниофитов и криптомонад приобретены независимо. Пластиды хлорарахн и- офитов получены в результате симбиоза амебы с зелеными во-
250
