
- •Экзаменационные вопросы/ответы на экзамен по биохимии для педиатрического факультета 2012 года
- •1. Биохимия, ее задачи. Значение биохимии для медицины. Современные биохимические методы исследования.
- •2. Аминокислоты, их классификация. Строение и биологическая роль аминокислот. Хроматография аминокислот.
- •3. Электро-химические свойства белков как основа методов их исследования. Электрофорез белков крови.
- •4. Принципы классификации белков. Характеристика простых белков. Характеристика гистонов и протаминов.
- •6. Хромопротеины. Строение и функции гемоглобина. Типы гемоглобинов. Миоглобин.
- •7. Углевод-белковые комплексы. Строение углеводных компонентов. Гликопротеины и их протеоглиганы.
- •8. Липид-белковые комплексы. Строение липидных компонентов. Структурные протеолипиды и липопротеины, их функции.
- •9. Ферменты, их химическая природа, структурная организация. Активный центр ферментов, его строение. Роль металлов в ферментативном катализе, примеры.
- •10. Коферменты и их функции в ферментативных реакциях. Витаминные коферменты. Примеры реакций с участием витаминных коферментов.
- •11. Номенклатура и классификация ферментов. Характеристика класса оксидоредуктаз. Примеры реакций с участием оксидоредуктаз
- •13. Характеристика класса лиаз, изомераз и лигаз (синтетаз), примеры реакций.
- •12. Характеристика классов ферментов трансфераз и гидролаз. Примеры реакций с участием данных ферментов.
- •14. Современные представления о механизме действия ферментов. Стадии ферментативной реакции, молекулярные эффекты, примеры.
- •15. Ингибирование ферментов. Конкурентное и неконкурентное ингибирование, примеры реакций. Лекарственные вещества как ингибиторы ферментов.
- •17. Обмен веществ и энергии. Этапы обмена веществ. Общий путь катаболизма. Катаболизм пирувата.
- •18.Современные представления о биологическом окислении. Компоненты дыхательной цепи и их характеристика
- •21.Роль белков в питании. Превращение белков в органах пищеварительной системы. Роль соляной кислоты в переваривании белков. Характеристика протеолитических ферментов желудочного и кишечного соков.
- •23. Переаминирование и декарбоксилирование аминокислот. Химизм процессов, характеристика ферментов и коферментов. Образование амидов.
- •24. Дезаминирование аминокислот. Виды дезаминирования. Окислительное дезаминирование. Непрямое дезаминирование аминокислот на примере тирозина.
- •25. Синтез мочевины (орнитиновый цикл), последовательность реакций. Биологическая роль.
- •27. Генетические дефекты обмена фенилаланина и тирозина.
- •28. Механизмы репликации днк (матричный принцип, полуконсервативный способ). Условия, необходимые для репликации. Этапы репликации
- •28. Биосинтез рнк (транскрипция). Условия и этапы транскрипции. Процессинг рнк. Альтернативный сплайсинг
- •29. Биосинтез белка. Этапы трансляции и их характеристика. Белковые факторы биосинтеза белка. Энергетическое обеспечение биосинтеза белка.
- •31. Строение оперона. Регуляция биосинтеза белка у прокариотов. Функционирование лактозного и гистидиновых оперонов.
- •32. Особенности и уровни регуляции биосинтеза белка у эукариотов. Амплификация генов, энхансерные и сайленсерные элементы.
- •33. Основные углеводы организма человека, их строение и классификация, биологическая роль.
- •54. Роль углеводов в питании. Переваривание и всасывание углеводов в органах пищеварительной системы. Написать реакции. Непереносимость дисахаридов.
- •34. Катаболизм глюкозы в анаэробных условиях. Химизм процесса, биологическая роль.
- •34. Катаболизм глюкозы в тканях в аэробных условиях. Гексозодифосфатный путь превращения глюкозы и его биологическая роль. Эффект Пастера.
- •36. Гексозомонофосфатный путь превращения глюкозы в тканях и его биологическая роль.
- •37. Биосинтез и распад гликогена в тканях. Биологическая роль этих процессов. Гликогеновые болезни.
- •38. Пути образования глюкозы в организме. Глюконеогенез. Возможные предшественники, последовательность реакций, биологическая роль.
- •39. Характеристика основных липидов организма человека, их строение, классификация, суточная потребность и биологическая роль.
- •40. Биологическая ценность липидов пищи. Переваривание, всасывание и ресинтез липидов в органах пищеварительной системы.
- •42. Характеристика липопротеинов крови, их биологическая роль. Роль липопротеинов в патогенезе атеросклероза Коэффициент атерогенности крови и его клинико- диагностическое значение.
- •43. Окисление высших жирных кислот в тканях. Окисление жирных кислот с нечетным числом углеродных атомов, энергетический эффект.
- •44. Окисление глицерина в тканях. Энергетический эффект этого процесса.
- •45. Биосинтез высших жирных кислот в тканях. Биосинтез жиров в печени и жировой ткани.
- •46. Холестерол. Его химическое строение, биосинтез и биологическая роль. Причины гиперхолестеринемии.
- •47. Витамины, их характеристика, отличительные признаки. Роль витаминов в обмене веществ. Коферментная функция витаминов (примеры).
- •48. Структура и функции витамина а.
- •49. Витамин д, его строение, метаболизм и участие в обмене веществ. Признаки проявления гиповитаминоза.
- •50. Участие витамина е и к в метаболических процессах, их применение в мед. Практике.
- •51. Структура витамина в1, его участие в метаболических процессах, примеры реакций.
- •53. Витамин в2. Строение , участие в обмене веществ.
- •78. Витамин в6 и pp. Роль в обмене аминокислот, примеры реакций, строение.
- •54. Характеристика витамина с, строение. Участие в обмене веществ, проявление гиповитаминоза. Витамин р.
- •55. Витамин в12 и фолиевая кислота. Их химическая природа, участие в метаболических процессах. Причины гиповитаминозов.
- •56. Витамины – антиоксиданты, их биологическая роль. Витаминоподобные вещества. Антивитамины.
- •59. Механизм действия липофильных сигнальных молекул. Механизм действия nо. Действие сигнальных молекул через тирозинкиназные рецепторы. Принципы иммунноферментного анализа уровня сигнальных молекул.
- •61. Гормоны передней доли гипофиза, классификация, их химическая природа, участие в регуляции процессов метаболизма. Семейство пептидов проопиомеланокортина.
- •63. Гормоны задней доли гипофиза, место их образования, химическая природа, влияние на функции органов-мишеней.
- •66. Тиреоидные гормоны, место их образования, строение, транспорт и механизм действия на метаболические процессы.
- •65. Глюкагон и соматостатин. Химическая природа. Влияние на обмен веществ.
- •67. Тиреокальцитонин, паратиреоидный гормон. Химическая природа, участие в регуляции обмена веществ.
- •70. Гормоны половых желез: эстрадиол и тестостерон, их строение, механизм действия и биологическая роль.
- •68 Участие адреналина в регуляции обмена веществ. Место выработки. Структура адреналина,механизм его гормонального действия, метаболические эффекты.
- •69. Кортикостероидные гормоны. Структура, механизм действия, их роль в поддержании гомеостаза. Участие глюкокортикоидов и минералокортикоидов в обмене веществ.
- •64. Инсулин, схема строения, участие в регуляции метаболических процессов. Специфика в действии на рецепторы органов мишеней, инсулиноподобные факторы роста (ифр)
17. Обмен веществ и энергии. Этапы обмена веществ. Общий путь катаболизма. Катаболизм пирувата.
Обмен веществ - необходимое условие жизни. Обмен веществ всегда связан с обменом энергии. Выделяют закрытые и открытые системы. Обмен веществ - это процессы взаимоотношения организма с внешней средой, представляющие совокупность химических реакций, которым подвергаются различные вещества с момента их поступления в организм до момента их выделения в виде конечных продуктов. Основные компоненты живых систем - белки, жиры, углеводы. В организм человека должно поступать: Белков - 100 г. в сутки, Жиров - 100 г. в сутки, Углеводов - 400 г. в сутки. За сутки при обмене этих веществ образуется 2000-3000 ккал энергии.
ЭТАПЫ ОБМЕНА ВЕЩЕСТВ.

1.Поступление веществ из внешней среды посредством питания и дыхания.
2.Превращение веществ в организме - МЕЖУТОЧНЫЙ обмен
3.Выделение конечных продуктов.
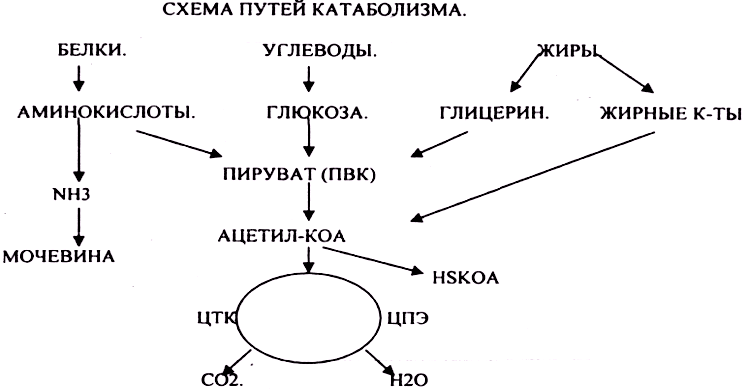
Распад БЖУ до ПИРУВАТА идёт индивидуально для каждой группы органических соединений и носит название специфического пути катаболизма. С образованием ПИРУВАТА начинается общий путь катаболизма, идентичный для обмена всех питательных веществ.
18.Современные представления о биологическом окислении. Компоненты дыхательной цепи и их характеристика
В цикле КРЕБСА АЦЕТИЛ-КОА распадается до СО2 с образованием восстановленных КОФЕРМЕНТОВ - НАДН

АТФ в реакции не участвует, а используется энергия макроэргической связи АЦЕТИЛ-КОА
ЦИТРИЛ-КОА не устойчив и очень быстро распадается под влиянием воды.
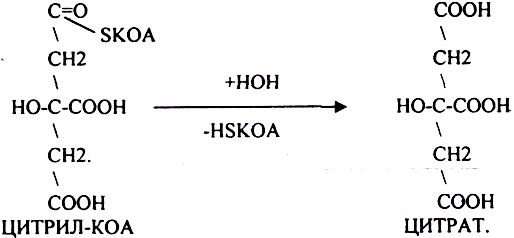
Цитрат превращается в свой изомер (ИЗОЦИТРАТ) под влиянием фермента АКОНИТАЗЫ.

ИЗОЦИТРАТ подвергается далее ДЕГИДРИРОВАНИЮ под влиянием -ИЗОЦИТРАТДЕГИДРОГЕНАЗЫ.

ЩЯВЕЛЕВО-ЯНТАРНАЯ К-ТА подвергается прямому ДЕКАРБОКСИЛИРОВАНИЮ.
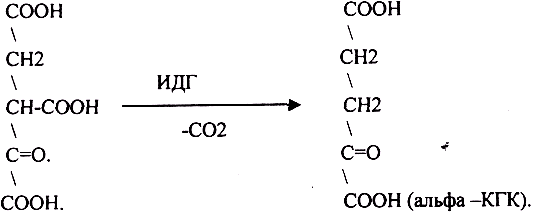
-КГК подвергается реакции ОКИСЛИТЕЛЬНОГО ДЕКАРБОКСИЛИРОВАНИЯ, катализируемой комплексом ферментов (КЕТОГЛУТАРАТДЕГИДРОГЕНАЗНЫЙ комплекс), включающий 3 фермента и 5 КОФЕРМЕНТОВ.

СУКЦИНИЛ-КОА подвергается реакции субстратного ФОСФОРИЛИРОВАНИЯ.
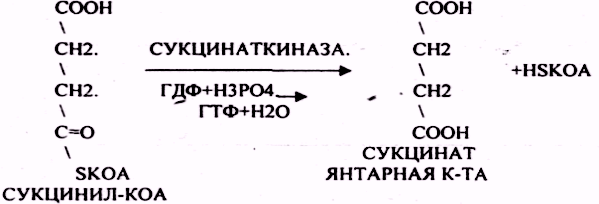
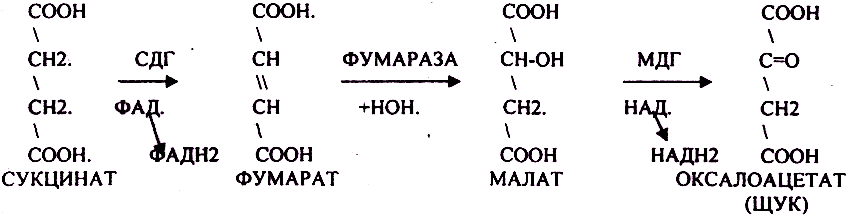
Т.о. происходит распад АЦЕТИЛ-КОА до СО2 и восстановленного HSKOA.
ФУНКЦИИ ЦТК.
1.Катаболическая - распад АЦЕТИЛА.
2.Анаболическая. Компоненты ЦТК могут использоваться для синтеза др. соединений. ЩУК - синтез АСП.
3.Интегративная. Взаимосвязь обмена БЖУ.
4.Энергетическая. Образование 1 молекулы АТФ. Если ЦТК работает вместе с дыхательной цепью, то образуется ещё 1 АТФ.
5.ВОДОРОДГЕНЕРИРУЮЩАЯ - в результате ЦТК образуется 3 молекулы НАДН2 и 1 молекула ФАДН2. Они транспортируются в ЦТЭ.
19)Молекулярные механизмы окислительного фосфорилирования (теория Митчелла). МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ.Теория ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ выдвинута английским учёным П. МИТЧЕЛОМ в 1961 г. и названа ХЕМИООСМОТИЧЕСКОЙ ТЕОРИЕЙ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ. Он объяснил процесс синтеза АТФ с биохимической позиции, но его взгляды не получили признания. Однако в последующем его теория подтвердилась, и через 17 лет он был удостоен Нобелевской премии.Основные положения теории:1.Мембрана МИТОХОНДРИЙ не проницаема для протонов.2.Образуется протонный потенциал в процессе транспорта электронов и протонов.3.Обратный транспорт протонов в МАТРИКС сопряжен с образованием АТФ.Процесс транспорта электронов происходит во внутренней мембране. Первые реакции окисления происходят в матрице. Протоны переносятся в межмембранное пространство, а электроны продвигаются по дыхательной цепи. В процессе работы дыхательной цепи внутренняя мембрана со стороны матрицы заряжается отрицательно, а со стороны межмембранного пространства положительно. Следовательно, возникает разность потенциалов, градиент концентрации ионов, и, соответственно, градиент РН. Т.о. РН со стороны матрицы будет менее кислая. Во время дыхания создаётся ЭЛЕКТРО-ХИМИЧЕСКИЙ градиент: концентрационный и разности потенциалов. Электрический и концентрационный градиент составляет ПРОТОНДВИЖУЩУЮ силу, которая даёт силу для синтеза АТФ. На определённых участках внутренней мембраны есть протонные каналы, образованные АТФ-СИНТЕТАЗОЙ. Протоны могут проходить обратно в матрицу, при этом образующаяся энергия идёт на синтез АТФ.УСЛОВИЯ ОБРАЗОВАНИЯ АТФ.1. Целостность мембраны - непроницаемость её для протонов.2. Наличие специальных каналов.3. Движение протонов в матрицу сопровождается выделением энергии, используемой для синтеза АТФ.Вопрос о том, что позволяет протонам переходить в межмембранное пространство остаётся не вполне ясным.Основные компоненты ЭТЦ представляют собой интегральные белки и фиксированные в мембране: 1.НАДН-ДГ.2.QН2-ДГ.3.ЦИТОХРОМОКСИДАЗА.4.KOQ не связан с белками.5.ЦИТОХРОМ с - не фиксирован к мембране.Выдвигается теория Q-цикла транспорта протонов.2Н + 2е + KOQ KOQ*H2 KOQ*H2 KOQ + 2Н + 2е - на наружной поверхности внутренней мембраны.Т.о. в соответствии с ХЕМООСМОТИЧЕСКОЙ теорией МИТЧЕЛА окисление НАДН2 и ФАДН2 в дыхательной цепи создаёт сначала ЭЛЕКТРОНО-ХИМИЧЕСКИЙ протонный потенциал, градиент концентрации ионов на внутренней мембране, а обратный транспорт протонов через мембрану сопряжен с ФОСФОРИЛИРОВАНИЕМ, т.е. образованием АТФ.
