
- •Экзаменационные вопросы/ответы на экзамен по биохимии для педиатрического факультета 2012 года
- •1. Биохимия, ее задачи. Значение биохимии для медицины. Современные биохимические методы исследования.
- •2. Аминокислоты, их классификация. Строение и биологическая роль аминокислот. Хроматография аминокислот.
- •3. Электро-химические свойства белков как основа методов их исследования. Электрофорез белков крови.
- •4. Принципы классификации белков. Характеристика простых белков. Характеристика гистонов и протаминов.
- •6. Хромопротеины. Строение и функции гемоглобина. Типы гемоглобинов. Миоглобин.
- •7. Углевод-белковые комплексы. Строение углеводных компонентов. Гликопротеины и их протеоглиганы.
- •8. Липид-белковые комплексы. Строение липидных компонентов. Структурные протеолипиды и липопротеины, их функции.
- •9. Ферменты, их химическая природа, структурная организация. Активный центр ферментов, его строение. Роль металлов в ферментативном катализе, примеры.
- •10. Коферменты и их функции в ферментативных реакциях. Витаминные коферменты. Примеры реакций с участием витаминных коферментов.
- •11. Номенклатура и классификация ферментов. Характеристика класса оксидоредуктаз. Примеры реакций с участием оксидоредуктаз
- •13. Характеристика класса лиаз, изомераз и лигаз (синтетаз), примеры реакций.
- •12. Характеристика классов ферментов трансфераз и гидролаз. Примеры реакций с участием данных ферментов.
- •14. Современные представления о механизме действия ферментов. Стадии ферментативной реакции, молекулярные эффекты, примеры.
- •15. Ингибирование ферментов. Конкурентное и неконкурентное ингибирование, примеры реакций. Лекарственные вещества как ингибиторы ферментов.
- •17. Обмен веществ и энергии. Этапы обмена веществ. Общий путь катаболизма. Катаболизм пирувата.
- •18.Современные представления о биологическом окислении. Компоненты дыхательной цепи и их характеристика
- •21.Роль белков в питании. Превращение белков в органах пищеварительной системы. Роль соляной кислоты в переваривании белков. Характеристика протеолитических ферментов желудочного и кишечного соков.
- •23. Переаминирование и декарбоксилирование аминокислот. Химизм процессов, характеристика ферментов и коферментов. Образование амидов.
- •24. Дезаминирование аминокислот. Виды дезаминирования. Окислительное дезаминирование. Непрямое дезаминирование аминокислот на примере тирозина.
- •25. Синтез мочевины (орнитиновый цикл), последовательность реакций. Биологическая роль.
- •27. Генетические дефекты обмена фенилаланина и тирозина.
- •28. Механизмы репликации днк (матричный принцип, полуконсервативный способ). Условия, необходимые для репликации. Этапы репликации
- •28. Биосинтез рнк (транскрипция). Условия и этапы транскрипции. Процессинг рнк. Альтернативный сплайсинг
- •29. Биосинтез белка. Этапы трансляции и их характеристика. Белковые факторы биосинтеза белка. Энергетическое обеспечение биосинтеза белка.
- •31. Строение оперона. Регуляция биосинтеза белка у прокариотов. Функционирование лактозного и гистидиновых оперонов.
- •32. Особенности и уровни регуляции биосинтеза белка у эукариотов. Амплификация генов, энхансерные и сайленсерные элементы.
- •33. Основные углеводы организма человека, их строение и классификация, биологическая роль.
- •54. Роль углеводов в питании. Переваривание и всасывание углеводов в органах пищеварительной системы. Написать реакции. Непереносимость дисахаридов.
- •34. Катаболизм глюкозы в анаэробных условиях. Химизм процесса, биологическая роль.
- •34. Катаболизм глюкозы в тканях в аэробных условиях. Гексозодифосфатный путь превращения глюкозы и его биологическая роль. Эффект Пастера.
- •36. Гексозомонофосфатный путь превращения глюкозы в тканях и его биологическая роль.
- •37. Биосинтез и распад гликогена в тканях. Биологическая роль этих процессов. Гликогеновые болезни.
- •38. Пути образования глюкозы в организме. Глюконеогенез. Возможные предшественники, последовательность реакций, биологическая роль.
- •39. Характеристика основных липидов организма человека, их строение, классификация, суточная потребность и биологическая роль.
- •40. Биологическая ценность липидов пищи. Переваривание, всасывание и ресинтез липидов в органах пищеварительной системы.
- •42. Характеристика липопротеинов крови, их биологическая роль. Роль липопротеинов в патогенезе атеросклероза Коэффициент атерогенности крови и его клинико- диагностическое значение.
- •43. Окисление высших жирных кислот в тканях. Окисление жирных кислот с нечетным числом углеродных атомов, энергетический эффект.
- •44. Окисление глицерина в тканях. Энергетический эффект этого процесса.
- •45. Биосинтез высших жирных кислот в тканях. Биосинтез жиров в печени и жировой ткани.
- •46. Холестерол. Его химическое строение, биосинтез и биологическая роль. Причины гиперхолестеринемии.
- •47. Витамины, их характеристика, отличительные признаки. Роль витаминов в обмене веществ. Коферментная функция витаминов (примеры).
- •48. Структура и функции витамина а.
- •49. Витамин д, его строение, метаболизм и участие в обмене веществ. Признаки проявления гиповитаминоза.
- •50. Участие витамина е и к в метаболических процессах, их применение в мед. Практике.
- •51. Структура витамина в1, его участие в метаболических процессах, примеры реакций.
- •53. Витамин в2. Строение , участие в обмене веществ.
- •78. Витамин в6 и pp. Роль в обмене аминокислот, примеры реакций, строение.
- •54. Характеристика витамина с, строение. Участие в обмене веществ, проявление гиповитаминоза. Витамин р.
- •55. Витамин в12 и фолиевая кислота. Их химическая природа, участие в метаболических процессах. Причины гиповитаминозов.
- •56. Витамины – антиоксиданты, их биологическая роль. Витаминоподобные вещества. Антивитамины.
- •59. Механизм действия липофильных сигнальных молекул. Механизм действия nо. Действие сигнальных молекул через тирозинкиназные рецепторы. Принципы иммунноферментного анализа уровня сигнальных молекул.
- •61. Гормоны передней доли гипофиза, классификация, их химическая природа, участие в регуляции процессов метаболизма. Семейство пептидов проопиомеланокортина.
- •63. Гормоны задней доли гипофиза, место их образования, химическая природа, влияние на функции органов-мишеней.
- •66. Тиреоидные гормоны, место их образования, строение, транспорт и механизм действия на метаболические процессы.
- •65. Глюкагон и соматостатин. Химическая природа. Влияние на обмен веществ.
- •67. Тиреокальцитонин, паратиреоидный гормон. Химическая природа, участие в регуляции обмена веществ.
- •70. Гормоны половых желез: эстрадиол и тестостерон, их строение, механизм действия и биологическая роль.
- •68 Участие адреналина в регуляции обмена веществ. Место выработки. Структура адреналина,механизм его гормонального действия, метаболические эффекты.
- •69. Кортикостероидные гормоны. Структура, механизм действия, их роль в поддержании гомеостаза. Участие глюкокортикоидов и минералокортикоидов в обмене веществ.
- •64. Инсулин, схема строения, участие в регуляции метаболических процессов. Специфика в действии на рецепторы органов мишеней, инсулиноподобные факторы роста (ифр)
9. Ферменты, их химическая природа, структурная организация. Активный центр ферментов, его строение. Роль металлов в ферментативном катализе, примеры.
Ферменты - это биологические катализаторы белковой природы. Ферменты начинают своё каталитическое действие в ЖКТ, продолжают его в тканях, на этапе выведения и образования конечных продуктов. Все реакции в организме ферментативные.
1. Повышают скорость реакции.
2. В реакциях они не расходуются.
3. Для обратимых процессов и прямая, и обратная реакция катализируется одним и тем же ферментом.
ОТЛИЧИТЕЛЬНЫЕ ПРИЗНАКИ.
1 .Ферменты обладают более высокой эффективностью действия.
2.Ферменты чувствительны к температуре (ТЕРМОЛАБИЛЬНЫ)
3.Ферменты чувствительны к значениям РН среды.
4.Ферменты обладают высокой специфичностью действия.
5.Ферменты - это катализаторы с регулируемой активностью.
Ферменты, как и все функциональные белки, могут быть простыми и сложными. Простые ферменты представлены только белковой частью (состоят из АК) - ПЕПСИН, ТРИПСИН, ФОСФАТАЗЫ. В структурном отношении имеют 3 уровня организации.
Сложные ферменты представлены:
1 .Белковой частью (состоит из АК) - АПОФЕРМЕНТ;
2.Небелковой частью - КОФАКТОР.
Выделяют 2 основных КОФАКТОРА:
А. Ионы металлов (К, Na, Ca, Mg, Mn) большинство всех ферментов являются МЕТАЛЛОФЕРМЕНТАМИ. В продуктах питания должны обязательно содержаться микроэлементы.
В. КОФЕРМЕНТЫ - низкомолекулярные органические вещества не белковой природы. Активный центр - это участок в молекуле фермента, где происходит связывание и превращение субстрата. АКТ. Ц обычно располагается в гидрофобном углублении , изолируя субстрат от воды. В образовании АКТ. Ц, участвуют боковые группы АК (12-20 АК), причём эти АК могут находиться на разных участках ПОЛИПЕПТИДНОЙ цепи, но при формировании пространственной конфигурации фермента они укладываются т.о., что располагаются в области активного центра. В образовании активного центра принимают участие следующие группы: NH2 (АРГ,ЛИЗ), СООН (АСП, ГЛУ), SH (ЦИС), ОН (СЕР,ТРЕ), ИМИДАЗОЛ (ГИС), ГУАНИДИНО-группа.. Контактный участок -это место в активном центре фермента, где происходит связывание субстрата с его активным центром. Контактный участок обеспечивает специфическое сродство субстрата к ферменту. Каталитический участок - место, где проходит сама каталитическая реакция.
10. Коферменты и их функции в ферментативных реакциях. Витаминные коферменты. Примеры реакций с участием витаминных коферментов.
КОФЕРМЕНТЫ - низкомолекулярные органические вещества не белковой природы. Они чаще всего содержат в своём составе различные витамины, следовательно, их делят на две группы: 1.Витаминные. 2.Невитаминные.
1.ТИАМИНОВЫЕ в составе витамин В1 (ТИАМИН) - ТМФ – ТИАМИНМОНОФОСФАТ, ТДФ- ТИАМИНДИФОСФАТ, ТТФ - ТИАМИНТРИФОСФАТ. ТПФ связана с ферментами ДЕКАРБОКСИЛАЗАМИ альфа КЕТОКИСЛОТ (ПВК, альфа КГК)

2.ФЛАВИНОВЫЕ содержат витамин В2 - ФМН – ФЛАВИНМОНОНУКЛЕОТИД, ФАД - ФЛАВИИАДЕНИНДИНУКЛЕОТИД.
ФМН и ФАД связанны с ферментами ДЕГИДРОГЕНАЗАМИ. Участвуют в реакциях ДЕГИДРИРОВАНИЯ.
3. ПАНТОТЕИНОВЫЕ (витамин ВЗ) - KOF A (HS-KOA - HS КОЭНЗИМ А) - КОФЕРМЕНТ АЦИЛИРОВАНИЯ.
4. НИКОТИНАМИДНЫЕ содержат витамин РР (НИАЦИН)- НАД (НИКОТИНАМИДАДЕНИНДИНУКЛЕОТИД), НАДФ (НИКОТИНАМИДАДЕНИНДИНУКЛЕОТИДФОСФАТ). Связаны с ДЕГИДРОГЕНАЗАМИ:

5.ПИРИДОКСИНОВЫЕ содержат витамин В6. ПАФ – ПИРИДОКСАМИНОФОСФАТ, ПФ - ПИРИДОКСАЛЬФОСФАТ.:
1.Реакции ПЕРЕАМИНИРОВАНИЯ (ТРАНСАМИНИРОВАНИЕ). Связан с ферментами АМИНОТРАНСФЕРАЗАМИ.
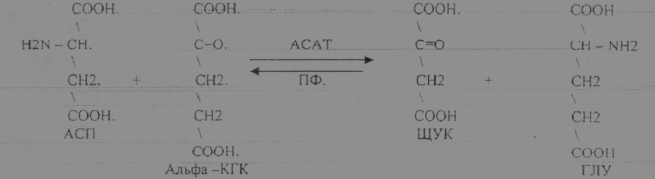
2.РЕАКЦИИ ДЕКАРБОКСИЛИРОВАНИЯ АК.
