
- •Оптические спектры
- •Законы поглощения света
- •Способы изображения спектров поглощения
- •1. Электронная спектроскопия связь электронных спектров поглощения со строением органических соединений
- •Связывающие орбитали: σ, π;
- •Несвязывающая орбиталь: n;
- •Разрыхляющие орбитали: π*, σ*
- •Энергия орбиталей повышается снизу вверх
- •Электронные спектры поглощения отдельных классов органических соединений
- •Растворители, применяемые при измерении электронных спектров поглощения
- •2. Инфракрасная спектроскопия
- •Спектры комбинационного рассеяния
- •3. Ядерный магнитный резонанс
- •Основы метода
- •Химический сдвиг
- •Соотношения между химическим сдвигом и молекулярной структурой
- •Непрямое спин-спиновое взаимодействие ядер
- •Интегрирование сигналов
- •Пример расшифровки спектра 1н ямр
- •4. Масс-спектрометрия
- •Методы ионизации
- •Список литературы
Интегрирование сигналов
Площадь под резонансным сигналом всегда пропорциональна числу резонирующих ядер. Так, например, площади под сигналами в ПМР спектре толуола находятся в соответствии с соотношением числа фенильных и метильных протонов (5:3) (Рис.16).

Рис.16. Интегрирование сигналов протонов толуола [2].
Из интеграла можно получить следующую информацию:
а) количественный элементный анализ на содержание элементов с магнитными ядрами (например, 1H, 19F, 31P и т.д);
б) определение числа эквивалентных ядер в молекуле. Таким образом можно, например, определять длину цепи жирных кислот или соотношение различных фрагментов в сополимерах;
в) количественный изотопный анализ. Можно определять также степень изотопного замещения (например, дейтерирования) в различных положениях молекулы;
г) количественный анализ простых и равновесных смесей. Преимущество такого метода состоит в том, что в процессе съемки положение равновесия не затрагивается (например, кето-енольное равновесие).
Пример расшифровки спектра 1н ямр
Задача 1. Объясните спектр ПМР диэтилового эфира

янтарной кислоты, приведенный на рисунке 17.
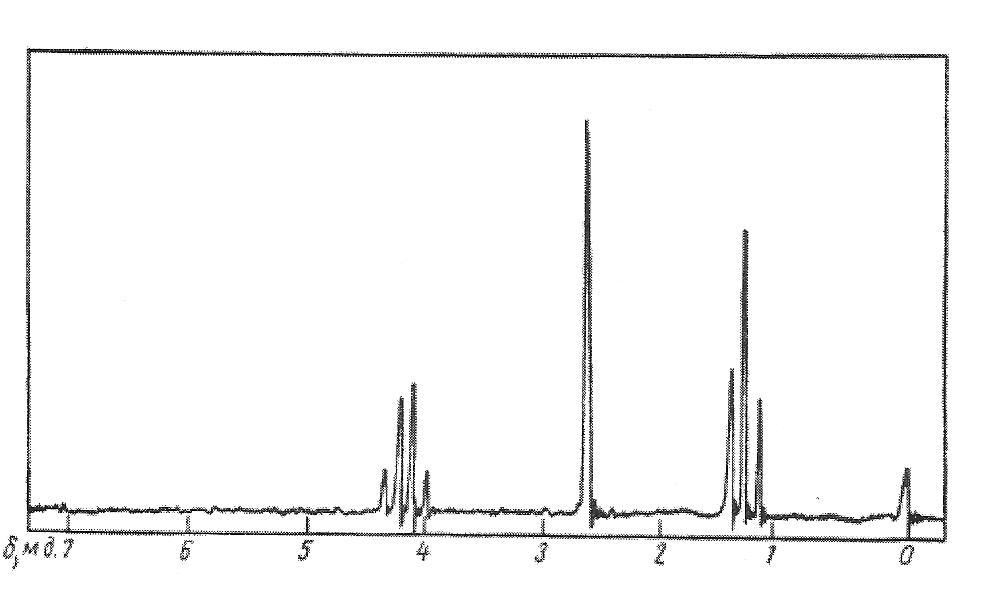
Рис.17. ПМР-спектр диэтилового эфира янтарной кислоты [2].
В соответствии с обозначениями трех типов протонов в формуле диэтилового эфира янтарной кислоты химические их сдвиги δ являются следующими:
δ, м.д. а - 1,25; б - 4,15; в - 2,62.
4. Масс-спектрометрия
Введение
Наиболее мощными и многоцелевыми из физико-химических методов анализа являются спектроскопия ядерного магнитного резонанса и масс-спектрометрия. Оба метода активно используются в химии, биологии, медицине, экологии, криминалистике и т. д.
Говоря о достоинствах масс-спектрометрии, следует прежде всего отметить чувствительность, экспрессность, информативность и надежность метода. Для получения достоверного масс-спектра индивидуального соединения достаточно 10-9 – 10-10 г вещества. При необходимости простого детектирования конкретного соединения в смеси порог обнаружения может быть легко снижен до 10-12 – 10-14 г а в некоторых случаях чувствительность может быть увеличена еще на несколько порядков.
Для получения обычного спектра электронного удара индивидуального соединения необходимо затратить всего 1-2 мин, а время анализа сложной смеси органических соединений в режиме хроматомасс-спектрометрии определяется исключительно хроматографическим временем удерживания компонентов. При этом следует учесть, что в памяти компьютера масс-спектрометра остается информация о всех компонентах смечи, т.е. вводя в прибор 0.1 мкл образца, можно легко получить информацию о его качественном и количественном составе.
В основе метода масс-спектрометрии лежит относительно простая идея: молекулы вещества подвергают ионизации тем или иным способом, образовавшиеся ионы сортируются по величинам их отношения масса/ заряд, затем регистрируется число ионов для каждого значения этого отношения в виде спектра. Например, в широко используемом масс-спектрометре с ионизацией электронным ударом (ЭУ, electron-impact, E1) молекулы в паровой фазе бомбардируются пучком элекгронов с высокой энергией, а результат регистрируется в виде спектра положительных ионов, которые разделены по величинам масса/заряд (m/z).

Рис. 18. Масс-спектр с ионизацией ЭУ бензамида и схема, объясняющая образование главных фрагментных ионов [1]
Для иллюстрации рассмотрим масс-спектр с ионизацией электронным ударом бензамида, показанный на рис. 17 и представляющий диаграмму относительного содержания (высота вертикальных линий) в зависимости от m/z. Пик положительного иона с m/z 121 обусловлен целой молекулой (М), потерявшей при ударной ионизации электронным пучком один электрон. Он называется пиком молекулярного иона и обозначается М·+. Из возбужденного молекулярного иона возникает ряд фрагментных, или осколочных, ионов, образование некоторых из них объяснено на схеме рис. 17.
Обычной практикой является объединение масс-спектрометра с газовым (ГХ-МС) или жидкостным (ЖХ-МС) хроматографом. Масс-спектрометрия широко используется как для анализа соединений с известными масс-спектрами, так и для анализа совершенно новыx соединений. В случае известных соединений компьютерный поиск проводится сравнением их экспериментальных масс-спектров с библиотечными, совпадение спектров является убедительным доказательством идентичности веществ. В случае неизвестного соединения на основе данных по молекулярному иону, характеру фрагментации и других спектроскопических методов (например, ИК и ЯМР) его можно идентифицировать.
Техника эксперимента
В последнее десятилетие происходило быстрое развитие и совершенствование масс-спектрометров. Не обсуждая устройство отдельных моделей приборов, отметим, что они подразделяются по типам в зависимости от способа ионизации и метода разделения ионов.
