
- •Г. Н. Роганов органическая химия Учебно-методическое пособие
- •Часть 2
- •Содержание
- •Часть 1
- •Часть 2
- •5 Карбоновые кислоты
- •5.1 Алифатические карбоновые кислоты
- •5.1.1 Одноосновные насыщенные кислоты
- •5.1.2 Одноосновные ненасыщенные кислоты
- •5.1.3 Двухосновные насыщенные кислоты
- •5.1.4 Двухосновные ненасыщенные кислоты
- •5.2 Ароматические карбоновые кислоты
- •6 Жиры
- •7 Амины
- •7.1 Алифатические амины
- •7.2 Ароматические амины
- •8 Ароматические диазо- и азосоединения, красители
- •9 Гидроксикислоты
- •9.1 Алифатические гидроксикислоты
- •9.2 Оптическая изомерия органических соединений
- •9.3 Ароматические гидроксикислоты (фенолокислоты)
- •10 Аминокислоты, полипептиды
- •10.1 Аминокислоты
- •10.2 Полипептиды
- •11 Альдегидо- и кетокислоты
- •12 Углеводы
- •12.1 Моносахариды
- •12.2 Дисахариды
- •12.3 Полисахариды
- •13 Гетероциклические соединения
- •13.1 Пятичленные гетероциклические соединения
- •13.2 Шестичленные гетероциклические соединения
- •14 Терпены
- •Список использованной литературы
- •Приложение а учебно-методические материалы для самостоятельной работы студентов
- •Продолжение приложения а
- •Продолжение приложения а
- •Приложение б
- •Часть 2
10.2 Полипептиды
Известно, что аминокислоты входят в состав белков. Белки находятся во всех растительных и животных организмах и являются главными носителями жизни (Ф.Энгельс: «Жизнь есть способ существования белковых тел…»).
Несмотря на многочисленность белков, в их состав входят не более 22 разных аминокислот. При гидролизе белок превращается в смесь аминокислот.
Изучение состава, строения и свойств белков составляет предмет последующего курса «Биологическая химия». В рамках курса «Органическая химия» рассмотрим вопросы об основных формах связи аминокислот в сложной молекуле белка и основные принципы химического синтеза полипептидов. Гидролиз природных белков показал, что в их состав входят α-аминокислоты. Ещё в 1891 г. А.Я. Данилевский высказал предположение, что α-аминокислоты связываются в белке за счёт амидных связей, образованных карбоксилом одной молекулы аминокислоты и аминогруппой другой.
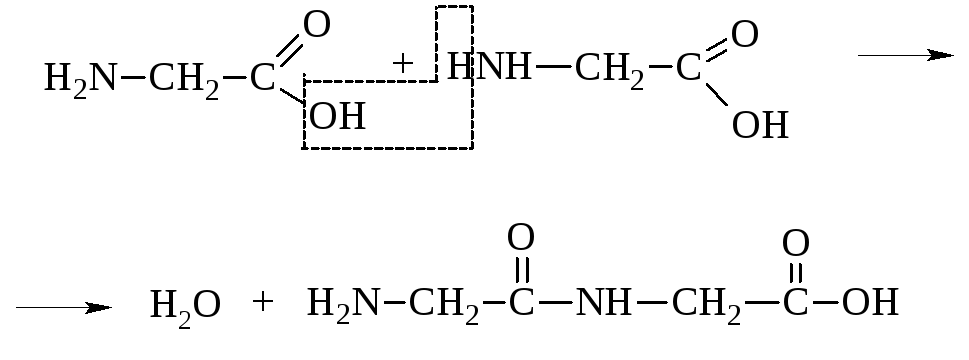
Такого рода связи носят название «пептидных связей». Этим путём могут быть соединены 2,3,4… остатка одинаковых или разных α-аминокислот в виде дипептида, трипептида, тетрапептида и т. д. Такие соединения в общем случае называются полипептидами.
Молекулы полипептидов (белков) в общем случае будут иметь следующую структуру:
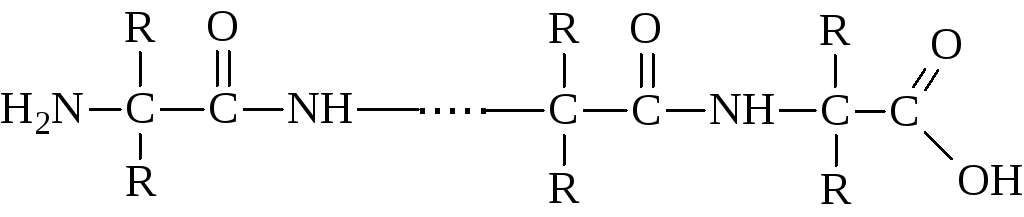
Полипептиды различаются между собой длиной основной цепи, составом и строением радикалов R и последовательностью их чередования в структуре молекулы, иными словами, последовательностью чередования остатков аминокислот. По концам молекулы полипептида расположены карбоксильная и аминогруппы.
Белки построены сложнее полипептидов. Белками называют полипептиды большой молекулярной массы, способные к организации устойчивой пространственной структуры, которой нет у полипептидов. Однако отдельные фрагменты белковой молекулы могут рассматриваться как полипептидные звенья.
Пептиды имеют чрезвычайно важное значение. Пептидные гормоны и нейропептиды, например, регулируют большинство процессов организма человека, в том числе, принимают участие в процессах регенерации клеток. Пептиды иммунологического действия защищают организм от попавших в него токсинов. Для правильной работы клеток и тканей необходимо адекватное количество пептидов. Однако с возрастом и при болезнях возникает дефицит пептидов, который существенно ускоряет износ тканей, приводит к старению всего организма. Сегодня проблему недостаточности пептидов в организме научились решать. Пептидный набор клетки восполняют синтезированными в лабораторных условиях пептидами.
Поскольку природные полипептиды состоят из остатков различных α-аминокислот, при их получении синтетическим путём возникают большие трудности. Во-первых, необходимо выдержать определённую последовательность соединения аминокислот, и во-вторых – избежать соединения двух молекул одной кислоты, остаток которой вводится в пептид при наращивании его цепи.
Первое обстоятельство выполняется при стадийном проведении синтеза. На каждой стадии к полипептиду, полученному на предыдущей стадии, добавляется один аминокислотный остаток и продукт очищается. Однако, из-за большого числа таких стадий и трудоемкости очистки синтез занимает много времени и общий выход конечного продукта чрезвычайно мал. Действительно, первый полный синтез пептида, гормона окситоцина (1953 г.), содержащего всего 8 амино-кислотных остатков, рассматривался как выдающееся достижение, принесшее его автору, В. дю Виньо, Нобелевскую премию 1955 года.
Следует отметить, что две различные аминокислоты могут образовывать четыре дипептида. Так, в смеси глицина и аланина образуются следующие дипептиды:
 Количество
дипептидов резко возрастает с увеличением
числа участвующих в их образовании
неодинаковых аминокислот.
Количество
дипептидов резко возрастает с увеличением
числа участвующих в их образовании
неодинаковых аминокислот.
Для того, чтобы избежать произвольного соединения остатков аминокислот, в том числе и одинаковых, применяют специальные приемы пептидного синтеза: защиту (блокирование) одних функциональных групп и активацию других.
Так, чтобы в смеси глицина и аланила однозначно получался только первый дипептид (глицилаланин), необходимо заблокировать аминогруппу глицина и карбоксильную группу аланина. Образование остальных трех дипептидов становится невозможным. Желательно при этом активировать кислотную группу глицина, переведя ее, например, в хлорангидридную, и аминогруппу аланина.
При синтезе полипептидов, содержащих большое число аминокислотных остатков, требуется проведение множества реакций, которые сопровождаются однотипными операциями по выделению и очистке продукта на каждой стадии, что сопряжено с большими затратами времени. Для решения этих проблем был предложен твердофазный синтез пептидов на полимерной матрице (Меррифилд, 1962 г., Нобелевская премия). В настоящее время созданы автоматические приборы (синтезаторы), которые в запрограммированной последовательности осуществляют все необходимые операции. Эти методики используются, например, для получения гормона инсулина, необходимого больным диабетом для снижения содержания сахара в крови.
