
- •Задача 2
- •3. В аптеку поступил рецепт для приготовления микстуры следующего состава:
- •Задача 8
- •4. В таблеточном цехе на подготовительном этапе порошок лекарственной субстанции подвергли измельчению.
- •5. В аптеку часто поступают рецепты на изготовление порошков, содержащих указанное лекарственное вещество, по прописи:
- •Задача 13
- •2. В аптеке данное лекарственное вещество может быть использовано при изготовлении микстуры следующего состава:
- •5. Предложите оптимальную технологическую и аппаратурную схему производства настойки.
- •Задача 14
- •Задача 15
- •4. В каком помещении аптеки осуществляют процесс изготовления глазных капель? Какие другие лекарственные формы требуют аналогичных условий изготовления? Ответ обоснуйте.
- •Задача 16
- •1. На производственной практике студент обратил внимание на то, что в аптеке с большим трудом реализуются требования, предъявляемые государственной фармакопеей к лекарственной форме «Суспензии».
- •2. Предложите технологические приемы, обеспечивающие агрегативную устойчивость суспензии в условиях промышленного производства?
- •Задача 17
- •3. Удобной лекарственной формой, содержащей данное лекарственное средство, является бактерицидный лейкопластырь.
- •Технологическая схема производства лейкопластырей
- •4. В аптеке из данного лекарственного вещества готовят раствор следующего состава:
- •Задача 19
- •2. В условиях промышленного производства получают таблетки с лекарственным веществом, формула которого приведена выше.
- •Технологическая схема производства таблеток методом прямого прессования
- •3. В аптеку поступил рецепт на изготовление лекарственного средства следующего состава:
- •Задача 22
- •2. Дайте сравнительную характеристику настойкам как лекарственной форме (состав, стабильность, эффективность и др.).
- •Технологическая схема производства настоек методом перколяции
- •4. В аптеке изготовлена внутриаптечная заготовка порошков по прописи:
- •Задача 26
- •I. В период эпидемии гриппа в аптеку обратился больной за препаратом «Антигриппокапс» следующего состава: Состав на одну капсулу:
- •3. Дайте сравнительную характеристику лекарственной форме «капсулы». Перечислите факторы, влияющие на качество капсул.
- •Технологическая схема производства твердых желатиновых капсул методом погружения
- •Задача 34
- •2. В условиях фармацевтического производства для получения сока используют листья подорожника большого свежие.
- •Основные этапы получения соков:
- •Технологическая схема получения соков
- •5. В аптеку поступил рецепт для изготовления порошков по прописи:
- •Задача 39
- •2. В аптеке глазные мази с лекарственным веществом указанной структуры 0,5%-й или 1%-й концентрации по 10,0 г изготавливают в качестве, внутриаптечной заготовки.
- •5. На фармацевтическом производстве из лекарственного растительного сырья плоды облепихи готовят препарат «Облепиховое масло».
- •Задача 42
- •2. В аптеку поступил рецепт на изготовление сиропа мятного по следующей прописи:
- •4. Дайте классификацию сиропов. Предложите оптимальную технологическую и аппаратурную схему промышленного производства сиропов.
- •Технологическая схема производства сиропа сахарного
- •Задача 48
- •3. В аптеку поступил рецепт на изготовление микстуры с экстрактом плодов боярышника:
- •4. В условиях фармацевтического производства получают жидкий экстракт боярышника.
- •Технологическая схема производства жидких экстрактов-концентратов
- •Задача 54
- •3. В аптеку поступил рецепт на экстемпоральное изготовление микстуры по следующей прописи:
- •4. В условиях фармацевтического производства получают настойки пустырника и валерианы.
- •4. В условиях фармацевтического производства выпускаются лекарственные средства, содержащие экстракт сенны или сумму сеннозидов а и б в виде драже или таблеток, покрытых оболочкой.
- •Задача 60
- •1. Практикант представил для проверки провизору-технологу (куратору производственной практики в аптеке) план изготовления мази по прописи:
- •Технологическая схема производства мазей
- •2. Реактор - смеситель
- •Задача 62
- •3. Обоснуйте требования к стерильным лекарственным формам в соответствии с требованиями gmp. Укажите классы чистоты помещений и технологические приемы, обеспечивающие чистоту помещений.
- •Технологическая схема производства глазных капель в тюбик – капельницах (флаконах)
- •Задача 64
- •2. Охарактеризуйте стабильность кислоты аскорбиновой в водном растворе.
- •3. Проведите сравнительную оценку различным способам стерилизации инъекционных растворов в промышленном производстве.
- •Задача 68
- •3. В аптеке лпу из-за отсутствия раствора промышленного производства возникла необходимость изготовления инъекционного раствора кофеин-бензоата натрия.
- •5. В условиях крупного фармацевтического производства предложите технологические и аппаратурные схемы наполнения ампул раствором с учетом физико-химических свойств инъекционных растворов.
- •6. Составьте и обоснуйте технологическую и аппаратурную схему промышленного производства водного медицинского раствора.
- •Технологическая схема производства растворов
- •Задача 71
- •3. Проверьте осмотическую активность 2%-го раствора пилокарпина гидрохлорида.
- •Задача 74
- •Технологическая схема производства инъекционных растворов в ампулах
- •Задача 76
- •6. Дайте характеристику лекарственной формы «Инъекционные растворы».
- •Задача 80
- •1. На крупном фармацевтическом предприятии получили 1000 л сиропа по прописи:
- •Задача 89
- •6. В условиях крупного фармацевтического производства:
- •Особенности технологии неводных растворов на нелетучих растворителях
- •Изготовление глицериновых растворов
- •Изготовление масляных растворов
- •Особенности изготовления растворов на димексиде
- •Задача 93
- •4. Охарактеризуйте основные группы вспомогательных веществ, используемые в промышленном производстве таблеток.
- •Вспомогательные вещества.
- •Задача 95
- •3. Обоснуйте особенности изготовления водных извлечений из названных Вами видов сырья.
- •Задача 101
- •1. В аптеке витаминные глазные капли состава:
- •5. В условиях фармацевтического производства выпускаются лекарственные средства - драже, содержащие витамины.
- •Задача 103
- •2. Руководствуясь нд, предложите оптимальный вариант технологии изготовления 5%-го спиртового раствора левомицетина.
- •3. Предложите и обоснуйте технологическую и аппаратурную схему производства 5%-ного спиртового раствора левомицетина в условиях промышленного производства.
- •Задача 104
- •5. Предложите и обоснуйте технологическую и аппаратурную схемы промышленного производства гранул как лекарственной формы.
- •Задача 112
- •3. На основании теоретических и практических основ организации производства экстракционных фитопрепаратов:
- •Задача 120
- •2. Предложите методы стабилизации инъекционных растворов легко-окисляющихся веществ в промышленном производстве и их хранение. Укажите механизм стабилизации.
- •Задача 122
- •Задача 126
- •1. В рецептурно-производственный отдел аптеки поступил рецепт:
- •Задача 129
- •1. Студенту, проходящему производственную практику в аптеке, было предложено изготовить препарат по прописи;
- •Задача 130
- •1. В рпо аптеки поступил рецепт:
- •5. В состав данной лекарственной формы входит сухой экстракт красавки.
- •Задача 133
- •Задача 135
- •Особенности изготовления суппозиториев методом выливания:
Технологическая схема производства инъекционных растворов в ампулах
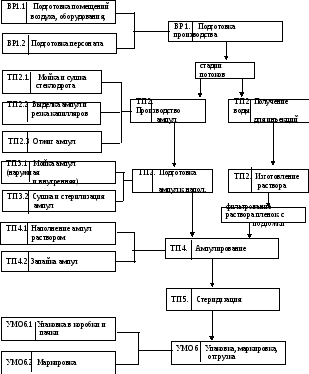
Задача 76
2. Для изготовления в аптеках в условиях малосерийного производства утверждены суппозитории детские с эуфиллином «Suppositoria rectalia cum Euphyllino 0,05 seu 0,1 pro infantibus» (МУ 13-003-92). В качестве основы предложен твердый жир тип А (?) или масло какао. Масса свечи 1,35-1,37 г, 1/Е эуфиллина - 0,8. Срок хранения при Т не > 5°С - 6 мес.
• Рассчитайте количество лекарственного вещества и основы для изготовления суппозиториев с концентрацией эуфиллина 0,1 методом выливания в формы.
• Обоснуйте технологию изготовления.
Выписана мягкая ЛФ, ректальные суппозитории с веществом, растворимым в воде.
Оборотная сторона ППК:
Масса свечи 1,36
На 10 свечей 1,36*10=13,6
Масса эуфиллина 1,0
Масса основы жировой 13,6-1*0,8=12,8 (с учетом коэффициента замещения)
Технология изготовления:
В ступке растираем эуфиллин с небольшим количеством воды. На водяной бане расплавляем жировую основу и постепенно добавляем лекарственное вещество из ступки и помешиваем. Затем выливаем свечи в формы, смазанные мыльным спиртом
6. Дайте характеристику лекарственной формы «Инъекционные растворы».
• Объясните понятие о стерильной серии. Укажите способы стерилизации инъекционных растворов. Дайте сравнительную характеристику предложенных способов.
• Объясните сущность механической стерилизации. Назовите фильтрующие материалы и установки
Инъекционные лекарственные формы или лекарственные средства для парентерального применения, являются официнальными. К лекарственным средствам для парентерального применения относятся стерильные водные и неводные растворы, суспензий, эмульсий и сухие твердые вещества (порошки, пористые массы, таблетки), которые растворяют в стерильном растворителе непосредственно перед применением. Растворы для парентерального применения объемом 100 мл и более относятся к инфузионным.
В качестве растворителей применяют воду для инъекций, жирные масла, этилолеат. В основе комплексного растворителя могут быть использованы спирт этиловый, глицерин, пропиленгликоль, полиэтиленоксид 400, бензилбензоат, бензиловый спирт, другие растворители.
При изготовлении лекарственных средств для парентерального применения могут использоваться вспомогательные вещества: консерванты, антиоксиданты, стабилизаторы, эмульгаторы, солюбилизаторы и другие. Консерванты применяют в многоразовых средствах для парентерального применения, а также в одноразовых препаратах,в соответствии с частными фармакопейными статьями (ФС). Лекарственные средства для внутриполостных, внутрисердечных, внутриглазных или других инъекций, имеющих доступ к спинномозговой жидкости, а также при разовой дозе, превышающей 15 мл, не должны содержать консервантов. Количество добавляемых вспомогательных веществ, если нет других указаний в частных ФС, не должно превышать следующих концентраций: для консервантов подобных хлорбутанолу, крезолу, фенолу — до 0,5 %, антиоксидантов типа сернистого ангидрида или эквивалентных количеств сульфита, бисульфита или метабисульфита калия и натрия — до 0,2 %.
В технологии лекарственных форм промышленного производства в настоящее время используют 3 группы методов стерилизации:
механические;
химические;
- физические
Механические методы стерилизации
Стерилизующая фильтрация.* Микробные клетки и споры можно рассматривать как нерастворимые образования с очень малым (1—2 мкм) размером частиц. Подобно другим включениям, они могут быть отделены от жидкости механическим путем — фильтрованием сквозь мелкопористые фильтры. Этот метод стерилизации включен в ГФ XI для стерилизации термолабильных растворов.
Химическая стерилизация подразделяется на стерилизацию растворами (веществами) и стерилизацию газами (газовая стерилизация).
Физические методы стерилизации
Тепловая (термическая) стерилизация. В настоящее время монопольное положение среди возможных методов стерилизации в фармацевтическом производстве занимает тепловая стерилизация.
В зависимости от температурного режима тепловая стерилизация подразделяется на стерилизацию:
паром под давлением (автоклавирование);
текучим паром;
тиндализацию;
воздушную.
Микробные клетки и споры можно рассматривать как нерастворимые образования с очень малым (1—2 мкм) размером частиц. Подобно другим включениям, они могут быть отделены от жидкости механическим путем — фильтрованием сквозь мелкопористые фильтры. Этот метод стерилизации включен в ГФ XI для стерилизации термолабильных растворов. -
По механизму действия фильтрующие перегородки, используемые для стерильной фильтрацииУподразделяют на глубинные и поверхностные (мембранные) с размером пор не более 0,3 мкм.
Глубинные фильтры характеризуются сложным механизмом задержания микроорганизмов (ситовым, адсорбционным, инерционным). .Ввиду большой толщины таких фильтров удерживаются и частицы меньшего размера, чем размер пор фильтрующей перегородки.
Глубинные фильтры классифицируют на: керамические и фарфоровые (размер пор 3—4 мкм), стеклянные (около 2 мкм), бумажно-асбестовые (1 — 1,8 мкм). Недостатками керамических и фарфоровых фильтров является продолжительность стерилизации, потеря раствора в порах толстого фильтра, образование микротрещин из-за хрупкости материала и, следовательно, ненадежность стерилизации.
Так, стеклянные и бумажно-асбестовые фильтры несовершенны. Стеклянные фильтры малопроизводительны, бумажно-асбестовые фильтры не рекомендуются для стерилизации инъекционных растворов, поскольку они состоят из волокнистых материалов и имеется угроза отрыва волокон от фильтра. Попадая в организм с раствором, такие волокна могут вызывать различные патологические реакции.
В последние годы большое распространение для стерилизующей фильтрации получили микропористые мембранные фильтры. Они лишены недостатков, присущих стеклянным и бумажно-асбестовым фильтрам.
Мембранные фильтры представляют собой тонкие (100— 150 мкм) пластины из полимерных материалов, характеризующиеся ситовым механизмом задержания микроорганизмов и постоянным размером пор (около 0,3 мкм). Во избежание быстрого засорения фильтра мембраны используют в сочетании с префильтрами, имеющими более крупные поры. При стерилизации больших объемов растворов оптимальным является применение фильтров обоих типов.
Использование глубинных и мембранных фильтров обеспечивает необходимую чистоту, стерильность и апирогенность раетворов для инъекций.
Стерилизующая фильтрация имеет преимущества по сравнению с методами термической стерилизации. Для многих растворов термолабильных веществ (апоморфина гидрохлорид, викасол, барбитал натрия и другие) его признают единственно доступным методом стерилизации. Метод весьма перспективный в производстве глазных капель.
