
Молекулярная физика (11-18)
.pdfУДК 53 (075) П 27
ББК 22.3 Я7
Перфильева, Э.А. Определение отношения теплоёмкостей газа по скор о- сти звука в газе. [Текст]: метод. указания/ Э.А. Перфильева. – Ухта: УГТУ, 2007. – 11 с.: ил.
Методические указания предназначены для выполнения контрольных р а- бот по теме «Молекулярная физика» для студентов специальностей 290700, 290300 и направлению 550100.
Содержание методических указаний соответствует рабочей учебной пр о- грамме. Методические указания рассмотрены и одобрены кафедрой физики от 19.02.07., пр. № 5 .
Рецензент: Серов И.К., доцент кафедры физики Ухтинского государственного технического университета
Редактор: Северова Н.А., доцент кафедры физики Ухтинского государствен ного технического университета
В методических указаниях учтены предложение рецензента и редактора.
План 2007 г., позиция |
41. |
|
|
Подписано в печать |
04.06.2007. |
|
|
Компьютерный набор: Протасов Иван, гр. ИСТ -05. |
. |
||
Обьем 11 с. Тираж 60 экз. |
Заказ № 211. |
|
|
© Ухтинский государственный технический университет, 200 7 169300, г. Ухта, ул. Первомайская, 13 .
Отдел оперативной полиграфии УГТУ. 169300, г. Ухта, ул. Октябрьская, 13.
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ ГАЗА ПО СКОРОСТИ ЗВУКА В ГАЗЕ
Краткая теория
Вследствие того, что молекулы идеального газа на расстоянии не взаим о- действуют друг с другом, внутренняя энергия такого газа будет складываться из энергии отдельных молекул. След овательно, внутренняя энергия одного моля идеального газа будет равна произведению числа Авогадро на среднюю энергию одной молекулы:
Uм NA |
i |
NAkT |
i |
RT. |
(1) |
|
|
||||
2 |
2 |
|
|
||
ί – число степеней свободы молекулы
k – постоянная Больцмана, NА – число Авогадро, число молекул в 1 моле. Внутренняя энергия произвольной массы газа m будет равна внутренней энергии одного моля, умноженной на число молей газа, содержащихся в массе
m:
U mUм m |
i |
RT. |
(2) |
|
|
||||
M |
M 2 |
|
|
|
R – молярная газовая постоянная.
Теплоемкостью какого-либо тела называется величина, численно равная количеству теплоты, которое нужно сообщить телу, чтобы повысить его темп е- ратуру на один градус.
Cтела |
dQ . |
(3) |
|
dT |
|
Величина (3) имеет размерность Дж/К. |
|
|
Теплоемкость моля вещества мы |
будем обозначать буквой |
C (C - |
большое). Размерность C равна Дж/моль·К.
Теплоемкость единицы массы вещества называется удельной теплоемк о- стью. Ее мы будем обозначать буквой c (c -малое). Размерность c равна
Дж/К··кг.
Между молярной и удельной теплоемкостью вещества имеется очевидное
соотношение: |
|
|
|
c |
C |
. |
(4) |
|
|||
|
M |
|
|
М – молярная масса газа
3
Величина теплоемкости зависит от условий, при которых происходит н а- гревание тела. Наибольший интерес предс тавляет теплоемкость при постоянном объеме Cv или при постоянном давлении C p , когда нагревание происходит
при постоянном объеме или при постоянном давлении. Согласно первому началу термодинамики количество теплоты, сообщенное газу, идет на приращение внутренней энергии и на работу расширения газа.
dQ = dU + dА
Если нагревание происходит при постоянном объеме, тело не совершает работы над внешними телами и, следовательно, вся теплота идет на приращение внутренней энергии тела:
dQv dU . |
(5) |
Из (5) вытекает, что теплоемкость любого тела при постоянном объеме |
|
равна: |
|
Cv dU . |
(6) |
dT |
|
Следовательно, чтобы получить теплоемкость моля идеального газа при постоянном объеме, нужно продифференцировать по температуре выраж ение
(1) для внутренней энергии газа. Произведя дифференцирование, получим:
Cv |
i |
R . |
(7) |
|
|||
2 |
|
|
|
Как следует из этого выражения, молярная теплоемкость идеального газа при постоянном объеме оказывается постоянной величино й, не зависящей от параметров состояния газа, в частности от температуры.
Заметим, что с учетом (7) выражение для внутренней энергии 1 моля идеального газа может быть записано в следующем виде:
Uм = Сν · ∆T. (8) Если нагревание газа происходит при постоянном давлении, то газ будет расширяться, совершая над внешними телами положительную работу. Следов а- тельно, для повышения температуры газа на один градус в этом случае понад о- бится больше тепла, чем при нагревани и при постоянном объеме, т.к. допол нительно теплота будет затрачиваться на совершение газом работы. Поэтому те п- лоемкость при постоянном давлении должна быть больше, чем при постоянном
объеме на работу расширения.
4

Напишем уравнение первого начала термодинамики для одного моля га-
за:
dQм dUм pdVм . |
(9) |
||||
где dА = pdV |
|
|
|
|
|
Cp |
dU |
|
dV |
|
(10) |
|
м p |
м . |
|||
|
dT |
dT p |
|
||
Слагаемое dUdTм дает, как мы видим, молярную теплоемкость газа при
постоянном объеме. Поэтому формула (10) может быть записана следующим образом:
|
|
|
Cp Cv |
dV |
|
(11) |
|
|
|
|
p |
|
м . |
||
|
|
|
|
|
dT p |
|
|
dV |
|
представляет собой приращение объема моля при по- |
|||||
Величина |
|
м |
|||||
|
dT p |
|
|
|
|
|
|
вышении температуры на один градус, получающееся в случае, если |
p посто- |
||||||
янно. В соответствии с уравнением состояния : (pV =ν RT) |
|
||||||
объем одного моля: (ν=1) |
|
|
|
|
|||
|
|
|
Vм |
RT . |
|
|
|
|
|
|
|
p |
|
|
|
Дифференцируя это выражение по T ( p const ), находим:
dV |
|
R |
. |
|
|
м |
p |
|
|
dT p |
|
|
||
Наконец подставляя этот результат в (11), получаем: |
|
|||
C p |
Cv |
R . |
(12) |
|
Таким образом, работа, которую совершает один моль идеального газа при повышении его температуры на один градус при постоянном давлении, оказывается равной молярной газовой постоянной.
Отметим, что соотношение (12) получено с использованием уравнения идеального газа и, следовательно, справедливо только для идеального газа.
С учетом формулы (7) можно получить для C p следующее выражение:
C p |
i |
R R |
i 2 |
R . |
(13) |
|
|
||||
2 |
2 |
|
|
||
5

Поделив (13) на (12), найдем характерное для каждого газа отношение C p к Cv :
|
C p |
|
i 2 |
. |
(14) |
|
Cv |
i |
|||||
|
|
|
|
Как следует из (14), величина определяется числом и характером степ е- ней свободы i . При жесткой связи молекул учитываются только поступател ь- ные и вращательные степени свободы. Так ка к, в составе воздуха кислород О2 и азот N2 (2-х атомные газы), принимаются i in iвр 3 2 5
Звуковые волны в газах и жидкостях являются продольными. В твердых телах могут распространятся как продольные, так и поперечные звуковые во л- ны. Скорость их распространения (скорость звука) зависит от упругих свойств среды и плотности и определяется формулой :
|
|
|
|
Vпр |
E |
, |
(15) |
|
|
|
|
где - плотность среды, E - модуль продольной упругости.
Процесс распространения звуковых волн в газах схематически можно представить следующим образом: источник механических колебаний передает эти колебания окружающим его газовым молекулам: в результате изменяется давление газа в данной микрообласти пространства. Так как газ обладает упр у- гими свойствами, то он немедленно расширяется и в данном элементарном объеме газа образуется разрежение, а микрообласть повышенного давления п е- ремещается несколько дальше от источника звука и т.д. Процессы сжатия и разряжения протекают очень быстро, поэтому изменение давления газа прои с- ходит без теплообмена.
Так как для газов модуль продольной упругости связан с давлением соо т- ношением:
|
E P , |
|
||
то для скорости звука в газе можно записать : |
|
|||
|
|
|
. |
|
|
|
|
(16) |
|
|
|
|
|
|
Выразив из уравнения Клапейрона – Менделеева:
6
pV m RT, |
(17) |
||||
|
M |
|
|
||
плотность газа и подставив в (16), получим: |
|
||||
|
|
|
|
|
|
|
|
RT |
|
, |
(18) |
|
M |
||||
|
|
|
|
||
откуда |
|
|
|
|
|
|
M . |
|
(19) |
||
|
|
RT |
|
|
|
Таким образом, для определения отношения теплоемкостей газа надо и з- мерить температуру газа и определить скорость звука в газе.
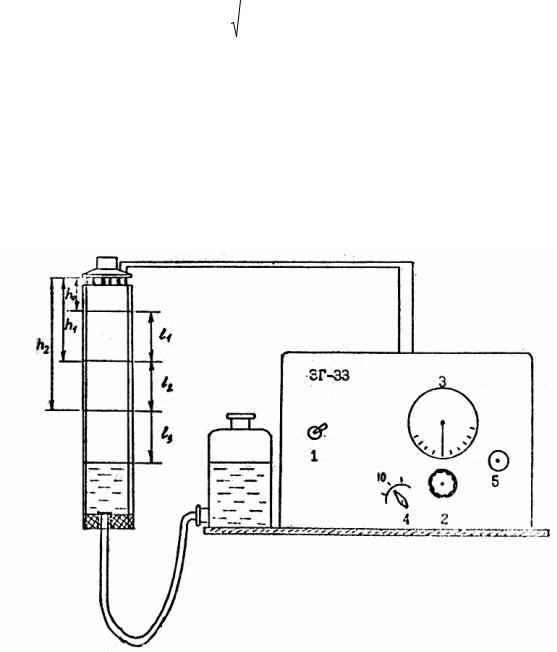
Установка для определения скорости звука в газе (рис. 1) состоит из звукового генератора, динамика и вертикальной трубы с водой, уровень которой можно менять с помощью соединенного с ней сосуда.
Рис. 1.
Звуковой генератор заставляет колебаться мембрану динамика с опред е- ленной фиксированной частотой . В результате возникают звуковые волны определенной длины , которые распространяются во все стороны от динам и- ка.
7
Звуковая волна, отраженная поверхностью воды в трубе возвращается о б- ратно к мембране динамика. В ре зультате амплитуда колебаний мембраны или увеличивается или уменьшается.
Усиление колебаний мембраны произойдет в том случае, если отраженная волна подойдет к плоскости мембраны в той же фазе, в которой находится в данный момент времени сама мембрана. Совп адение фаз сопровождается заметным усилением звука.
Пусть уровень воды в трубе находился в самом верхнем положении. При медленном опускании уровня можно заметить несколько его положений ( h0 , h1, h2 и т.д.), при которых происходит усиление звук а. Очевидно, что расстояние l между ближайшими уровнями усиление звука равно половине длины волны, т.к. усиление колебаний происходит только тогда, когда разность хода 2-х волн равна целому числу длин волн.
Таким образом, для определения длины волны , соответствующей данной частоте , необходимо определить расстояние между двумя ближайшими уровнями воды, дающими усиление звука, и удвоить его, т.е. 2l , где:
l h1 h0 h2 h1 h2 h2 ...
Скорость звука υ может быть определена через частоту и длину волны п о- средством соотношения:
υ = λν . |
|
|
(20) |
|
Подставляя найденное значение V в формулу (19) получим окончател ь- |
||||
ную формулу для отношения теплоемкостей : |
|
|
||
|
4 2l2 |
|
. |
(21) |
RT |
|
|||
|
|
|
|
|
Выполнение работы
Целью работы является определение отношения теплоемкостей для во з-
духа.
Работа выполняется в следующей последовательности:
1.Тумблером 1 «сеть» включить звуковой генератор и подо ж- дать 2-3 минуты, пока он прогреется.
2.Ручкой установки частоты 2 установить на круглой частотной шкале 3 одну из частот, заданных преподавателем в диапазоне 600 -1200
8

Гц. Для этого при положении переключателя множителя 4 в положении 10 установить против неподвижного штриха одно из чисел из инт ервала 60-120. С учетом множителя 10 это и будет заданная частота выну ж- денных колебаний мембраны динамика.
3.После того, как прибор прогреется, ручкой «Регулятор вых.» 5 установить минимальную громкость звука с тем, чтобы не мешать о с- тальным работающим в лаборатории.
4.Изменяя уровень воды в трубе от самого низкого до самого высокого и наоборот, найти и записать в таблицу высоту воздушного столба ( h0 , h1, h2 ), при которой громкость звука заметно возрастает. З а-
пись высот производить начиная с наибольшей высоты.
Т.к. для измерения длины волны берется абсолютное значение разности высот h1 h0 , h2 h1 и т.д., то не имеет значения где находится нулевая отметка шкалы. Отсчет можено вести как от динамика так и от любого конца трубы.
5.Закончив измерения с одной частотой, перейти на следу ю- щую и повторить измерения высот в той же последовательности.
6.Проведя все измерения, выключить звуковой генератор тумблером «сеть».
7.Измерить и записать в таблицу температуру воздуха вблизи установки.
8.По данным таблицы найти отрезки l1,l2 ,l3... и вычислить их
среднее значение.
9.По формуле (21) вычислить для каждого опыта. Найти среднее значение .
10.По формуле:
|
|
|
2 |
|
l 2 |
|
2 |
|
R 2 |
|
T |
2 |
|
||
|
4 |
|
|
4 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
l |
|
|
|
R |
T |
|
|
|||
|
|
|
|
|
|||||||||||
вычислить относительную погрешность δ затем и абсолютнуюср по результатам одного из опытов.
9

|
Таблица измерений и вычислений |
|
|
|
|
|
|
Номер опыта |
1 |
2 |
3 |
|
|
|
|
Измеряемые |
Численное |
значение измеряемой величин ы |
|
величины |
|
( x x ) |
|
|
|
|
|
Т |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
h0 |
|
|
|
|
|
|
|
h1 |
|
|
|
|
|
|
|
h2 |
|
|
|
|
|
|
|
h3 |
|
|
|
|
|
|
|
h4 |
|
|
|
|
|
|
|
h5 |
|
|
|
|
|
|
|
l1 |
|
|
|
|
|
|
|
l2 |
|
|
|
|
|
|
|
l3 |
|
|
|
|
|
|
|
l4 |
|
|
|
|
|
|
|
lср |
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ср |
|
|
|
|
|
|
|
Контрольные вопросы
1.Дайте определение теплоемкости тела и удельной теплоемкости вещества.
2.Как связаны удельная и молярная теплоемкости?
3.Что такое Cp иCv ?
4.Почему всегда больше единицы?
10
5.Каково ожидаемое значение для воздуха, если считать, что
воздух представляет собой смесь двухатомных газов?
6.К какому типу волн относятся звуковые волны?
7.Объясните назначение воды в данной работе.
Индивидуальные задания
1.Вычислить удельные теплоёмкости cp и cv газов: 1) гелия; 2) водорода; 3) углекислого газа. Ответ : 1) 3,12 кДж / ( кг · К ), 5,29 кДж / ( кг · К ); 2) 10,4 кДж / ( кг · К ), 14,6 кДж / ( кг · К ); 3) 567 Дж / ( кг · К ), 756 Дж / ( кг · К ).
2.Разность удельных теплоёмкостей cp - cv некоторого двухатомного газа равна 266 Дж / ( кг · К ). Найти молярную массу М газа. Ответ : 0,032 кг / моль.
3.Каковы удельные теплоёмкости cp и cv смеси газов , содержащей ки-
слород |
массой m1 = 10 г и азот массой m2 = 20 г ? Ответ : 715 Дж / ( кг · К ). |
|
4. |
Водород массой m = 4 г был нагрет на ∆Т = 10 |
К при постоянном дав- |
лении. Определить работу А расширения газа. Ответ : |
166 Дж. |
|
5. |
Азот массой m = 5 кг, нагретый на ∆Т = 150 К, сохранил постоянный V |
|
. Найти : 1) количество теплоты Q , сообщенное газу; 2) изменение ∆U внутренней энергии ; 3) совершённую газом работу А . Ответ: 67 кДж, 0
6.При изохорном нагревании кислорода объёмом V = 50 л давление газа изменилось на ∆р = 0,5 МПа. Найти количество теплоты Q , сообщенное газу. Ответ : 62,5 кДж.
7.Воздух массой m = 29 г нагрели на ∆Т = 200 К, причем газу было передано количество теплоты Q = 10 кДж. Найти изменение ∆U внутренней энергии газа и совершенную им работу А . Ответ : 4,2 кДж; 6,8 кДж.
Библиографический список
Трофимова Т.И. Курс физики: – M.: Высшая шк. 2000. – Гл.9., § 50-54.
11
