
- •Інструментальні методи аналізу Особливості фізико-хімічних методів аналізу
- •2. Спектральні (оптичні) методи аналізу
- •Оптичні методи аналізу
- •2.1. Загальні принципи оптичної спектроскопії
- •2.2. Класифікація спектрів
- •2.3. Емісійний спектральний аналіз
- •2.4. Структура і характеристика елементів спектральних приладів
- •2.5. Якісний емісійний спектральний аналіз
- •2.5.1. Способи визначення довжин хвиль
- •2.6. Кількісний аналіз
- •2.7. Полум’яно-фотометричний аналіз
- •2.8. Молекулярно-абсорбційні методи аналізу
- •2.8.1. Якісний аналіз
- •2.8.1.1. Закон Бугера-Ламберта-Бера
- •2.8.1.2. Відхилення від закон Бугера-Ламберта-Бера
- •2.8.3. Схема приладів для вимірювання спектра поглинання
- •2.8.4. Кількісний фотоколориметричний аналіз
- •2.8.5. Турбідиметрія, нефелометрія
- •3. Хроматографічні методи аналізу
- •3.1. Загальна характеристика та класифікація хроматографічних методів аналізу
- •3.2. Принципова схема газового хроматографа
- •3.3. Хроматограма та її характеристики
- •3.4. Теоретичні основи хроматографічного розділення
- •3.4.1. Теорія рівноважної газової хроматографії
- •3.4.2. Теорія нерівноважної хроматографії
- •3.4.3. Теорія тарілок
- •3.5. Розділювальна здатність хроматографічної колонки
- •3.5.1. Основні фактори, що впливають на розділювальну здатність колонок
- •3.6. Якісний хроматографічний аналіз
- •3.7. Кількісний хроматографічний аналіз
- •4. Електрохімічні методи аналізу
- •4.1. Потенціометричні методи аналізу
- •4.1.1. Класифікація електродів. Аналітичний сигнал
- •Порівняльна характеристика електродів
- •Характеристики основних електродів порівняння
- •4.1.2. Способи проведення аналізу в потенціометрії
- •4.2. Кондуктометричні методи аналізу
- •4.2.1. Види електричної провідності
- •4.2.2 Пряма кондуктометрія
- •4.2.3. Кондуктометричне титрування
- •4.3. Кулонометричні методи аналізу
- •4.3.1. Пряма кулонометрія
- •4.3.2. Кулонометричне титрування
- •5. Полярографічні методи аналізу
- •5.1. Види поляризації
- •5.2. Принципова схема полярографічної установки
- •5.3. Полярографічна хвиля
- •5.4. Якісний полярографічний аналіз
- •5.5. Кількісний полярографічний аналіз
- •5.6. Причини спотворення форми полярограм
- •5.7. Амперометричне титрування
- •5.8. Інверсійна вольтамперометрія
- •5.8.1. Анодна інверсійна вольтамперометрія
- •Опис приладу для інверсійної вольтамперометрії марки акв-07мк
5.4. Якісний полярографічний аналіз
Якісний полярографічний аналіз грунтується на вимірюванні потенціалу півхвилі йону, який відновлюється. Потенціалом півхвилі називається потенціал, при якому досягається сила струму, яка дорівнює половині граничного дифузійного струму. Потенціал півхвилі позначається – Е1/2 і залежить від природи іону, який відновлюється, природи і концентрації фонового електроліта, pH розчину і не залежить від концентрації йону. Потенціали півхвиль різних неорганічних і органічних речовин у фонових електролітах різного складу виміряні експериментально і наводяться в довідниковій літературі.
Процедура якісного аналізу полягає у фіксуванні полярограми досліджуваного розчину у певному фоновому електроліті, вимірюванні потенціалу півхвилі і пошуку у довідникових даних речовини, потенціал півхвилі якої у цьому ж фоні дорівнює виміряній величині потенціалу півхвилі.
Потенціал півхвилі можна виміряти графічно, провівши дотичні прямі через експериментальні точки дифузійного струму в межах полярографічної хвилі, а також до і після хвилі. Дві точки перетину цих прямих відповідають граничному дифузійному струму. Відрахувавши потенціал, який відповідає половині відстані між точками перетину, вимірюють потенціал півхвилі визначуваного іону.
Точніше визначити потенціал півхвилі можна з допомогою рівняння полярографічної хвилі для оборотних процесів Гейровського-Ільковича:
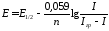 ,
,
де I - сила струму у будь-якій точці полярографічної хвилі.
Якщо побудувати графік залежності lgI/(Iгр - I) від Е, то одержимо пряму лінію, яка перетинає вісь абсцис (рис. 5.2).
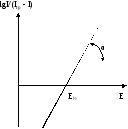
Рис. 5.2. Вольтамперна крива в напівлогарифмічних координатах
При наявності в розчині декількох йонів можлива окрема ідентифікація, якщо їх потенціали півхвилі відрізняються не менше ніж на 0,2 В. Якщо потенціали півхвилі в одному фоні відрізняються недостатньо, для окремої ідентифікації можна замінити фоновий електроліт.
5.5. Кількісний полярографічний аналіз
Кількісний полярографічний аналіз грунтується на залежності граничного дифузійного струму від концентрації визначуваної речовини, яка виведена Ільковичем:
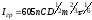
де Ігр - сила граничного дифузійного струму, мка, С - концентрація визначуваної речовини, ммоль/л, D - коефіцієнт дифузії, см2/c, m - швидкість витікання ртуті, мг/с, τ – період капання ртуті, с.
Добуток
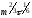 називається
характеристикою капіляра. Він залежить
від діаметра і довжини капіляра, висоти
підйому напірної посудини і температури.
Ця величина легко визначається
експериментально і при постійних
параметрах установки є сталою.
називається
характеристикою капіляра. Він залежить
від діаметра і довжини капіляра, висоти
підйому напірної посудини і температури.
Ця величина легко визначається
експериментально і при постійних
параметрах установки є сталою.
Концентрацію речовини можна визначити різними способами.
1. Розрахунковий спосіб полягає у фіксуванні полярограми, визначенні граничного дифузійного струму і розрахунку концентрації за рівнянням Ільковича.
Для використання цього простого способу необхідно крім визначення характеристики капіляра знати коефіцієнт дифузії, точне значення якого не завжди відоме, тому цей метод в аналітичній практиці використовується порівняно рідко.
2. Методи калібрування. У методах калібрування не обов’язково знати величину граничного дифузійного струму (Ігр) в мка. Можна користуватися пропорційною їй величиною висоти полярографічної хвилі (h) в мм. Висоту визначають з графіка, побудованого на міліметровому папері або з діаграмної стрічки самописця. Для використання методу абсолютного калібрування або калібрувальних коефіцієнтів необхідно, щоби розчини з досліджуваною речовиною і стандартні розчини мали однаковий коефіцієнт дифузії (D). Ця умова виконується, якщо до однакових об'ємів фонового електроліта додають однакові об'єми (не більше 10% від об'єму фонового електроліта) досліджуваного і стандартних розчинів.
У цьому випадку всі постійні величини можна об’єднати в одну константу: h = kC .
Для
аналізу розчинів, концентрація
визначуваної речовини в яких лежить на
границі чутливості, використовують
метод добавок. В електролітичну комірку
вміщають певний об’єм суміші досліджуваного
розчину з фоновим електролітом (Vx)
і вимірюють граничний дифузійний струм
(hx).
Потім в цей же електролізер додають
точно виміряний об’єм концентрованого
стандартного розчину (Vст,
Сст)
і знов вимірюють граничний дифузійний
струм (hx+ст).
Концентрацію досліджуваного розчину
розраховують за формулою:
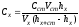 ,
,
або
з урахуванням зміни об'єму:
 .
.
Методом класичної полярографії можна визначати концентрації до 10-5 моль/л, а в деяких випадках до 10-7 моль/л з точністю 2-3%. Широко використовується для аналізу неорганічних і органічних речовин.
Недоліком методу є неможливість аналізу неелектроактивних речовин і необхідність роботи з шкідливою речовиною - ртуттю.
