
- •Інструментальні методи аналізу Особливості фізико-хімічних методів аналізу
- •2. Спектральні (оптичні) методи аналізу
- •Оптичні методи аналізу
- •2.1. Загальні принципи оптичної спектроскопії
- •2.2. Класифікація спектрів
- •2.3. Емісійний спектральний аналіз
- •2.4. Структура і характеристика елементів спектральних приладів
- •2.5. Якісний емісійний спектральний аналіз
- •2.5.1. Способи визначення довжин хвиль
- •2.6. Кількісний аналіз
- •2.7. Полум’яно-фотометричний аналіз
- •2.8. Молекулярно-абсорбційні методи аналізу
- •2.8.1. Якісний аналіз
- •2.8.1.1. Закон Бугера-Ламберта-Бера
- •2.8.1.2. Відхилення від закон Бугера-Ламберта-Бера
- •2.8.3. Схема приладів для вимірювання спектра поглинання
- •2.8.4. Кількісний фотоколориметричний аналіз
- •2.8.5. Турбідиметрія, нефелометрія
- •3. Хроматографічні методи аналізу
- •3.1. Загальна характеристика та класифікація хроматографічних методів аналізу
- •3.2. Принципова схема газового хроматографа
- •3.3. Хроматограма та її характеристики
- •3.4. Теоретичні основи хроматографічного розділення
- •3.4.1. Теорія рівноважної газової хроматографії
- •3.4.2. Теорія нерівноважної хроматографії
- •3.4.3. Теорія тарілок
- •3.5. Розділювальна здатність хроматографічної колонки
- •3.5.1. Основні фактори, що впливають на розділювальну здатність колонок
- •3.6. Якісний хроматографічний аналіз
- •3.7. Кількісний хроматографічний аналіз
- •4. Електрохімічні методи аналізу
- •4.1. Потенціометричні методи аналізу
- •4.1.1. Класифікація електродів. Аналітичний сигнал
- •Порівняльна характеристика електродів
- •Характеристики основних електродів порівняння
- •4.1.2. Способи проведення аналізу в потенціометрії
- •4.2. Кондуктометричні методи аналізу
- •4.2.1. Види електричної провідності
- •4.2.2 Пряма кондуктометрія
- •4.2.3. Кондуктометричне титрування
- •4.3. Кулонометричні методи аналізу
- •4.3.1. Пряма кулонометрія
- •4.3.2. Кулонометричне титрування
- •5. Полярографічні методи аналізу
- •5.1. Види поляризації
- •5.2. Принципова схема полярографічної установки
- •5.3. Полярографічна хвиля
- •5.4. Якісний полярографічний аналіз
- •5.5. Кількісний полярографічний аналіз
- •5.6. Причини спотворення форми полярограм
- •5.7. Амперометричне титрування
- •5.8. Інверсійна вольтамперометрія
- •5.8.1. Анодна інверсійна вольтамперометрія
- •Опис приладу для інверсійної вольтамперометрії марки акв-07мк
3.7. Кількісний хроматографічний аналіз
Кількісний хроматографічний аналіз базується на залежності між кількісними параметрами хроматографічних піків та концентрацією або кількістю речовини, яка введена в хроматограф.
За певних умов роботи детектора спостерігається лінійна залежність між кількісними параметрами хроматографічного піка Р та кількістю речовини в пробі, як, наприклад, між масою речовини в пробі та висотою піка згідно рівняння
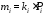 , (3.17)
, (3.17)
де ki - коефіцієнт пропорційності для і-того компоненту; mi - кількість і-того компоненту, введеного в хроматограф.
Під час введення в хроматограф кожен раз однакової маси проби кількість кожного компонента буде пропорційною концентрації Сі цього компонента в суміші. Тоді отримаємо коефіцієнт пропорційності kі, який називається калібрувальним коефіцієнтом:
 . (3.18)
. (3.18)
Метод кількісного аналізу, який використовує цю залежність називається методом абсолютного калібрування і застосовується для аналізу сумішей газоподібних речовин, тому що хроматографи обладнані дозувачами, які дозволяють вводити однакові об’єми газової проби.
Під час аналізу рідких проб користуються методом внутрішнього стандарту. Він полягає у тому, що до відомої маси проби mпр додають відому масу речовини-стандарту, якої немає в пробі mст, змішують їх і хроматографують одержану суміш. Масові частки компонентів проби розраховують за формулою:
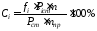 , (3.19)
, (3.19)
де Pi, Pст - кількісні параметри піків і-го компонента та речовини-стандарту, fi – нормувальний коефіцієнт, який дорівнює відношенню чутливостей хроматографа до компонента і речовини-стандарту.
Нормувальний коефіцієнт розраховують з хроматограми суміші, яка містить відомі концентрації компонентів (Сi) та речовини стандарту (Сст, % мас):
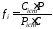 . (3.20)
. (3.20)
У випадку, коли необхідно визначати вміст всіх компонентів суміші розрахунки проводять за методом внутрішньої нормалізації. Цей метод можна застосовувати за умови, що всі компоненти суміші розділились і потрапили в детектор. Тоді суму їх концентрацій приймають за 100% і немає необхідності в додаванні речовини-стандарту.
Вміст і-того компоненту розраховують за формулою:
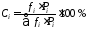 . (3.21)
. (3.21)
Нормувальні коефіцієнти розраховують за формулою (3.20), прийнявши одну з речовин за стандартну, тобто fст = 1.
4. Електрохімічні методи аналізу
Електрохімічні методи аналізу ґрунтуються на використанні залежності електричних параметрів електролітичної комірки від концентрації, природи та структури речовини, що бере участь в електродній (електрохімічній) реакції або в електрохімічному переносі зарядів між електродами. Електролітична комірка є електрохімічною системою, яка складається з електродів та електроліту, що контактують між собою.
За рекомендаціями ІЮПАК електрохімічні методи аналізу можна розділити на:
1. Методи, які ґрунтуються на перебігу електродних реакцій при відсутності електричного струму (потенціометрія) – вимірювання потенціалу Е.
2. Методи, які ґрунтуються на перебігу електродних реакцій при проходженні електричного струму крізь розчин електроліту (вольтамперометрія, кулонометрія) – вимірювання сили струму I; опору R чи електричної провідності W.
3. Методи, які не пов'язані з протіканням електродної реакції, а лише з електричними явищами в розчині (кондуктометрія і інші) – кількості електрики Q.
