
- •Предмет электрохимии.
- •Проводники первого и второго рода.
- •Электрохимические реакции.
- •Законы электролиза (законы фарадея).
- •Причины электролитической диссоциации.
- •Подвижность ионов.
- •Подвижность ионов гидроксония и гидроксила.
- •Числа переноса ионов.
- •Недостатки теории аррениуса.
- •Теория электролитов дебая и гюккеля.
- •Диссоциация воды. РН растворов.
- •Диссоциация слабых электролитов.
- •Гидролиз солей.
- •Буферные растворы.
- •Произведение растворимости.
- •Гальванические элементы. Эдс.
- •Термодинамика гальванического элемента.
- •Измерение эдс.
- •Строение границы электродраствор. Двойной электрический слой.
- •Электродный потенциал.
- •Классификация электродов.
- •Электроды первого рода.
- •Электроды второго рода.
- •Газовые электроды.
- •Амальгамные электроды.
- •Физические цепи.
- •Концентрационные цепи.
- •Химические цепи.
- •Аккумуляторы.
- •Кинетика электрохимических процессов.
- •Концентрационная поляризация.
- •Электрохимическое перенапряжение.
- •Напряжение разложения.
- •Закономерности перенапряжения выделения водорода.
- •1. Влияние плотности тока
- •2. Влияние природы металла
- •3. Влияние природы и состава раствора
- •4. Влияние температуры и некоторых других факторов
- •Теории водородного перенапряжения.
- •Теория замедленной рекомбинации
- •Теория замедленного разряда
- •Электроосаждение металлов.
- •Анодное растворение и пассивность металлов.
- •Коррозия металлов. Борьба с коррозией.
Амальгамные электроды.
Это полуэлементы, в которых амальгама какого-либо металла находится в контакте с раствором, содержащим ионы этого металла :
Мn+ Mm, Hg mMn+ + mne Mm (Hg)
Ртуть ведет себя как инертная среда, в которой растворен металл, а потенциалоопределяющими являются ионы этого металла :
![]() =
=
![]() + 2,303
+ 2,303![]() lg
lg
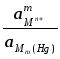
т.е. потенциал зависит от активности ионов металла не только в растворе, но и в амальгаме. Если металл находится в ртути в атомарном состоянии (m=1), то можно написать :
![]() =
=
![]() + 2,303
+ 2,303![]() lg
lg
![]()
Амальгамные электроды широко применяются в технике и в лабораторной практике. Кадмиевый амальгамный электрод Cd2+ Cd, Hg (Cd2+ + 2e Cd (Hg)) в виде амальгамы, содержащей 12,5% Cd, используется для изготовления нормальных элементов Вестона, ЭДС которых практически не изменяется со временем.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ, или РЕДОКСИ-ЭЛЕКТРОДЫ. Любая электродная реакция связана с изменением окислительно-восстановительного состояния участвующих в ней веществ, и в этом смысле все электроды представляют собой редокси-системы. Однако термин окислительно-восстановительные, или редокси-электроды, употребляется обычно в тех случаях, когда в реакции не участвуют непосредственно металлы или газы. Металл в редокси-электроде, обмениваясь электронами с участниками окислительно-восстановительной реакции, принимает потенциал, отвечающий установившемуся редокси-равновесию. К металлическому проводнику предъявляются здесь те же требования, что и в случае газовых электродов.
Следует различать простые и сложные редокси-электроды. В первом случае электродная реакция сводится к перемене валентности ионов без изменения их состава, например :
Fe3+ + e = Fe2+
Tl3+ + 2e = Tl+
MnO4- + e = MnO42-
Fe (CN)63- + e = Fe (CN)64-
Если обозначить окисленные ионы Ox, а восстановленные Red, то все написанные выше реакции можно выразить одним общим уравнением :
Ox + ne = Red
Простой редокси-электрод записывается в виде схемы :
Red, Ox Pt
а его потенциал дается уравнением
Red,Ox
= oRed,Ox
+ 2,303
![]() lg
lg
![]()
Как видно, потенциал простого редокси-электрода определяется отношением активностей ионов в двух различных степенях окисления. Если элемент образует ионы нескольких валентностей, то ему будет отвечать столько редокси-электродов, сколько можно получить попарных сочетаний (три валентности три различных редокси-электрода).
Потенциалы
простых редокси-электродов можно легко
связать с потенциалами соответствующих
электродов первого рода.
Пусть, например, металл М способен
существовать в растворе в виде ионов
высшей валентности Мh
и низшей валентности Mn.
Для него возможны два электрода первого
рода Mh
M
и Mn
M
и один редокси-электрод Mn,
Mh
M
, стандартные потенциалы которых
соответственно равны
![]() ,
,![]() и
и![]() .
Связь между этими величинами можно
найти, проведя мысленно процесс
электрохимического растворения металла
М с получением ионов высшей валентностиMh
либо непосредственно, либо через
промежуточное образование ионов низшей
валентности Mn.
Предполагается, что процесс растворения
протекает обратимо и изотермически в
бесконечно большом объеме раствора, в
котором активности ионов каждого сорта
равны 1. Этот процесс можно представить
в виде следующего простого цикла :
.
Связь между этими величинами можно
найти, проведя мысленно процесс
электрохимического растворения металла
М с получением ионов высшей валентностиMh
либо непосредственно, либо через
промежуточное образование ионов низшей
валентности Mn.
Предполагается, что процесс растворения
протекает обратимо и изотермически в
бесконечно большом объеме раствора, в
котором активности ионов каждого сорта
равны 1. Этот процесс можно представить
в виде следующего простого цикла :
hFoh
M Mh
nFon (hn)Fon,h
Mn
Из цикла следует : hoh = non + (h n)on,h
Это
уравнение известно как правило
Лютера ;
по нему можно рассчитать стандартный
потенциал любого из трех электродов,
если известны значения стандартных
потенциалов двух других электродов.
Уравнение применяется в тех случаях,
когда непосредственное определение
одного из потенциалов или затруднительно,
или невозможно. Так, например, потенциал
электрода первого рода Fe3+
| Fe
, измерить который непосредственно не
удается из-за неустойчивости в этих
условиях ионов Fe3+,
можно найти из доступных прямому
измерению стандартных потенциалов
электрода первого рода Fe2+
| Fe
и простого редокси-электрода Fe2+,
Fe3+|
Fe
:
![]() =
=![]() +
+![]()
В сложных редокси-электродах реакция протекает с изменением валентности реагирующих частиц и их состава. В реакциях такого рода участвуют обычно ионы водорода и молекулы воды; участие молекул воды не сказывается на характере уравнений для электродного потенциала, т.к. активность воды в ходе реакции (за исключением очень концентрированных растворов) остается постоянной. Схему сложного редокси-электрода можно записать следующим образом :
Red, Ox, H+ | Pt
Т.о., потенциал сложного редокси-электрода является функцией не только активностей окисленных и восстановленных частиц, но и активности водородных ионов. Например, для системы MnO4- Mn2+, в которой протекает электродная реакция
MnO4- + 8H+ + 5e = Mn2+ + 4H2O
потенциал электрода передается уравнением :
![]() =
=
![]() +
+
![]() ln
ln
 =
=
=
![]() + 2,303
+ 2,303
![]() lg
lg
 + 2,303
+ 2,303![]()
![]() lg
lg
![]()
Сложные редокси-электроды можно использовать как индикаторные электроды при измерении рН. Для этой цели часто применяют электрод, обратимый по отношению к системе хинон-гидрохинон. Для системы хинон-гидрохинон (х, гх) с реакцией
С6Н4О2 + 2Н+ + 2е = С6Н4(ОН)2
потенциалу электрода отвечает уравнение
х,
гх = ох,
гх + 2,303
![]() lg
lg
![]() = ох,
гх + 2,303
= ох,
гх + 2,303
![]() lg
lg
![]() +
+
+
2,303
![]() lg
lg
![]()
В раствор, рН которого хотят измерить, вводят эквимолярную смесь хинона и гидрохинона. Если считать, что отношение концентраций равно отношению активностей
![]() =
=
![]() = 1
= 1
то уравнение упрощается до
х,
гх = ох,
гх + 2,303
![]() lg
lg
![]() = ох,
гх
2,303
= ох,
гх
2,303
![]() рН
рН
и потенциал такого электрода, обычно называемого хингидронным , будет определяться непосредственно значением рН раствора. При 25оС ох, гх = 0,6992 В ; температурная зависимость ох, гх хорошо изучена. Хингидронный электрод легко приготовляется и удобен в работе. Хингидронным электродом нельзя пользоваться в щелочных растворах (гидрохинон слабая кислота, в щелочной среде он сильно диссоциирует и концентрация его в насыщенном растворе не является постоянной), а также в присутствии сильных окислителей или восстановителей.
Лекция 47
Классификация электрохимических цепей. Физические цепи. Концентрационные цепи. Химические цепи. Аккумуляторы.
Учитывая природу электродной реакции, можно классифицировать не только различные типы электродов, но и их комбинации. Различают три основных типа электрохимических систем, часто называемых электрохимическими цепями.
1. Система составлена из двух химически одинаковых электродов, на которых совершается одна и та же электродная реакция. ЭДС таких систем была бы равна нулю, если бы физические свойства электродов, а следовательно, и их стандартные потенциалы были одинаковыми. Электрохимические системы, в которых электроды отличаются только физическими свойствами, называются физическими цепями. Как правило, один из двух электродов физической цепи находится в более устойчивом, а другой в менее устойчивом при данных условиях состоянии. Источником электрической энергии в физических цепях служит свободная энергия перехода электрода из менее устойчивого в более устойчивое состояние.
Два электрода совпадают по своим физическим свойствам, качественному химическому составу и природе электродной реакции. Они отличаются лишь тем, что активность одного или нескольких участников реакции на электродах неодинакова. Электрохимические цепи, в которых электроды отличаются только активностью (концентрацией) участников электродной реакции, называются концентрационными цепями. Источником электрической энергии в концентрационных цепях служит энергия переноса вещества от большей активности к меньшей.
Два электрода могут отличаться и по химическим, и по физическим свойствам. Такие цепи называются химическими. В химических цепях источником электрической энергии служат протекающие в них химические реакции.
