
- •В.И.Павлова, н.В.Мамылина, ю.Г.Камскова Анатомо-физиологические и возрастные особенности сердечно-сосудистой системы человека. Челябинск
- •Введение
- •1. Морфологическая характеристика сердца
- •2. Возбудимость, проводимость и автоматия миокарда
- •3.Ионные механизмы генеза биопотенциалов кардиомиоцитов
- •4. Рефрактерность миокарда
- •5. Связь между возбуждением, сокращением и метаболизмом миокарда
- •6. Фазовая структура сердечного цикла
- •7. Компоненты нормальной электрокардиограммы
- •8. Миогенная регуляция деятельности сердца
- •9. Рефлекторные влияния на сердечную деятельность
- •10. Пороки развития сердца
- •11. Возрастные особенности сердца
- •А) Возрастные особенности сердечно-сосудистой системы у новорожденных и грудных детей
- •Б)Структурно-функциональные особенности сердечно-сосудистой системы у детей и подростков
- •12. Изменение механизмов регуляции деятельности сердца с возрастом
- •Вопросы для самоконтроля:
- •Литература
- •Оглавление
5. Связь между возбуждением, сокращением и метаболизмом миокарда
Важнейшим свойством миокарда, обеспечивающим насосную функцию сердца, является сократимость. Сократительный аппарат в кардиомиоцитах, как и в других типах мышечной ткани, представлен миофибриллами. Они расположены параллельно друг другу с высокой степенью упорядоченности и окружены мембранами саркоплазматического ретикулума, а также митохондриями. Структура миофибрилл и их расположение обусловливают поперечную исчерченность сократительных кардиомиоцитов.
Миофибриллы состоят из белковых нитей - миофиламентов, уложенных в регулярно повторяющиеся по всей их длине участки (саркомеры). Различают два типа миофиламентов: толстые, образованные белком миозином, и тонкие, образованные другим белком - актином.
Молекула миозина состоит из длинной хвостовой части, суженной шейки и утолщенной головки. Каждая толстая нить содержит более 100 молекул миозина, собранных в пучок, в средней части которого находятся хвостовые частицы молекул, а на обоих концах- выступающие над поверхностью нити головки.
Каждая тонкая нить состоит из двух линейных молекул актина, спирально скрученных друг с другом. В желобках между нитями актина уложены линейные молекулы белка тропомиозина (по две пары молекул на один шаг спирали актиновой нити). Вблизи соединений между двумя последовательными молекулами тропомиозина к актину прикрепляются глобулярные молекулы еще одного белка - тропонина.
Роль указанных белков в процессе мышечного сокращение объясняется «теорией скользящих нитей», которую разработали X. Хаксли и А. Хаксли в 50-х годах XX в. Согласно этой теории, при сокращении миозиновые нити скользят вдоль актиновых. При этом одни нити вдвигаются в промежутки между другими, что и приводит к укорочению саркомера. Движение нитей осуществляется благодаря «гребковым» движениям головок миозина: головка прикрепляется к участку связывания на актине, потом наклоняется, сдвигая нити друг относительно друга, и отсоединяется от актина. Далее головка прикрепляется к следующему участку связывания на актиновой нити, и цикл повторяется. Сила сокращения определяется количеством связей между миофиламентами.
Энергообеспечение этого процесса осуществляется за счет гидролиза АТФ головками миозина, причем АТФ-азная активность головок проявляется только после их связывания с актином. В расслабленной мышце соединению актина и миозина препятствуют молекулы тропонина, «закрывающие» участки связывания на актиновой нити. При возбуждении кардиомиоцита происходит быстрое поступление в саркоплазму ионов Са 2+, которые соединяются с тропонином. Присоединение Са2+ приводит к изменению конформации тропонин-тропомиозинового комплекса. При этом молекулы тропомиозина смещаются, актиновые и миозиновые нити вступают во взаимодействие, и начинается процесс сокращения. Чем больше ионов Са2+ поступит к миофибриллам при возбуждении, тем сильнее будет сокращение.
Таким образом, повышение концентрации ионов Са2+ в саркоплазме является ключевым фактором, обеспечивающим электромеханическое сопряжение - связь между возбуждением кардиомиоцита (электрический процесс) и его сокращением (механический процесс).
Электромеханическое сопряжение в кардиомиоците представляет собой последовательность событий, которая начинается с возникновения потенциала действия на плазматической мембране (рис.5). Когда мембранный потенциал достигает уровня -40 мВ, повышается проницаемость медленных потенциалзависимых Са2+-каналов, через которые в саркоплазму из внеклеточной среды поступает небольшое количество так называемых триггерных (запускающих) ионов Са2 + . Эти ионы увеличивают проницаемость Са2+ -каналов цистерн саркоплазматического ретикулума, и в саркоплазму поступают ионы Са2+, депонированные в цистернах. При этом количество «внутренних» ионов Са2+, высвобождающихся из цистерн, в десятки раз превышает количество «внешних» триггерных ионов. Резкое повышение концентрации ионов Са2+ в саркоплазме устраняет тропомиозиновую блокаду сокращения. Особая роль в описанном процессе принадлежит системе Т-трубочек, которые проводят деполяризацию наружной мембраны кардиомиоцита вглубь мышечного волокна. Таким образом обеспечивается вход триггерных ионов Са 2+ саркоплазму в непосредственной близости к цистернам саркоплазматического ретикулума и миофибриллам.
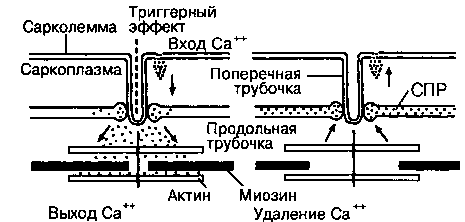
Рис.5 . Схема сопряжения возбуждения и сокращения в кардиомиоцитах (объяснение в тексте)
Так как входящий кальциевый ток достигает максимальной величины во время фазы 2 («плато») потенциала действия кардиомиоцита, длительность этой фазы в норме определяет силу сокращения.
По окончании фазы «плато» Са2+-каналы сарколеммы инактивируются, и поступление ионов Са2+ к миофибриллам прекращается. Одновременно усиливается выведение этих ионов во внешнюю среду и в саркоплазматический ретикулум Са2+-насосами. Уменьшение внутриклеточной концентрации ионов Na+ вследствие работы K+/Na+-насоса активизирует также удаление ионов Са2+ по механизму Ca2+/ Na+- обмена. В результате концентрация ионизированного Са2+ в саркоплазме резко уменьшается что приводит к восстановлению тропомиозиновой блокады и к расслаблению миокарда.
Кроме высвобождения ионов Са2+ из саркоплазматического ретикулума, существует и другой механизм поступления больших количеств ионов Са2+ в саркоплазму рабочего кардиомиоцита при его возбуждении. Этот механизм обеспечивается специфическими мембранными белками-переносчиками, которые осуществляют Ca2+/Na+ обмен - сопряженный транспорт ионов кальция и натрия через мембрану. В покое «ведущим» является входящий ток ионов Na+, энергия которого используется для выведения из клетки ионов Са2+. При возбуждении кардиомиоцита направление Ca2+/Na+ обмена меняется на противоположное по сравнению с покоем: «ведущим» становится входящий ток Са2+, а «ведомым» - выходящий ток Na+. В результате концентрация внутриклеточных ионов Са2+ возрастает.
Нарушение процесса электромеханического сопряжения приводит к тому, что электрический импульс, продолжая возникать и распространяться в миокарде, не вызывает сокращения сердечной мышцы. В этом случае электрическая активность сердца продолжает регистрироваться (например, на электрокардиограмме), тогда как его насосная функция снижается практически до нуля, что приводит к остановке кровообращения. Такое состояние называется электромеханической диссоциацией и может явиться одной из непосредственных причин внезапной смерти .
То, что для сокращения кардиомиоцитов необходимо поступление ионов Са2+ из внеклеточной среды, отличает сердечную мышцу от скелетной, в которой для инициации сокращения достаточно ионов Са2+ , поступающих из саркоплазматического ретикулума по потенциалзависимым каналам. Поэтому сократимость сердечной мышцы в значительной степени зависит от концентрации внеклеточного кальция, а также от действия биологически активных веществ, например, катехоламинов, влияющих на поступление ионов Са2+ в кардиомиоциты.
Снижение сократимости миокарда является одной из основных причин развития сердечной недостаточности – состояния, при котором нарушается гемодинамическая функция сердца и нормальное кровоснабжение органов и тканей. В клинической практике для лечения сердечной недостаточности применяют сердечные гликозиды - вещества, выделенные из таких растений, как наперстянка (дигиталис), строфант, ландыш и др. Эти препараты блокируют K+/Na+-нacoc мембраны, что приводит к возрастанию внутриклеточной концентрации Na+ и усилению поступления ионов Са2+ в кардиомиоцит по механизму Ca2+/Na+ обмена (как в покое, так и при возбуждении). В результате увеличивается продолжительность фазы «плато», а, следовательно, и сократимость миокарда.
Обеспечение таких свойств миокарда, как автоматия, возбудимость, проводимость и сократимость требует постоянных затрат энергии. Энергия расходуется в процессе работы ионных насосов, а также при сокращении миокарда. Непосредственным энергетическим субстратом в указанных процессах являются молекулы АТФ. Большую роль играет также другое макроэргическое соединение - креатинфосфат, который является быстромобилизуемым резервом для ресинтеза АТФ из АДФ и фосфорной кислоты. В свою очередь, энергия для образования макроэргических связей АТФ и креатинфосфата выделяется в процессах биологического окисления. Миокард характеризуется очень высокой степенью потребления кислорода. В покое эта величина достигает 10 мл/мин на 100 г ткани, что составляет около 15% от общего количества потребляемого организмом кислорода. Высокая степень зависимости метаболизма миокарда от доставки кислорода отличает сердечную мышцу от скелетных, в которых значительная часть энергии во время сократительной активности поступает за счет анаэробного окисления. В качестве источника энергии миокард может использовать различные вещества, причем доля каждого субстрата в энергообеспечении работы сердца определяется функциональным состоянием организма. В условиях основного обмена около 70% потребляемого миокардом кислорода расходуется на окисление свободных жирных кислот и их транспортной формы – кетоновых тел. После приема пищи, который приводит к повышению концентрации глюкозы в крови, потребление глюкозы миокардом резко возрастает, и доля кислорода, приходящаяся на окисление этого субстрата, может достигать 90%. При интенсивной физической нагрузке в крови значительно возрастает концентрация молочной кислоты, которая образуется в процессе анаэробного гликолиза в скелетных мышцах. В этих условиях молочная кислота становится одним из основных источников получения энергии в миокарде.
