
- •В.И.Павлова, н.В.Мамылина, ю.Г.Камскова Анатомо-физиологические и возрастные особенности сердечно-сосудистой системы человека. Челябинск
- •Введение
- •1. Морфологическая характеристика сердца
- •2. Возбудимость, проводимость и автоматия миокарда
- •3.Ионные механизмы генеза биопотенциалов кардиомиоцитов
- •4. Рефрактерность миокарда
- •5. Связь между возбуждением, сокращением и метаболизмом миокарда
- •6. Фазовая структура сердечного цикла
- •7. Компоненты нормальной электрокардиограммы
- •8. Миогенная регуляция деятельности сердца
- •9. Рефлекторные влияния на сердечную деятельность
- •10. Пороки развития сердца
- •11. Возрастные особенности сердца
- •А) Возрастные особенности сердечно-сосудистой системы у новорожденных и грудных детей
- •Б)Структурно-функциональные особенности сердечно-сосудистой системы у детей и подростков
- •12. Изменение механизмов регуляции деятельности сердца с возрастом
- •Вопросы для самоконтроля:
- •Литература
- •Оглавление
3.Ионные механизмы генеза биопотенциалов кардиомиоцитов
Возбудимость, проводимость и автоматия миокарда обеспечиваются электрохимическими процессами, происходящими на плазматической мембране кардиомиоцитов (сарколемме). Важнейшим параметром, характеризующим эти процессы, является электрический заряд внутренней поверхности мембраны - мембранный потенциал. Мембранный потенциал кардиомиоцитов периодически изменяется (рис.2 ). В период времени между двумя электрическими импульсами возбуждения мембранный потенциал (так называемый максимальный диастолический потенциал) достигает в разных клетках миокарда от -50 до -95 мВ. В сократительных кардиомиоцитах весь этот период мембранный потенциал стабилен и называется поэтому потенциалом покоя.
Мембранные потенциалы клеток водителей ритма во время диастолы не стабильны. Поэтому для этих клеток термин «потенциал покоя» не применяется. В момент возбуждения (генерации электрического импульса) регистрируется резкое колебание мембранного потенциала в сторону положительных величин (деполяризация), с последующим возвращением к уровню максимального диастолического потенциала. Этот электрический импульс называется потенциалом действия.
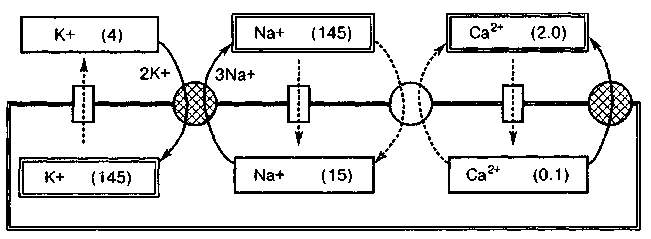
Рис.2 . Ионные градиенты и транспорт ионов через плазматическую мембрану кардиомиоцита
в скобках - концентрации ионов, ммоль/л; сплошные стрелки - активный транспорт; пунктирные стрелки - пассивный транспорт; прямоугольники - ионные каналы; заштрихованные кружки - ионные насосы; светлый кружок – Na+/Ca2+- переносчик.
Величина мембранного потенциала в любой момент времени определяется трансмембранными токами ионов (в основном -
калия, натрия и кальция). Скорость движения ионов через сарколемму зависит от функционирования мембранных белков-переносчиков: ионных каналов и насосов (рис.2 ).
Через ионные каналы осуществляется облегченная диффузия ионов - пассивный транспорт, не требующий затрат энергии. Направление и скорость диффузии определяются величиной электрохимического градиента для данного иона (т. е. разностью его внутри- и внеклеточной концентраций и зарядом мембраны). Большинство каналов ионоселективны, т. е. преимущественно проницаемы для какого-либо одного вида ионов,
Движение ионов против электрохимического градиента (активный транспорт) осуществляется ионными насосами, которые сопряжены с мембранными ферментами (АТФ-азами). Последние ускоряют гидролиз АТФ, а выделяющаяся при этом энергия расходуется на перенос ионов. Среди таких переносчиков наибольшую роль в кардиомиоцитах играют: K+/Na+ -насос (переносит ионы Na+ наружу клетки, а ионы К+ - внутрь) и Са2+-насос (выводит ионы Са2+ из кардиомиоцита). Основным результатом деятельности ионных насосов является создание и поддержание градиентов концентрации ионов по сторонам плазматической мембраны: снаружи значительно повышена концентрация ионов Na+ и Са2 +, а внутри - ионов К+.
В межимпульсный период проницаемость мембраны кардиомиоцитов для ионов К+ значительно больше, чем для других ионов. Поэтому возникновение отрицательного диастолического потенциала определяется, в основном, пассивно выходящим из клетки током ионов калия. Другим током, участвующим в формировании диастолического потенциала кардиомиоцитов, является активный ток, непосредственно создаваемый K +/Na+ -насосом. При работе этого насоса происходит неэквивалентный (электрогенный) обмен ионов: на каждые 2 иона К+, введенных в клетку, выводится 3 иона Na+. В результате возникает выходящий из клетки ток положительных зарядов - насосный ток, который увеличивает отрицательный внутриклеточный заряд. Доля насосного тока в формировании мембранного потенциала тем больше, чем больше электрическое сопротивление сарколеммы, и может составлять 25% и более (особенно в клетках Пуркинье). Активность K+ /Na+- АТФ-азы и величина насосного тока регулируются концентрациями переносимых ионов, усиливаясь при увеличении внеклеточной концентрации ионов К+ и внутриклеточной концентрации ионов Na+.
В клетках водителей ритма сердца диастолический потенциал нестабилен и самопроизвольно отклоняется от максимального отрицательного уровня в сторону деполяризации. Этот феномен, называемый спонтанной (медленной) диастолической деполяризацией, свойственен всем проводящим кардиомиоцитам и является основой их автоматии. Когда в результате спонтанной деполяризации мембранный потенциал достигает критического уровня (порогового потенциала), пейсмекер генерирует потенциал действия. При развитии потенциала действия в одном кардиомиоците деполяризация распространяется на соседние невозбужденные клетки. В результате мембранный потенциал этих клеток достигает порогового уровня, и в них также возникает потенциал действия. Таким образом, распространение возбуждения по миокарду происходит согласно «принципу домино»: предыдущая клетка возбуждает последующую.
В норме с наибольшей скоростью спонтанная диастолическая деполяризация протекает в пейсмекерах синоатриального узла. Поэтому в этих клетках пороговый потенциал достигается наиболее быстро, что и обусловливает самую большую частоту генерации потенциалов действия (60-80 в 1 мин). В изолированных кардиомиоцитах атриовентрикулярного соединения и проводящей системы желудочков (латентные пейсмекеры) спонтанная диастолическая деполяризация протекает с меньшей скоростью, а в сократительных кардиомиоцитах отсутствует. Таким образом, в норме перечисленные клетки возбуждаются не спонтанно, а лишь под влиянием импульсов, поступающих от синоатриального узла. Пусковыми стимулами для возбуждения кардиомиоцитов могут явиться и внешние электрические импульсы, получаемые от искусственных водителей ритма (кардиостимуляторов), а также механическое раздражение, например, сильный удар в область грудины при остановке сердца.
Основная роль в формировании потенциала действия кардиомиоцита принадлежит входящему в клетку току ионов Na + и (или) Са2+ . Сила этого тока регулируется потенциалзависимыми ионными каналами, которые при диастолическом уровне мембранного потенциала закрыты, а при деполяризации открываются (активируются). Когда деполяризация достигает величины порогового потенциала, количество активированных каналов становится достаточным для замыкания положительной обратной связи: «деполяризация - активация ионных каналов - усиление входящего тока - деполяризация». В результате возникает самоподдерживаемый, лавинообразный вход катионов в клетку, составляющий суть формирования потенциала действия. Описанный процесс приводит к сильной деполяризации мембраны, при которой каналы входящего тока инактивируются, т. е. закрываются и временно теряют способность к активации. Сила входящего тока при этом падает, а мембранный потенциал вследствие выхода из клетки ионов К+ возвращается к диастолическому уровню. В межимпульсный период каналы входящего тока вновь обретают способность к активации, а исходное распределение ионов по обе стороны сарколеммы восстанавливается за счет работы ионных насосов.
В 1975 г. американский электрофизиолог П. Крейнфилд предложил классифицировать кардиомиоциты по скорости развития фазы деполяризации потенциала действия на клетки с « медленным ответом» и клетки с «быстрым ответом». В сарколемме клеток первого типа представлены, в основном, «медленные» каналы входящего тока, которые характеризуются низкими скоростями активации и инактивации. Эти каналы проницаемы для ионов Са2+ и Na+ (в соотношении примерно 1000 : 1) и обозначаются как Ca 2+,Na +- или просто Са 2+-каналы. В поверхностной мембране кардиомиоцитов с «быстрым ответом», кроме указанного вида каналов, находятся также «быстрые» натриевые каналы ,проницаемые исключительно для ионов Na+ и обладающие высокими скоростями активации и инактивации. Именно свойства ионных каналов входящего тока и определяют особенности формирования потенциала действия и электрофизиологические параметры «медленных» и «быстрых» кардиомиоцитов, сравнительная характеристика которых представлена в табл.1 .
Таблица 1
Основные типы кардиомиоцитов и их свойства
|
Морфофункциональная характеристика |
Проводящие |
Сократительные
| ||
|
Р-клетки |
Клетки Пуркинье | |||
|
Основная локализация |
СА-узел |
АВ-соединение |
Система Гиса-Пуркинье |
Остальной миокард |
|
Электрофизиологическая характеристика |
С медленным ответом |
С быстрым ответом | ||
|
Максимальный диастолический потенциал |
-60-…-50 |
-70…--60 |
-95…-90 |
-90…-80 |
|
Параметры потенциала действия: |
| |||
|
Амплитуда (мВ) |
60-70 |
70-80 |
100-120 |
100-120 |
|
Овершут (мВ) |
0-10 |
5-15 |
20-30 |
20-30 |
|
Длительность (мс) |
100-300 |
100-300 |
300-500 |
200-300* |
|
Скорость нарастания фазы 0 (В/с) |
1-10 |
5-20 |
500-1000 |
100-300 |
|
Скорость проведения (м/с) |
До 0,05 |
0,1 |
1-4 |
0,1-0,5** |
|
Собственная частота импульсации (имп/мин) |
60-80 |
40-60 |
20-40 |
…*** |
* Длительность потенциала действия в предсердиях – 100-300 мс
** Скорость проведения в AN-зоне атриовентрикулярного соединения около 0,05 м/с, в пучке Гиса - меньше, чем в волокнах Пуркинье, в сократительных миоцитах предсердий - меньше, чем в желудочках.
*** Сократительные кардиомиоциты не обладают автоматией.
Клетки с «быстрым ответом». К этому типу относятся все сократительные кардиомиоциты, а также проводящие кардиомиоциты предсердий и некоторые элементы проводящей системы желудочков (волокна Пуркинье). Кроме высокой скорости деполяризации, указанные клетки характеризуются большой амплитудой потенциала действия, а также высокой скоростью и надежностью проведения возбуждения. Максимальный диастолический потенциал в этих кардиомиоцитах составляет около -90 мВ, а процесс формирования потенциала действия складывается из следующих пяти фаз (рис.3,б ):
Фаза 0 - быстрая деполяризация - протекает со скоростью, достигающей 1000 В/с (в клетках Пуркинье), и обеспечивается, в основном, входящим током ионов Na+. Необходимое количество «быстрых» Na+ -каналов активируется при деполяризации мембраны до пороговой величины, составляющей около -60 мВ. Когда мембранный потенциал достигает примерно -40 мВ, начинают активироваться «медленные» Са2+-каналы, и к натриевому току добавляется входящий кальциевый ток, вклад которого становится значимым только в формировании положительных значений мембранного потенциала - «овершута». На протяжении всей фазы 0
регистрируется также выходящий ток ионов К+, однако сила этого тока мала, по сравнению с натриевым током, так как проницаемость мембраны для ионов К+ в эту фазу значительно меньше, чем для Na+, а клетка большую часть времени заряжена внутри отрицательно.
Фаза 1 - начальная быстрая реполяризация. Когда величина мембранного потенциала достигает примерно + 20 мВ, натриевые каналы быстро инактивируются, и вход ионов Na+ в клетку прекращается. Входящий ток Са2+ при этом сохраняется, так как «медленные» Са 2+-каналы инактивируются позже. В то же время реверсия мембранного потенциала вызывает заметное усиление выходящего тока К+ (в частности, из-за активации потенциалзависимых калиевых каналов). Интенсивный выход ионов К+ на фоне относительно небольшого входящего тока Са2+ приводит к уменьшению положительного заряда внутри клетки. В клетках волокон Пуркинье в эту фазу происходит также кратковременная активация потенциалзависимых хлорных каналов, через которые анионы Сl- поступают в клетку, что ускоряет реполяризацию.
Фаза 2 - медленная реполяризация (фаза «плато»). Характеризуется примерным равновесием между выходящим током ионов К+ и входящим током ионов Са2+ , что обеспечивает относительную стабилизацию мембранного потенциала. Фаза «плато» является наиболее значимой для сократительных кардиомиоцитов, так как входящие в это время в цитоплазму ионы Са2+ инициируют процесс сокращения. Кроме того, от длительности фазы «плато» зависит продолжительность периода рефрактерности.
Фаза 3 - конечная быстрая реполяризация. Примерно через 200 мс после начала потенциала действия Са 2+-каналы практически полностью инактивируются, а вход ионов Са2+ в кардиомиоцит прекращается. Продолжающийся выход ионов К+ обеспечивает возвращение мембранного потенциала к максимальному диастолическому уровню.
Фаза 4 - покой (в сократительных кардиомиоцитах) или спонтанная диастолическая деполяризация (в клетках Пуркинье).
Таблица 2
Сравнительная характеристика кардиомиоцитов с «быстрым» и «медленным ответом»
|
Параметр |
Клетки с быстрым ответом |
Клетки с медленным ответом |
|
Расположение в сердце |
Сократительные кардиомиоциты и проводящие волокна предсердий и желудочков |
СА-узел, АВ-соединение; коронарный синус и клапаны |
|
Параметр |
Клетки с быстрым ответом |
Клетки с медленным ответом |
|
СДД и автоматия (фаза 4) |
Есть только у клеток Пуркинье |
Есть |
|
«Быстрые» Na+-каналы |
Есть |
Нет |
|
«Медленные» Са2+-каналы |
Есть |
Есть |
|
Пороговый потенциал (мВ) |
-70.. .-60 |
-50.. .-40 |
|
Основной ионный ток фазы 0, его блокатор, скорость активации и инактивации |
Na+ Лидокаин Высокая |
Са2+ Верапамил Низкая |
|
Сравнительные значения МДП и параметров ПД (скорость нарастания Фазы 0, амплитуда, скорость и надежность проведения) |
Высокие |
Низкие |
|
Продолжительность рефрактерного периода |
Примерно равна длительности ПД |
Превышает длительность ПД на 100 мс и более |
Клетки с «медленным ответом» представлены, в основном, проводящими кардиомиоцитами синоатриального узла и атриовентрикулярного соединения. Для этого типа кардиомиоцитов, по сравнению с «быстрыми» клетками (табл.2 ), характерны меньшая величина максимального диастолического потенциала (МДП) (около -60 мВ), а также меньшая амплитуда потенциала действия (ПД) и скорость его распространения. Фазы де- и реполяризации потенциала действия «медленных» клеток протекают более плавно, чем в «быстрых» (рис.3,а ).
Фаза 0 - быстрая деполяризация - характеризуется небольшой по сравнению с «быстрыми» клетками скоростью (до 20 В/с) и обеспечивается входящим током ионов Са2+ . Пороговый потенциал, при котором активируется достаточное для обеспечения этого тока количество «медленных» Са 2+-каналов, примерно равен -40 мВ.
Фазы 2 и 3 - реполяризация. По сравнению с «быстрыми» клетками фаза I (начальная быстрая реполяризация) отсутствует, вершина потенциала действия и фаза реполяризации сглажены, «плато» не выражено и четкой границы между фазами 2 и 3 нет. Величина мембранного потенциала в фазу реполяризации определяется соотношением между выходящим током ионов К+ и входящим током ионов Са2+ на фоне медленной инактивации Са2+-каналов. Завершается реполяризация достижением уровня максимального диастолического потенциала.
Фаза 4 - спонтанная диастолическая деполяризация. В истинных пейсмекерах в результате этого процесса мембранный потенциал достигает порогового уровня, фаза 4 плавно переходит в фазу 0 очередного потенциала действия, и цикл повторяется. В латентных пейсмекерах спонтанная диастолическая деполяризация прерывается импульсом, приходящим от синоатриального узла, что обусловливает скачкообразный переход фазы 4 в фазу 0 следующего цикла. Спонтанная диастолическая деполяризация и, следовательно, автоматия характерны для всех клеток с «медленным ответом», в то время как среди «быстрых» клеток этим свойством в норме обладают лишь клетки Пуркинье. Вместе с тем, в условиях повреждения сократительные кардиомиоциты также могут самовозбуждаться и генерировать электрические импульсы, что является одной из причин возникновения экстрасистолии и других нарушений ритма сердца.

Рис.3 . Потенциалы действия кардиомиоцитов
По оси ординат - мембранный потенциал (мВ); по оси абсцисс - время (мс), П -пороговый потенциал (критический уровень деполяризации).
А-клетки-пейсмекеры синоатриального узла («медленные» клетки): 0 - быстрая деполяризация; 2-3 - реполяризация; 4 - медленная (спонтанная) диа-столическая деполяризация. МДП - максимальный диастолический потенциал.
б - сократительные кардиомиоциты желудочков («быстрые» клетки); 0- быстрая деполяризация; 1 - начальная быстрая реполяризация; 2 - медленная реполяризация; 3 - конечная быстрая реполяризация; 4 - покой. ПП - потенциал покоя; ПД - амплитуда потенциала действия; Р - реверсия мембранного потенциала. ∆t- время проведения возбуждения от синоатриального узла к желудочкам.
Ионные механизмы спонтанной диастолической деполяризации окончательно не установлены. В разных клетках-пейсмекерах она может быть вызвана повышением проницаемости для ионов Na+ (или Са2+ ) и усилением входящего в клетку тока этих ионов или (и) снижением проницаемости для ионов К+ и уменьшением соответствующего выходящего тока.
