
- •Глава 1. Галоидпроизводные углеводородов
- •Номенклатура алкилгалогенидов, алкенилгалогенидов, алкинилгалогенидов и арилгалогенидов
- •1. Получение алкилгалогенидов
- •1.1. Галогенирование алканов
- •1.2. Присоединение галогеноводородов к алкенам
- •1.3. Замещение гидроксильной группы на галоген.
- •1.4. Свойства Галоидпроизводных углеводородов
- •1.4.1. Реакции нуклеофильного замещения
- •1.4.2. Механизм sn1
- •Дифенилметилгалогенид Трифенилметилгалогенид
- •1.4.3. Механизм sn2
- •1.4.4. Реакции отщепления
- •1.4.5. Реакции алкилгалогенидов с металлами
- •Глава 2. Спирты
- •Номенклатура одноатомных спиртов
- •2.4. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
- •2.5. Гидролиз алкилгалогенидов
- •2.6. Свойства одноатомных спиртов
- •Температуры кипения некоторых спиртов и изомерных им простых эфиров
- •Кислотно-основные свойства спиртов
- •Кислотность спиртов
- •Из этих данных следует, что равновесие в системе спирт – щелочь всегда смещено в сторону спирта, а не алкоголята:
- •Замещение гидроксильной группы на галоген. Получение алкилгалогенидов
- •Получение алкилгалогенидов из спирта и галогеноводородных кислот
- •Получение алкилгалогенидов из спиртов и галогенидов фосфора
- •Дегидратация спиртов
- •2.10. Образование простых эфиров из спиртов
- •2.11. Получение простых эфиров по Вильямсону
- •2.12. Окисление спиртов
- •Восстановление спиртов
- •Взаимодействие с щелочными и щелчноземельными металлами.
- •2.15. Двухатомные спирты
- •2.16. Получение диолов
- •2.17. Свойства диолов
- •2.21. Расщепление простых эфиров кислотами
- •Глава 3. Тиолы и сульфиды
- •3.1 Получение тиолов
- •3.2 Свойства тиолов
- •Решения некоторых тестовых задач по теме спирты и тиолы
- •Только в реакциях 3) и 4) используются третичные спирты. Поскольку стабильность третичного карбениевого иона бензильного типа выше, чем стабильность третичного карбениевого иона алкильного типа:
- •5. Какого алкена образуется меньше при дегидратации 3-метилгексанола-3?
- •Глава 4. Альдегиды и кетоны
- •Альдегиды классификация
- •Строение карбонильной группы
- •4.1. Реакционные центры в молекулах альдегидов и кетонов
- •4.2. Химические свойства альдегидов и кетонов
- •4.3. Реакции альдегидов и кетонов по механизму нуклеофильного присоединения (an)
- •4.4. Реакции нуклеофильного присоединения по карбонильной группе с последующим отщеплением воды.
- •4.5. Окисление альдегидов и кетонов.
- •4.6. Реакция Канниццаро -Тищенко
- •4.7. Реакции полимеризации.
- •Получение альдегидов и кетонов
- •4.9. Медико-биологическое значение соединений с карбонильной группой
- •Отдельные представители альдегидов и кетонов
- •Эталонное решение задач
1.4.5. Реакции алкилгалогенидов с металлами
Алкилгалогениды реагируют с активными металлами, такими как литий и магний в растворе диэтилового эфира, который служит инертной средой, в которой образующиеся металлоорганические соединения обычно достаточно хорошо растворимы.
![]()
![]()
Необходимо исключить присутствие влаги, кислорода и двуокиси углерода, с которыми данные металлоорганические соединения легко реагируют. Обычно их получение и дальнейшие реакции проводят в инертной атмосфе-ре, в качестве которой используется азот или аргон. Соединения магния RMgHal получили особое название реактивы Гриньяра (в честь французско-го химика Виктора Гриньяра, открывшего эти соединения).
Вследствие большого различия в электроотрицательности магния и углерода связь C-Mg полярна, причём отрицательным концом диполя является углерод, а положительным – магний, и реактив Гриньяра как бы содержит в связанном виде карбанион R¯, который является сильным Брен-стедовским основанием.
![]()
Литийорганические и магнийорганические соединения легко реагируют с разнообразными классами органических соединений, такими как сами алкилгалогениды, соединениями, содержащими двойные С=О и C=N связи, тройную C≡N связь, а также с такими неорганическими соединениями как CO2, кислород, сера, галогены и др. Обычно эти реакции рассматриваются при обсуждении свойств конкретных органических соединений.
Протонные растворители (соединения, содержащие связи O-H, N-H) к которым могут быть отнесены вода, спирты, органические кислоты, первич-ные и вторичные амины, реагируют с реактивами Гриньяра согласно следую-щей общей схеме
![]()
Исторически первой исследованной реакцией алкилгалогенидов с активными металлами была реакция Вюрца, в которой алкилгалогенид реагирует с металлическим натрием согласно следующему уравнению.
2RHal + 2Na → R-R + 2NaHal
Считается, что первой стадией этой реакции является образование натрий-органического соединения, которое при действии на него алкилгалогенида
образует углеводород.
1) RHal + 2Na → RNa + NaHal 2) RNa + RHal → R-R + NaHal
Как правило реакция неприменима для получения углеводородов из двух разных алкилгалогенидов, т.к. в этом случае образуется смесь трёх разных углеводородов
3RHal + 3R1Hal + 6Na → 6NaHal + R-R + R-R1 + R1- R1
Обычно в реакции Вюрца используются бромиды или иодиды, но не хлориды и фториды. В настоящее время реакция имеет ограниченное применение для синтеза алканов.
Глава 2. Спирты
Спиртами называют производные углеводородов, которые содержат одну или несколько гидроксильных групп вместо атомов водорода . По числу гидроксильных групп спирты подразделяются на одноатомные, двухатом-ные, трехатомные и т.д.
СН3СН2-ОН ; HO-CH2CH2-OH ; HO-CH2CH(OH)CH2-OH
Этанол Этандиол-1,2 Глицерин
(этиленгликоль) (пропантриол-1,2,3)
одноатомный двухатомный трёхатомный
Простейшие ненасыщенные спирты, в которых гидроксил связан с двойной или тройной связью, этенол и этинол неустойчивы.

Ацетальдегид на 11.2 ккал более устойчив по сравнению с этенолом, а кетен на 39.1 ккал более устойчив чем этинол, соответствующие константы равновесия составляют 2×108 и 7.5×1024 . Простейший спирт ароматического ряда - C6H5OH, обычно относят к классу фенолов; по сравнению с циклогексадиеноном-2,4 фенол более устойчив на 19.7 ккал,

и в отличие алифатического ряда данное равновесие смещено в сторону фенола, а константа равновесия составляет 5×10-14 . Подобное отличие от алифатического ряда связано со стабилизацией фенола за счет его ароматичности. В том случае, когда гидроксильная группа отделена от двойной или тройной связи по крайней мере двумя одинарными связями, как в аллиловом или пропаргиловом спиртах (в скобках приведены названия согласно номенклатуре IUPAC),
CH2=CH–CH2–OH CH≡C–CH2–OH
аллиловый спирт (пропен-2-ол) пропаргиловый спирт (пропин-2-ол)
такие ненасыщенные спирты вполне устойчивы и проявляют свойства, характерные как для спиртов, так и для ненасыщенных соединений. Согласно
другой классификация спиртов, основанной на положении гидроксильной группы в углеводородной цепи, они могут быть первичными, в том случае, когда гидроксил находится в начале цепи и, таким образом, спирт содержит -СH2OH группу, вторичными, когда гидроксил находится в середине цепи и спирт содержит -CH(OH)- группу или третичными, когда гидроксил находится в месте разветвления цепи и спирт содержит группу
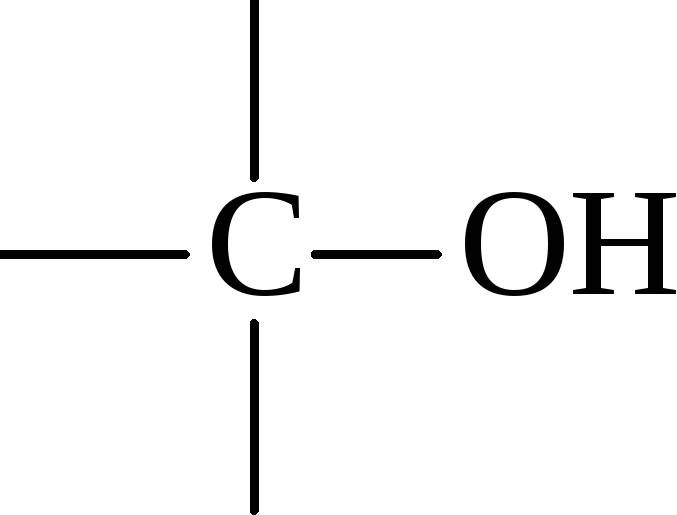
Эта классификация полезна, так как она в большинстве случаев тесно связана с различием в свойствах первичных, вторичных и третичных спиртов. Отдельные примеры первичных, вторичных и третичных спиртов приведены ниже.
-

первичный
бутиловый спирт
(бутанол-1)
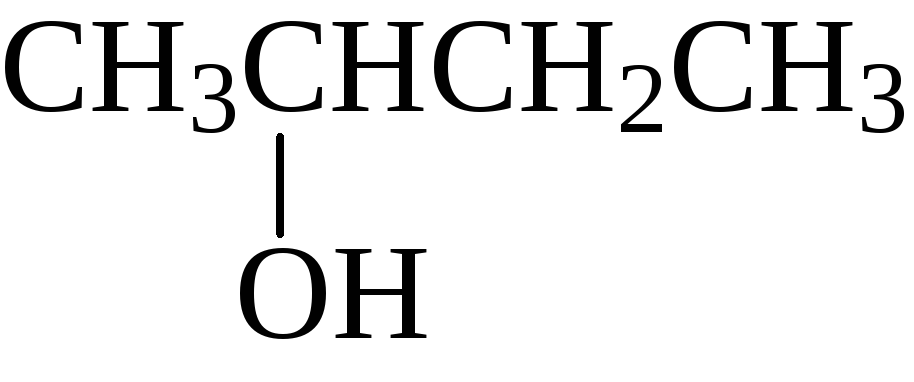
вторичный бутиловый спирт
(бутанол-2)

третичный
бутиловый спирт
(2-метилпропанол-2)
В скобках приведены названия спиртов в соответствии с номенклатурой IUPAC.
