- •Глава 1. Галоидпроизводные углеводородов
- •Номенклатура алкилгалогенидов, алкенилгалогенидов, алкинилгалогенидов и арилгалогенидов
- •1. Получение алкилгалогенидов
- •1.1. Галогенирование алканов
- •1.2. Присоединение галогеноводородов к алкенам
- •1.3. Замещение гидроксильной группы на галоген.
- •1.4. Свойства Галоидпроизводных углеводородов
- •1.4.1. Реакции нуклеофильного замещения
- •1.4.2. Механизм sn1
- •Дифенилметилгалогенид Трифенилметилгалогенид
- •1.4.3. Механизм sn2
- •1.4.4. Реакции отщепления
- •1.4.5. Реакции алкилгалогенидов с металлами
- •Глава 2. Спирты
- •Номенклатура одноатомных спиртов
- •2.4. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
- •2.5. Гидролиз алкилгалогенидов
- •2.6. Свойства одноатомных спиртов
- •Температуры кипения некоторых спиртов и изомерных им простых эфиров
- •Кислотно-основные свойства спиртов
- •Кислотность спиртов
- •Из этих данных следует, что равновесие в системе спирт – щелочь всегда смещено в сторону спирта, а не алкоголята:
- •Замещение гидроксильной группы на галоген. Получение алкилгалогенидов
- •Получение алкилгалогенидов из спирта и галогеноводородных кислот
- •Получение алкилгалогенидов из спиртов и галогенидов фосфора
- •Дегидратация спиртов
- •2.10. Образование простых эфиров из спиртов
- •2.11. Получение простых эфиров по Вильямсону
- •2.12. Окисление спиртов
- •Восстановление спиртов
- •Взаимодействие с щелочными и щелчноземельными металлами.
- •2.15. Двухатомные спирты
- •2.16. Получение диолов
- •2.17. Свойства диолов
- •2.21. Расщепление простых эфиров кислотами
- •Глава 3. Тиолы и сульфиды
- •3.1 Получение тиолов
- •3.2 Свойства тиолов
- •Решения некоторых тестовых задач по теме спирты и тиолы
- •Только в реакциях 3) и 4) используются третичные спирты. Поскольку стабильность третичного карбениевого иона бензильного типа выше, чем стабильность третичного карбениевого иона алкильного типа:
- •5. Какого алкена образуется меньше при дегидратации 3-метилгексанола-3?
- •Глава 4. Альдегиды и кетоны
- •Альдегиды классификация
- •Строение карбонильной группы
- •4.1. Реакционные центры в молекулах альдегидов и кетонов
- •4.2. Химические свойства альдегидов и кетонов
- •4.3. Реакции альдегидов и кетонов по механизму нуклеофильного присоединения (an)
- •4.4. Реакции нуклеофильного присоединения по карбонильной группе с последующим отщеплением воды.
- •4.5. Окисление альдегидов и кетонов.
- •4.6. Реакция Канниццаро -Тищенко
- •4.7. Реакции полимеризации.
- •Получение альдегидов и кетонов
- •4.9. Медико-биологическое значение соединений с карбонильной группой
- •Отдельные представители альдегидов и кетонов
- •Эталонное решение задач
4.5. Окисление альдегидов и кетонов.
Альдегиды окисляются легче, чем другие классы органических соединений. Особенно легко окисляются ароматические альдегиды (например, бензальдегид). Реакции окисления альдегидов принято записывать в виде схемы:

Окислителями альдегидов могут быть:
кислород воздуха;
реактив Толленса [Ag(NH3)2]OH;
реактив Фелинга – щелочной раствор комплексной соли, которая
образуется при взаимодействии гидроксида меди (П) и калий-натри-
евой соли винной кислоты;
раствор перманганата калия (KMnO4);
раствор дихромата калия (K2Cr2O7) и др.
Реакции альдегидов с реактивами Толленса и Фелинга являются качественными реакциями на альдегидную группу.
Кетоны окисляются очень трудно и только в жестких условиях (например, раствор K2Cr2O7 в H2SO4(конц) при нагревании). В результате происходит разрушение углерод-углеродных связей и образуется смесь продуктов окисления.
4.6. Реакция Канниццаро -Тищенко
Эта реакция (которую также называют дисмутацией, диспропорциони-рованием, оксо-редукцией) характерна только для альдегидов, у которых отсутствует атом водорода при -углеродном атоме.

4.7. Реакции полимеризации.
Эти реакции характерны, в основном, для альдегидов. 3640% раствор формальдегида в воде называют формалином. При длительном стоянии раствора выпадает белый осадок в виде белых хлопьев. Этот осадок представляет собой полимер параформ.
Образование полимера можно рассматривать как последовательное нуклеофильное присоединение молекул формальдегида. Линейная полимеризация формальдегида:
 Реакция
формальдегида с аммиаком приводит к
образованию уротропина. Реакции
альдегидов и кетонов с аммиаком
осложняются тем, что первоначальные
продукты (см. выше) в дальнейшем могут
циклизоваться:
Реакция
формальдегида с аммиаком приводит к
образованию уротропина. Реакции
альдегидов и кетонов с аммиаком
осложняются тем, что первоначальные
продукты (см. выше) в дальнейшем могут
циклизоваться:

Уротропин используется как дезинфицирующее средство при воспалении мочевых путей. Препарат эффективен, если моча дает кислую реакцию, так как уротропин расщепляется с выделением формальдегида только в кислой среде. Уротропин входит в состав ряда лекарственных препаратов, например, кальцекса.
Получение альдегидов и кетонов
а) получение альдегидов (на примере этаналя):

б) получение кетонов (на примере ацетона):

4.9. Медико-биологическое значение соединений с карбонильной группой
Альдегидная группа (HCO) обуславливает наркотическое действие и дезинфицирующие свойства. Карбонильную группу содержат в своем соста-ве многие биоорганические соединения, которые участвуют во многих мета-болических процессах (моносахариды, олигосахариды, оксокислоты, актив-ная форма витамина В6 – пиридоксаль, кофермент пиридоксальфосфат).
Отдельные представители альдегидов и кетонов
|
|
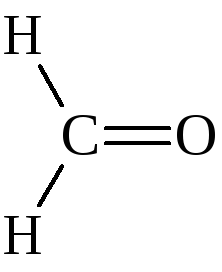
Формальдегид бесцветный газ с резким запахом. Ядовит. 40% раствор формальдегида формалин применяется в медицине как дезинфицирующее средство и консервант анатомических препаратов. Используется для получения уротропина, который применяют в качестве лекарственного препарата. |
|
|
Хлоральгидрат применялся в качестве успокаивающего и снотворного средства. |
|
|
Уксусный альдегид (ацетальдегид) жидкость с неприятным запахом. В промышленных условиях используется для получения альдолей и ацеталей. |
|
|
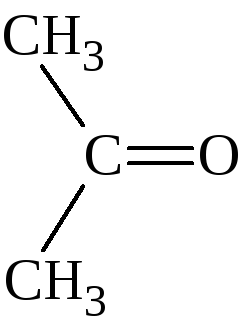
Ацетон (диметилкетон) бесцветная жидкость с характерным запахом. Применяется как реагент в многочисленных реакциях органического синтеза. |