
- •1 Вопрос. Физико-химические свойства.
- •2 Вопрос
- •Цветные реакции на белки.
- •3 Вопрос. Белки, их биологическая роль:
- •4 Вопрос Совместные представления о пространственной структуре белков.
- •5 Вопрос. Общая характеристика сложных белков: нуклеотиды, хромопротеиды, фосфопротеиды, гликопротеиды, липопротеиды.
- •6 Вопрос Расщепление аминокислот в печени.
- •7 Вопрос Хромопротеиды и их физиологическая функция.
- •8 Вопрос Обмен белков.
- •Переваривание
- •Пять основных путей метаболизма аминокислот.
- •9 Вопрос
- •10 Вопрос Биосинтез белка. Регуляция синтеза.
- •Главные открытия 50-х годов 20 века.
- •Стадии биосинтеза
- •Моменты инициирования
- •Генетический код и его характеристики.
- •11. Рибосомы, их строение и функции в синтезе белка. Инициация биосинтеза. Элонгация, терминация.
- •12.Регуляция биосинтеза
- •13 Вопрос Строение ферментов
- •Свойства ферментов.
- •14 Вопрос Ингибирование ферментов. Ингибиторы.
- •Обратимое ингибирование. Типы.
- •15 Вопрос Отличие белков-ферментов от других катализаторов.
- •Химизм ферментативной реакции. Факторы, влияющие на способность фермента ускорять реакцию.Пример.
- •Факторы, влияющие на способность ферментов ускорять реакцию.
- •16 Вопрос. Мультиферментные системы.
- •Изоферменты
- •17 Вопрос. Регуляторные ферменты (регуляция ферментативной активности).
- •Аллостерическая регуляция.
- •18 Вопрос
- •3 Класс – гидролазы
- •19 Вопрос
- •2 Класс – трансфераза
- •20 Вопрос
- •22 Вопрос. Оксидоредуктазы
- •23 Вопрос. Биоэнергетика. Биологическое окисление.
- •Аэробные (флабиновые) ферменты.
- •Коанзим – ку (убиксины)
- •Оксидазы
- •Цитохромы.
- •Процесс окисления начинается с окисления субстрата:
- •Энергетический обмен:
- •24. Окислительное фосфорилирование, сопряженное с дыханием. Теория Митчела.
- •25. Нуклеопротеиды. Их строение. Биологически важные моно - , динуклеотиды.
- •26. Рнк – локализация в клетке, микро и макроструктура. Биологическая роль.
- •27. Днк – структура, нуклеотидный состав, принципы комплиментарности и ее биологическая роль.
- •28. Углеводы, их биологическая роль, классификация. Структура и свойства моносахаридов.
- •29. Строение и свойства дисахаридов.
- •30 Вопрос. Гетерополисахариды
- •31 Вопрос. Обмен углеводов
- •Инсулин
- •Глюкогон
- •32 Вопрос Гликолиз (распад глюкозы)
- •Гликолиз
- •Спиртовое брожение
- •33 Вопрос. Цикл Кребса
- •Пентозный цикл
- •34 Вопрос. Липиды Классификация. Наименование липидов. Основные понятия
- •35 Вопрос. Фосфолипиды (мембранные липиды)
- •Глицерофосфолипиды
- •Сфингофосфолипиды
- •Желчные кислоты
- •38. Синтез триглицеридов и фосфоглицеридов.
- •39Вопрос. Обмен липидов. Внутриклеточное превращение. Кетонные тела.
- •Внутриклеточное превращение
- •40 Вопрос Кетонные тела
32 Вопрос Гликолиз (распад глюкозы)
Углеводы могут расщепляться в аэробных и в анаэробных условиях. В основном расщеплению подвергается глюкоза.
Гликолиз
- анаэробный процесс (хронологически создан раньше) расщепления глюкозы. Характерен и микроорганизмам, и растениями, и животным. последовательность гликолитических реакций различается у организмов характером регуляции скорости и метаболической судьбой образования пирулата. Процесс гликолиза в общем содержит 10 реакций:


Следующие стадии способствуют накоплению Е.
Глицеральальдегидфосфатдегидрогеназа


Выделилось 2 молекулы АТФ. Выигрыш энергии составляют эти 2 молекулы АТФ.
Если процесс гликолиза в скелетной мышце, то он не завершается гликолизом. Пировиноградная кислота далее расщепляется в анаэробных условиях (восстановление до молочной кислоты).

Спиртовое брожение
Если процесс происходит в дрожжевых клетках, то пировиноградная кислота подвергается спиртовому брожению.
Процесс декарбоксилирования

Все процессы брожения – анаэробные.

Анаэробное расщепление пировиноградной кислоты. Пировиноградная кислота, образуется в анаэробных условиях или молочная кислота превращается под действием НАД+:

33 Вопрос. Цикл Кребса
Ацетилкоанзм-А расщепляется в универсальном цикле Кребса. Образование его происходит под действием мультиферм.системы – пируват декарбоксилазный комплекс. У млекопитающих (эукариот) эта система находится в митохондриях, у прокариот – в цитоплазме. Состоит комплекс из 5-ти коферментов: тиаминпирофосфат, липоевая кислота, коанзим А, ФАД, НАД+.
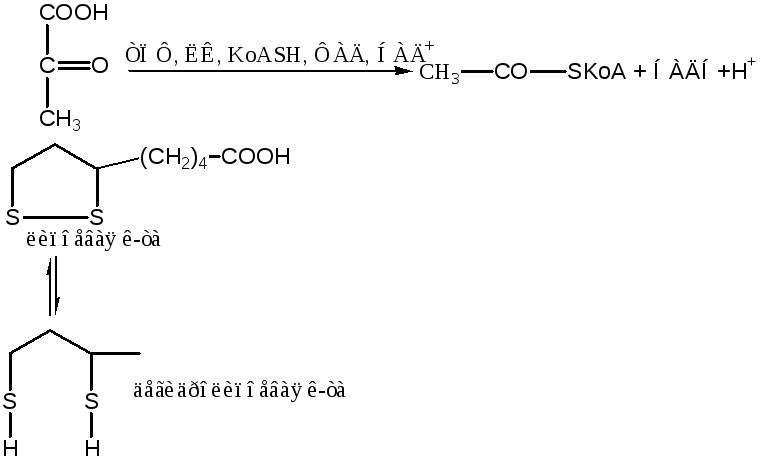


Цикл трикарбоновых кислот (Кребса) был открыт и доказан Кребсом в 1953г, получил за это Нобелевскую премию.
Было доказано, что цикл локализован во внутр.мембране метохондрий. Все ферменты находятся либо в матриксе, либо во внутренней мембране:
Аконитаза, сукцинатдегидрогеназа.
В матриксе:- пируватдегидрогеназный комплекс;
- цитрат синтетаза;
- изоцитратдегидрогеназа;
- α-кетоглутаратдегидрогеназный комплекс;
- фумараза;
- малатдегидрогеназа;
Щавелевая кислота.

E’ – регуляторный фермент. Реакция лимитирует общую скорость цикла лимонной кислоты.
Цитрат -> изоцитрат

E’’ – сложный фермент, содержитFeи кислотнолабильный атомS
Изоцитрат дегидрируется с образованием α кетоглутаровой к-ты.

Образовавшийся α – кетоглутарат окисляется до сукцината.
ГТФ + АДФ –> ГДФ + АТФ
Под действием ФАД – дегидрогиназы образуется фумаровая кислота

В цикле Кребса 12 молекул АТФ.
Живые клетки научились использовать этот процесс расщепления в свою пользу. При расщеплении 1 молекулы глюкозы образуется 36 молекул АТФ (аэробные условия) и 2 в анаэробных.
Реакции гликолиза обратимые.
Пентозный цикл
Часть глюкозы может расщепляться другим способом. Существует важный цикл – фосфоглюконатный (пентозный). Образуются пентозы, гептозы и октозы, именно этот путь расщепления способствует образованию НАДФН+Н+, необходимых для синтеза жирных кислот.
Имеет 2 фазы. Все реакции протекают в цитоплазме и ядрах. Первая фаза окислительная. Она сопровождается окислением глюкозо-6-фосфата, вторая фаза не окислительная, представляет собой взаимопревращение 3,4,5,7 и 8 углеродных сахарофосфатов, в результате чего регенирируется глюкозо-6-фосфат.
Е – глюкозо-6-фосфатдегидроназа ->
НАДН+H+- небелковая часть
глюконо-δ-лактон

Иногда пентозный цикл и заканчив-ся на образовании этих пентоз.
Вторая стадия (реакции) цикла аналогична во многом реакции фотосинтеза.
Очень важны 2 типа реакций, протекающих под действием фермента транскеталазы и трансальдолазы. Они же действуют в фотосинтезе. Транскеталаза переносит СН2ОН-С=О. Перенос осуществляется с кетулоза 5-фосфат на рибоза 5-фосфат.
Образуется глицерин альдегид.

Трансальдолаза переносит СН2ОН, С=О, НО-Н на глицеринвый альдегид.

Транскеталазная реакция. Переносится фрагмент кселюлоза-5-Р-продукт 1 фазы, взаимодействует с эритрозой 4-Р, происходит перенос группы O=C-CH2OHна эритрозу 4-P
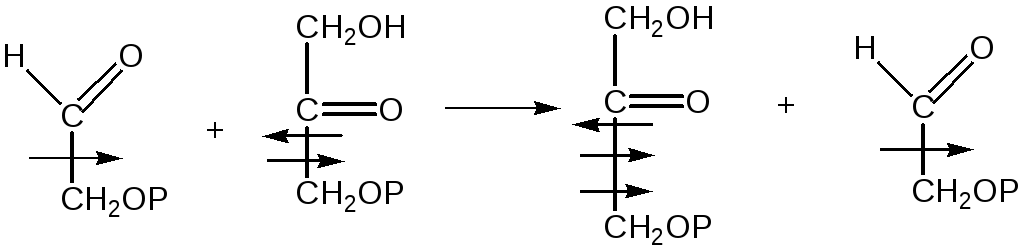

В этом цикле м.б. выделены все эти продукты.
Фотосинтезирующие растения способны улавливать солнечную энергию и запасать ее в форме АТФ и НАДФН+Н+.
Они служат источником для синтеза углеводов в растительных клетках. Солнечная энергия помогает утилизировать углекислый газ и др.в-ва, запасаться углеводами, углекислый газ и кислород постоянно циркулируют, проходя через биосферу за счет фотосинтеза. Ежегодно растительный мир генерирует за счет солнечной энергии не менее 10^(17) ккал свободной энергии, что в 10 раз превышает энергию полезных ископаемых, потребляемое за год всем населением земного шара.
Глюкоза -> глюкуроновая + аскорбинова к-та. Глюкоза -6 Р под действием Ф превращается в глюкозу -1-Р


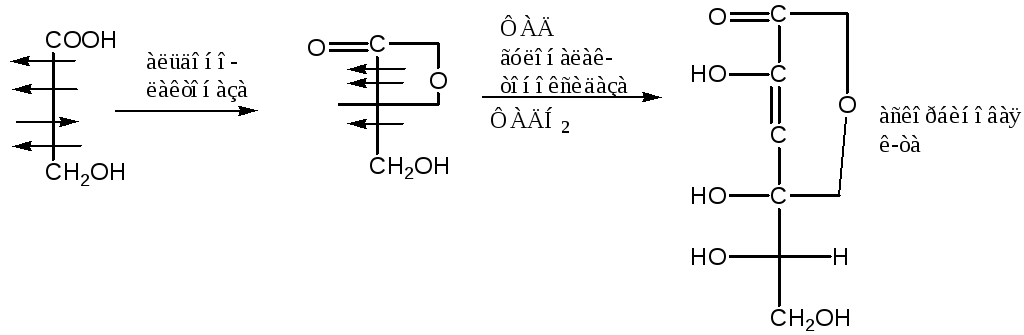
Так синтезируется витамин С. В организме не образуется, т.к. отсутствует гулонолактоноксидаза => получают извне.
