
- •1 Вопрос. Физико-химические свойства.
- •2 Вопрос
- •Цветные реакции на белки.
- •3 Вопрос. Белки, их биологическая роль:
- •4 Вопрос Совместные представления о пространственной структуре белков.
- •5 Вопрос. Общая характеристика сложных белков: нуклеотиды, хромопротеиды, фосфопротеиды, гликопротеиды, липопротеиды.
- •6 Вопрос Расщепление аминокислот в печени.
- •7 Вопрос Хромопротеиды и их физиологическая функция.
- •8 Вопрос Обмен белков.
- •Переваривание
- •Пять основных путей метаболизма аминокислот.
- •9 Вопрос
- •10 Вопрос Биосинтез белка. Регуляция синтеза.
- •Главные открытия 50-х годов 20 века.
- •Стадии биосинтеза
- •Моменты инициирования
- •Генетический код и его характеристики.
- •11. Рибосомы, их строение и функции в синтезе белка. Инициация биосинтеза. Элонгация, терминация.
- •12.Регуляция биосинтеза
- •13 Вопрос Строение ферментов
- •Свойства ферментов.
- •14 Вопрос Ингибирование ферментов. Ингибиторы.
- •Обратимое ингибирование. Типы.
- •15 Вопрос Отличие белков-ферментов от других катализаторов.
- •Химизм ферментативной реакции. Факторы, влияющие на способность фермента ускорять реакцию.Пример.
- •Факторы, влияющие на способность ферментов ускорять реакцию.
- •16 Вопрос. Мультиферментные системы.
- •Изоферменты
- •17 Вопрос. Регуляторные ферменты (регуляция ферментативной активности).
- •Аллостерическая регуляция.
- •18 Вопрос
- •3 Класс – гидролазы
- •19 Вопрос
- •2 Класс – трансфераза
- •20 Вопрос
- •22 Вопрос. Оксидоредуктазы
- •23 Вопрос. Биоэнергетика. Биологическое окисление.
- •Аэробные (флабиновые) ферменты.
- •Коанзим – ку (убиксины)
- •Оксидазы
- •Цитохромы.
- •Процесс окисления начинается с окисления субстрата:
- •Энергетический обмен:
- •24. Окислительное фосфорилирование, сопряженное с дыханием. Теория Митчела.
- •25. Нуклеопротеиды. Их строение. Биологически важные моно - , динуклеотиды.
- •26. Рнк – локализация в клетке, микро и макроструктура. Биологическая роль.
- •27. Днк – структура, нуклеотидный состав, принципы комплиментарности и ее биологическая роль.
- •28. Углеводы, их биологическая роль, классификация. Структура и свойства моносахаридов.
- •29. Строение и свойства дисахаридов.
- •30 Вопрос. Гетерополисахариды
- •31 Вопрос. Обмен углеводов
- •Инсулин
- •Глюкогон
- •32 Вопрос Гликолиз (распад глюкозы)
- •Гликолиз
- •Спиртовое брожение
- •33 Вопрос. Цикл Кребса
- •Пентозный цикл
- •34 Вопрос. Липиды Классификация. Наименование липидов. Основные понятия
- •35 Вопрос. Фосфолипиды (мембранные липиды)
- •Глицерофосфолипиды
- •Сфингофосфолипиды
- •Желчные кислоты
- •38. Синтез триглицеридов и фосфоглицеридов.
- •39Вопрос. Обмен липидов. Внутриклеточное превращение. Кетонные тела.
- •Внутриклеточное превращение
- •40 Вопрос Кетонные тела
22 Вопрос. Оксидоредуктазы
Делим на 2 группы:
Дегидрогеназы, они катализируют дегидрировании субстратов с использованием в качестве акцепторов водорода любые молекулы, кроме молекулы О.
Оксидазы – катализируют окисление субстрата молекулярным кислородом в качестве акцептора водорода.
1 1 1 1 Донор – спиртовая группа алкоголь НАД+оксидоредуктаза (наддегидрогеназа)
С пиртовая
акцепторH+
пиртовая
акцепторH+
группа-донор является НАД+

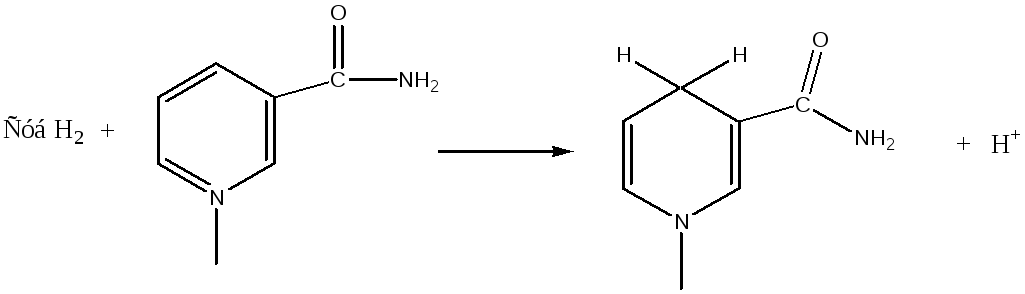
НАД+- небелковая часть дегидрогеназы; выполняет каталитическую функцию (никотинамидадениндинуклеотид).

Обладает витаминной активностью (витамин РР)
1 .1.2
.1.2
Акцептор цитохром
1.1.3 – акцептор кислорода
1. 1. 3. 4. β-Д- глюкоза: кислородоредуктаза
Донор акцептор

1. 2 – альдегидная группа доноров
1. 2. 1 – акцептор НАД+
1. 2. 1. 12. – Д-глицеральдегид 3 фосфат: НАД+оксидоредуктаза

23 Вопрос. Биоэнергетика. Биологическое окисление.
Все клетки тканей дышат: поглощают кислород, выделяют углекислый газ и воду.
Вода образуется в результате ОВР, где субстраты отдают электроны или протоны, то есть окисляются и атомы Н переносятся с водорода на кислород, образуется молекула воды. Субстрат становится пригодным для дальнейшего расщепления. Дыхание связано с фосфорилированием (запасание энергии, высвободившейся в результате дыхания из АТФ).
В процессе окисления участвуют оксидоредуктаза (оксидоредуктазы переносят Н+, и оксидазы – перенос электронов).
Дегидрогеназы могут быть 2-ух типов:
НАД+ и НАДФ+
Аэробные – ФАД дегидрогеназы и ФМН
Отличие анаэробных от аэробных – аэробные могут переносить Н на кислород, а анаэробные не могут.
Всего 150 НАД дегидрогеназ (отличаются белковой частью). Впервые были открыты в 1933 г Варгутом и Эйлером.
В клетках есть фермент – трансгидрогеназа. Под его действием происходит обратимый перенос атомов Н с одной молекулы на другую:
НАД + Н++ НАДФ+↔ НАДФН + НАД++ Н+
Аэробные (флабиновые) ферменты.
Желтые дыхательные ферменты. В качестве простетических групп содержат (флавит) фосфорный эфир. Рибофлавина (витамин В2– имеет желтый цвет, выделен из дрожжей).
Фловинмононуклеотид содержит изоаллоксазиновое кольцо:

Перенос атома Н с помощью дыхательных ферментов:

Впервые выделены флавиновые ферменты Куном в 30-е гг 20 столетия. Была определена связь с витаминами В. В окисленной форме интенсивно окрашены (красный, коричневый, зеленый цвета). Кроме того: ФАДН2+ О2→ Н2О2+ ФАД
Может происходить перенос Н на кислород – аэробные дегидрогеназы.
Коанзим – ку (убиксины)
Коанзим – КУ (убиксины) - это жирорастворимый компонент дыхания, в большом количестве находится в мембранах (растворены в двойном липидном слое). Имеют роль хиноидную структуру. Открыты в 19 веке, роль в процессе дыхания выяснена не так давно.

Пластоксинон: n=9,λmax= 252 Нм
В печени у человека n=10
Убикиноны могут вклиниваться в процессы окисления – восстановления

Оксидазы
Оксидазы – дыхательные ферменты (цитохромы), были открыты в 1886 г Муном и роль в дыхании выяснена в 30-40-ых гг 20-го века.
Цитохромы– белки, участвующие в переносе электронов в аэробных клетках, включаются в процесс дыхания последовательно. Всего описано 5 типов, которые отличаются белковой частью и формой небелкового компонента – гемма (различие вRпротопорферинового кольца).

