
- •1 Вопрос. Физико-химические свойства.
- •2 Вопрос
- •Цветные реакции на белки.
- •3 Вопрос. Белки, их биологическая роль:
- •4 Вопрос Совместные представления о пространственной структуре белков.
- •5 Вопрос. Общая характеристика сложных белков: нуклеотиды, хромопротеиды, фосфопротеиды, гликопротеиды, липопротеиды.
- •6 Вопрос Расщепление аминокислот в печени.
- •7 Вопрос Хромопротеиды и их физиологическая функция.
- •8 Вопрос Обмен белков.
- •Переваривание
- •Пять основных путей метаболизма аминокислот.
- •9 Вопрос
- •10 Вопрос Биосинтез белка. Регуляция синтеза.
- •Главные открытия 50-х годов 20 века.
- •Стадии биосинтеза
- •Моменты инициирования
- •Генетический код и его характеристики.
- •11. Рибосомы, их строение и функции в синтезе белка. Инициация биосинтеза. Элонгация, терминация.
- •12.Регуляция биосинтеза
- •13 Вопрос Строение ферментов
- •Свойства ферментов.
- •14 Вопрос Ингибирование ферментов. Ингибиторы.
- •Обратимое ингибирование. Типы.
- •15 Вопрос Отличие белков-ферментов от других катализаторов.
- •Химизм ферментативной реакции. Факторы, влияющие на способность фермента ускорять реакцию.Пример.
- •Факторы, влияющие на способность ферментов ускорять реакцию.
- •16 Вопрос. Мультиферментные системы.
- •Изоферменты
- •17 Вопрос. Регуляторные ферменты (регуляция ферментативной активности).
- •Аллостерическая регуляция.
- •18 Вопрос
- •3 Класс – гидролазы
- •19 Вопрос
- •2 Класс – трансфераза
- •20 Вопрос
- •22 Вопрос. Оксидоредуктазы
- •23 Вопрос. Биоэнергетика. Биологическое окисление.
- •Аэробные (флабиновые) ферменты.
- •Коанзим – ку (убиксины)
- •Оксидазы
- •Цитохромы.
- •Процесс окисления начинается с окисления субстрата:
- •Энергетический обмен:
- •24. Окислительное фосфорилирование, сопряженное с дыханием. Теория Митчела.
- •25. Нуклеопротеиды. Их строение. Биологически важные моно - , динуклеотиды.
- •26. Рнк – локализация в клетке, микро и макроструктура. Биологическая роль.
- •27. Днк – структура, нуклеотидный состав, принципы комплиментарности и ее биологическая роль.
- •28. Углеводы, их биологическая роль, классификация. Структура и свойства моносахаридов.
- •29. Строение и свойства дисахаридов.
- •30 Вопрос. Гетерополисахариды
- •31 Вопрос. Обмен углеводов
- •Инсулин
- •Глюкогон
- •32 Вопрос Гликолиз (распад глюкозы)
- •Гликолиз
- •Спиртовое брожение
- •33 Вопрос. Цикл Кребса
- •Пентозный цикл
- •34 Вопрос. Липиды Классификация. Наименование липидов. Основные понятия
- •35 Вопрос. Фосфолипиды (мембранные липиды)
- •Глицерофосфолипиды
- •Сфингофосфолипиды
- •Желчные кислоты
- •38. Синтез триглицеридов и фосфоглицеридов.
- •39Вопрос. Обмен липидов. Внутриклеточное превращение. Кетонные тела.
- •Внутриклеточное превращение
- •40 Вопрос Кетонные тела
13 Вопрос Строение ферментов
Фермент- от латинского “Fermentum” – закваска, “enzume” – в дрожжах
С точки зрения химии, фермент – специфические белки, наделенные определенными свойствами, биокатализаторы.
Могут быть простыми и сложными.
Кроме собственно белка содержат не белковый компонент кофермент.
Холофермент– природный комплекс, состоящий из:
- Апофермента– собственно белок
- Кофермент– небелковая часть
Отдельно они не обладают биологической активностью.
Кофермент– небелковая часть (витамины) происхождение, кофактор - ионы каких-либо металлов (неорганическая часть) или сами металлы, связанные с белковой молекулой.
Белковая частьтермолабильна, высокомолекулярна, обуславливает специфичность фермента и влияет на активность фермента.
Кофермент – низкомолекулярное вещество, выполняет каталитическую функцию.
Строение большинства коферментов известно. Если фермент – простой белок, то его каталитическая функция связана с уникальной третичной структурой молекулы белка.
Активный центр– та часть фермента, которая непосредственно реагирует с субстратом (участник процесса метаболизма).
Фермент– белок, молекула субстрата – НМС. Если фермент – сложный белок, то в его активный центр всегда входит кофермент, белковая часть определяет специфичность данной реакции. Если фермент – простой белок, то реализация активного центра связана с третичной структурой белковой молекулы.
Кроме активного центра в ферментах есть еще другие центры, которые называются аллостерические центры. В этих центрах фермент связывается с какими-то НМС, называемыми эффекторами, модификаторами или модуляторами. Они отличны от молекулы субстратов, они либо активируют, либо дезактивируют фермент.
Свойства ферментов.
Специфичность – ферменты – специфические биокатализаторы. По специфичности их делят на классы
А) ферменты абсолютной специфичности – дейтсвуют на один субтсрат (пр: уреаза под ее действием мочевина расщипляется на углекислый газ и аммиак

Аденаза - дейтсвует на аденин
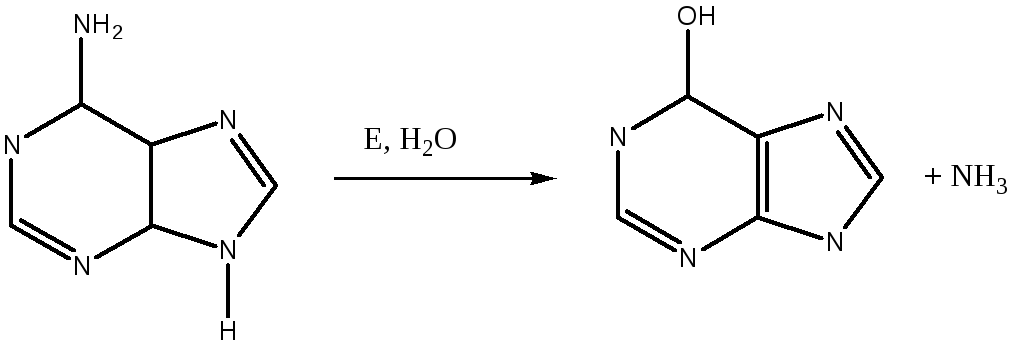
Б) абсолютно-групповая
В) относительно-групповая
Б и В трудно разделить, действуют на связь в субстратах, в которых одна часть у всех одинакова (ПР: гликозидаза: α-гликозидаза расщепляет гликозидные связм глюкозы

Пептидазы: расщепляют все белки в определенном месте, там где есть с С-конца аргинина и лизина.

Хемотрепсин: так же разрушает если есть аминокислота
Липаза: расщепляет жиры по сложно-эфирным связям.
Стереоспецифичность. Ферменты настроены на полипептиды и аминокислоты α –ряда. Фермент фумараза действует на фумаровую кислоту с образованием яблочной.

Фумаровая к-та яблочная кислота
Фермент фумараза действует только на фумаровую кислоту, на малеиновую влияния не оказывает.
β-галаксидаза не расщепляет лактозу, но расщепляет β-галактозу.
Слияние температуры – повышение температуры приводит к повышению скорости химической реакции. Исключение как только температура становится выше 40-600С, происходит разрушение четвертичной и третичной структуры белковой молекулы, при дальнейшем нагревании белок денатурирует, ферментативная реакция дальше не пойдет.
Вывод: все ферменты чувствительны к температуре. Оптимум температуры для человека 36,6 0С.
Влияние рН – реакция среды также существенна для ферментативной реакции. Лдля каждого фермента значение рН специфично.
Пептин (в желудке) рН = 1,5
Трепсин рН = 2,7
Амилаза (в слюне) рН = 6,8-7
Каталаза (в крови) рН = 7,6
Аргеназа (в кишечнике) рН = 9,7
Зависимость скорости ферментативной реакции от концентрации субстрата.
Если ферментативная реакция протекает при оптимальном рН, Т, то ∆υ в зависимости от концентрации субстрата описывается уравнением Михаэлиса-Ментона

υmax – максимальная скорость в данных условиях
К m
–
константа Михаэлиса, определяется как
[S]
на половине экспериментальной кривой.
m
–
константа Михаэлиса, определяется как
[S]
на половине экспериментальной кривой.
Определенная таким образом Кm не точная.
Чем она ниже, тем больше чувствительность к данному субстрату.
Чтобы
Кm
узнать точнее, пользуются обратными
координатами – уравнение
Лайнцивера-Берка:
![]()
![]() (линейная
зависимость)
(линейная
зависимость)

Очень точное определение Km
Каталаза в крови расщепляет перекись водорода до кислорода и воды. Кm = 25 ммоль.
Гексагеназа мозга катализирует реакцию:

Кm = 0,05 ммоль, для АДФ Кm= 0,04 ммоль.
Чтобы клетки мозга не погибли нужна глюкоза.
Единица активности фермента – такое количество фермента, которое катализирует превращение одного микромоль субстрата в одну минуту при 250С и оптимуме рН. Число оборотов фермента – такое число молекул субстрата, которое претерпевает превращение в единицу времени в расчете на одну молекулу фермента.
Пр: карбонатдегидротаза – действует эритроцитах, оборотное число 36 млн в минуту.
