
Вольдман - фхтс часть 1 (2007)
.pdfФедеральное агентство по образованию
Московская государственная академия тонкой химической технологии
им. М.В.Ломоносова
Кафедра химии и технологии наноразмерных и композиционных материалов
Г. М. Вольдман
ФИЗИКА И ХИМИЯ ТВЕРДОФАЗНЫХ РЕАКЦИЙ Часть 1
Учебное пособие
Москва 2007
www.mitht.ru/e-library
ББК 24.5
УДК 541.1
Вольдман Г.М.
Физика и химия твердофазных реакций.
Учебное пособие. – М.: МИТХТ им. М.В.Ломоносова, 2007, 118 с.
Утверждено библиотечно-издательской комиссией МИТХТ им. М.В.Ломоносова в качестве учебного пособия.
Вданном пособии приведены сведения о точечных структурных и
электронных дефектах кристаллической решетки с преобладающей ионной связью и
их роли в реакциях, сопровождающихся образованием твердого продукта.
Рассмотрены механизмы и закономерности возникновения тепловых и
нестехиометрических дефектов, методы расчета их концентрации. Выведены уравнения, описывающие кинетику образования твердых продуктов с преобладающей электронно-дырочной или ионной проводимостью, и
проанализированы закономерности протекания процесса при различных составах и типах разупорядоченности продукта.
Предназначено для студентов, обучающихся на 3 курсе бакалавриата по направлению 551600 «Материаловедение и технология новых материалов» и
изучающих дисциплину «Физика и химия твердофазных систем».
Рецензент:
Зав. кафедрой ХТНиКМ д.т.н. Левинский Ю.В.
© МИТХТ им. М.В.Ломоносова, 2007
2
www.mitht.ru/e-library
|
ОГЛАВЛЕНИЕ |
ВВЕДЕНИЕ.................................................................................................................................................. |
4 |
1. МЕХАНИЗМ ВЗАИМОДЕЙСТВИЯ МЕТАЛЛА С МЕТАЛЛОИДОМ И УСЛОВИЯ, НЕОБХОДИМЫЕ |
|
ДЛЯ ПРОТЕКАНИЯ ПРОЦЕССА ................................................................................................................ |
6 |
1.1.МЕХАНИЗМ ПРОЦЕССА…………………………………………………………………………………………...6
1.2.ПЕРЕМЕЩЕНИЕ ИОНОВ ПОД ДЕЙСТВИЕМ ЭЛЕКТРИЧЕСКОГО ПОЛЯ…………………………………………….8
1.2.1. Характер перемещения ионов в идеальной кристаллической решетке |
.................................. 8 |
1.2.2. Перемещение ионов в неидеальной кристаллической решетке ............................................. |
9 |
2. ОБРАЗОВАНИЕ ТЕПЛОВЫХ ДЕФЕКТОВ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ...................................... |
13 |
2.1.ОБЩИЕ ПОЛОЖЕНИЯ……………………………………………………………………………………………...13
2.2.ВОЗНИКНОВЕНИЕ ТОЧЕЧНЫХ СТРУКТУРНЫХ ДЕФЕКТОВ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ В РЕЗУЛЬТАТЕ
ТЕПЛОВОГО ДВИЖЕНИЯ……………………………………………………………………………………………... 14
2.2.1. Возникновение точечных структурных дефектов при переходе ионов в междоузлие.......... |
14 |
2.2.2. Возникновение дефектов в результате перехода ионов из объема на поверхность или с |
|
поверхности в объем ........................................................................................................................ |
16 |
2.3.ВОЗНИКНОВЕНИЕ ТЕПЛОВЫХ ЭЛЕКТРОННЫХ ДЕФЕКТОВ……………………………………………………… 21
2.4.КОНСТАНТЫ РАВНОВЕСИЯ ПРОЦЕССОВ ОБРАЗОВАНИЯ ТЕПЛОВЫХ ДЕФЕКТОВ……..…………………….…22
2.4.1. Константа равновесия образования дефектов по Френкелю в катионной подрешетке ....... |
22 |
2.4.2. Константы равновесия образования других тепловых дефектов.......................................... |
26 |
2.4.3. Расчет равновесной концентрации тепловых дефектов........................................................ |
28 |
2.4.4. Типы структурной разупорядоченности кристаллов .............................................................. |
31 |
2.4.5. Распространенность различных типов разупорядоченности................................................. |
34 |
3. ОБРАЗОВАНИЕ ДЕФЕКТОВ НЕСТЕХИОМЕТРИИ............................................................................. |
37 |
3.1. ТОЧЕЧНЫЕ СТРУКТУРНЫЕ ДЕФЕКТЫ, ОБУСЛОВЛЕННЫЕ ОТКЛОНЕНИЕМ СОСТАВА |
|
ОТ СТЕХИОМЕТРИЧЕСКОГО……..………………………………………………………………………………….…37 |
|
3.2.УСЛОВИЯ И МЕХАНИЗМ ОБРАЗОВАНИЯ НЕСТЕХИОМЕТРИЧЕСКОЙ ФАЗЫ……..………………………..….… 39
3.2.1.Связь между давлением газообразного металлоида и составом
равновесной твердой фазы.............................................................................................................. |
39 |
3.2.2. Механизм и равновесие возникновения недостатка металлоида (избытка металла).......... |
41 |
3.2.3. Механизм и равновесие возникновения избытка металлоида (недостатка металла).......... |
45 |
4.ЗАВИСИМОСТИ КОНЦЕНТРАЦИЙ ДЕФЕКТОВ ОТ ДАВЛЕНИЯ МЕТАЛЛОИДА В ГАЗОВОЙ ФАЗЕ48
4.1.ОБЩИЕ ПОЛОЖЕНИЯ……..…………………………………………………………………………………..…48
4.2.СООТНОШЕНИЕ МЕЖДУ КОНСТАНТАМИ РАВНОВЕСИЯ ПРОЦЕССОВ ВОЗНИКНОВЕНИЯ НЕДОСТАТКА И
ИЗБЫТКА МЕТАЛЛОИДА……..………………………………………………………………………….………..….…51
4.3.РАСЧЕТ РАВНОВЕСНЫХ КОНЦЕНТРАЦИЙ ДЕФЕКТОВ ПРИ ЗАДАННОМ ДАВЛЕНИИ МЕТАЛЛОИДА……..………53
|
4.3.1. Составление и решение системы уравнений......................................................................... |
53 |
|
4.3.2. Приближенный метод построения зависимостей концентраций дефектов от давления |
|
|
металлоида ....................................................................................................................................... |
58 |
|
4.4. АНАЛИЗ ХАРАКТЕРА ЗАВИСИМОСТЕЙ КОНЦЕНТРАЦИИ ДЕФЕКТОВ ОТ ДАВЛЕНИЯ МЕТАЛЛОИДА |
|
|
В ГАЗОВОЙ ФАЗЕ……..……………………………………………………………………………….…………….…75 |
|
5. |
ВЛИЯНИЕ ПРИМЕСЕЙ НА РАВНОВЕСИЕ ДЕФЕКТОВ В КРИСТАЛЛЕ............................................. |
77 |
|
5.1. ПРИМЕСИ, ОКАЗЫВАЮЩИЕ НАИБОЛЬШЕЕ ВЛИЯНИЕ НА РАВНОВЕСИЕ ДЕФЕКТОВ....................................... |
77 |
|
5.2. ПРИМЕСИ ЗАМЕЩЕНИЯ С ЗАРЯДОМ КАТИОНОВ, ПРЕВЫШАЮЩИМ ЗАРЯД КАТИОНОВ МАТРИЦЫ................... |
79 |
|
5.3. ПРИМЕСИ ЗАМЕЩЕНИЯ С ЗАРЯДОМ КАТИОНОВ МЕНЬШИМ, ЧЕМ ЗАРЯД КАТИОНОВ МАТРИЦЫ........ |
...............85 |
6. |
МЕХАНИЗМ И ЗАКОНОМЕРНОСТИ ПРОЦЕССА ОБРАЗОВАНИЯ ТВЕРДОГО |
ПРОДУКТА |
(ТЕОРИЯ КАРЛА ВАГНЕРА)..................................................................................................................... |
89 |
|
|
6.1. МЕХАНИЗМ И УСЛОВИЯ ПРОТЕКАНИЯ ПРОЦЕССА….……..………………………………..……………….…89 |
|
|
6.2. ЭЛЕКТРИЧЕСКАЯ СХЕМА ПРОЦЕССА……..…………………………………………………………….…….…90 |
|
|
6.3. СООТНОШЕНИЯ, ОПРЕДЕЛЯЮЩИЕ СИЛУ ТОКА……..………………………...…………………………….… 92 |
|
|
6.4. УРАВНЕНИЯ СКОРОСТИ ОБРАЗОВАНИЯ ТВЕРДОГО ПРОДУКТА.................................................................. |
100 |
|
6.5. ЗАВИСИМОСТЬ КОНСТАНТЫ СКОРОСТИ ОТ ДАВЛЕНИЯ МЕТАЛЛОИДА ........................................... |
.............102 |
|
6.5.1. Возможные лимитирующие стадии процесса ....................................................................... |
102 |
|
6.5.2. Константа скорости реакции при лимитирующем переносе заряда ионами........................ |
102 |
|
6.5.3. Константа скорости реакции при лимитирующем переносе заряда электронами............... |
108 |
|
6.6. АНАЛИЗ ОЖИДАЕМЫХ ЗАКОНОМЕРНОСТЕЙ ПРОЦЕССА С ПОМОЩЬЮ ТЕОРИИ |
|
|
ВАГНЕРА……..……………………………………………………………………………….…….…....................111 |
|
|
6.7. ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ РЕАКЦИЙ С УЧАСТИЕМ МЕТАЛЛА, ИМЕЮЩЕГО |
|
|
НЕСКОЛЬКО УСТОЙЧИВЫХ СТЕПЕНЕЙ ОКИСЛЕНИЯ………………………………………………………………...115 |
|
|
6.7.1. Характер образующейся оболочки........................................................................................ |
115 |
|
6.7.2. Закономерности образования многослойной оболочки........................................................ |
116 |
|
6.7.3. Соотношения между толщиной слоев................................................................................... |
118 |
|
|
3 |
www.mitht.ru/e-library
ВВЕДЕНИЕ
Реакции, протекающие с участием твердых веществ и сопровождающиеся образованием твердого продукта, лежат в основе многих важнейших процессов. К
ним относятся:
Образование соединений металлов с металлоидами (оксидов,
халькогенидов, галогенидов, карбидов и др.):
– синтез из элементов, например, синтез дисульфида молибдена – уникальной твердой смазки:
Mo(тв) + S2 (тв) = MoS2 (тв);
–образование оксидов из сульфидов при обжиге в технологических схемах
переработки минерального сырья цветных и редких металлов:
ZnS(тв) + 2O2 (газ) = ZnSO4 (тв);
MoS2 (тв) + 3,5О2 (газ) = MoО3 (тв) + 2SO2 (газ);
– образование оксидов и других соединений при коррозии металлов и
сплавов, например, Fe2O3 при ржавлении железа
ит.д.
Получение металлов из их твердых соединений восстановлением газообразными или твердыми восстановителями:
– восстановление триоксида вольфрама водородом
WO3 (тв) + 3H2 (газ) = W (тв) + 3H2O(газ);
– восстановление диоксида титана кальцием
TiO2 (тв) +2Ca(тв) = Ti(тв) +2CaO(тв)
ит.д.
Получение материалов типа сложных оксидов – ферритов, гранатов и др. с
уникальными свойствами, в том числе материалов с высокотемпературной
сверхпроводимостью, например, железо-иттриевого граната: 3Y2O3 (тв) + 5Fe2O3 (тв) = 5Y3Fe5O12 (тв)
и другие.
Общая характерная особенность всех перечисленных процессов состоит в том, что образующийся продукт разделяет реагирующие вещества, и это определяет сходство их механизма и кинетических закономерностей. Цель данного курса состоит в рассмотрении механизма и кинетики таких процессов и выработке умения предсказывать их закономерности.
4
www.mitht.ru/e-library
Сходство механизма и закономерностей всех подобных процессов позволяет рассматривать их на простейшем примере. Этим примером может служить реакция с участием одного простого твердого вещества и образованием одного твердого
продукта – реакция синтеза соединения металла при взаимодействии последнего с газообразным металлоидом (кислородом, галогенидами, парами серы и т.д.). В
продуктах таких реакций преобладает ионная связь, и они имеют кристаллическую решетку, состоящую из двух взаимно проникающих подрешеток – катионной и
анионной. В дальнейшем рассматривается только этот тип кристаллической
решетки. |
|
|
|
|
|
|
|||
|
|
В |
общем |
виде |
соединению металл-металлоид отвечает формула |
||||
Me |
Me |
X |
X |
|
MezMe |
X |
XzX |
(здесь символ «·» обозначает соотношение). Например, |
|
|
|
|
Me |
|
|
|
|||
Al2O3 2Al3+·3O2– (на 2 катиона Al3+ приходится 3 аниона Х2–).
При Me = X взаимное расположение катионов и анионов в кристаллической
решетке легко показать в плоскости. А поскольку к схеме кристаллической решетки
придется обращаться постоянно, в качестве иллюстрации будет использоваться
фаза с Me = X и соответственно zMe = zX, отвечающая формуле МеХ; этом для
удобства изложения принято zMe = zX = 2.
5
www.mitht.ru/e-library

1.МЕХАНИЗМ ВЗАИМОДЕЙСТВИЯ МЕТАЛЛА С МЕТАЛЛОИДОМ И УСЛОВИЯ, НЕОБХОДИМЫЕ ДЛЯ ПРОТЕКАНИЯ ПРОЦЕССА
1.1. МЕХАНИЗМ ПРОЦЕССА
Схематическое изображение начального состояния системы, состоящей из 3
фаз – твердого металла, газообразного металлоида (присутствующего в виде двухатомных молекул) и разделяющего их слоя твердого продукта, представлено на
рис. 1.
I |
|
|
II |
|||
|
Ме2+ Х2- |
Ме2+ Х2- |
Ме2+ Х2- |
|
||
|
|
|||||
|
Х2- Ме2+ |
Х2- Ме2+ |
Х2- Ме2+ |
|
||
|
Ме2+ Х2- |
Ме2+ |
Х2- |
Ме2+ Х2- |
|
|
Ме0(тв) |
Х2- Ме2+ |
МеХ(тв) |
Х2- Ме2+ |
Х2 (газ) |
||
Ме2+ Х2- |
Ме2+ Х2- |
|||||
|
|
|
|
|||
|
Х2- Ме2+ |
Х2- Ме2+ |
Х2- Ме2+ |
|
||
|
Ме2+ Х2- |
Ме2+ Х2- |
Ме2+ Х2- |
|
||
|
Х2- Ме2+ |
Х2- |
Ме2+ |
Х2- Ме2+ |
|
|
|
|
|
|
|
|
|
Рис. 1. Начальное состояние системы металл (Ме0(тв)) –твердый продукт (МеХ) –
– газообразный металлоид (Х2 (газ))
I и II – поверхности (границы) раздела фаз (соответственно Ме0/МеХ и МеХ/Х2)
Реакция Mе(тв) + 1/2 Х2 (газ) = MеХ(тв) окислительно-восстановительная:
Ме0 → Ме2+ + 2е–
1/2 Х20 + 2е– → Х2–
Ме0 + 1/2 Х20 → Ме2+ + Х2–;
окисление металла Ме0 с образованием катионов Ме2+ протекает на поверхности,
примыкающей к границе I, а восстановление металлоида Х20 – на границе II (рис. 2),
и электроны должны переходить от границы I к границе II сквозь слой МеХ.
6
www.mitht.ru/e-library
|
I |
|
|
|
II |
|||||
|
|
|
Ме2+ Х2- |
Ме2+ |
Х2- |
Ме2+ Х2- |
|
|
|
|
|
|
|
|
|
||||||
|
Ме2+ |
Х2- Ме2+ |
Х2- |
Ме2+ |
Х2- |
Ме2+ |
|
Х2– |
|
|
|
Ме2+ |
|
|
|||||||
|
Ме2+ Х2- |
Ме2+ |
Х2- |
Ме2+ |
Х2- |
|
Х2– |
|
||
|
Ме2+ |
|
|
|||||||
|
Х2- Ме2+ |
|
|
Х2- |
Ме2+ |
|
Х2– |
|
||
Ме0(тв) |
Ме2+ |
МеХ(тв) |
|
|
||||||
Ме2+ Х2- |
Ме2+ |
Х2- |
|
Х2– Х |
2 (газ) |
|||||
|
Ме2+ |
|
|
|
|
|||||
|
Х2- Ме2+ |
Х2- |
Ме2+ |
Х2- |
Ме2+ |
|
Х2– |
|
||
|
Ме2+ |
|
|
|||||||
|
Ме2+ Х2- |
Ме2+ |
Х2- |
Ме2+ Х2- |
|
Х2– |
|
|||
|
Ме2+ |
|
|
|||||||
|
Х2- Ме2+ |
Х2- |
Ме2+ |
Х2- |
Ме2+ |
|
Х2– |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 2. Система с образовавшимися на границах раздела фаз ионами
Но переход электронов от металла к металлоиду вовсе не является достаточным условием для протекания процесса. Во-первых, образование катионов и анионов само по себе не приводит к увеличению толщины слоя продукта,
поскольку для этого нужно возникновение новых плоскостей кристаллической решетки, в каждой из которых одновременно присутствуют ионы Ме2+ и Х2–,
располагающиеся в шахматном порядке. А во-вторых, появление на границе I
катионов, а на границе II анионов приводит к появлению электрического поля,
препятствующего перемещению электронов; очевидно, по мере накопления катионов и анионов напряженность поля растет, и в конце концов перемещение электронов и возникновение новых катионов и анионов станет невозможным – процесс прекратится.
И для образования новых плоскостей кристаллической решетки, и для понижения разности потенциалов между границами, очевидно, необходимо одно и то же – чтобы катионы Ме2+ переходили от границы I к границе II или анионы Х2–
переходили от границы II к границе I и анионы Х2–. В результате такого перехода они окажутся в одной плоскости и скомпенсируют заряды друг друга. Таким образом,
протекание процесса возможно только при направленном перемещении в
кристаллической решетке продукта катионов от границы I к границе II или анионов
от границы II к границе I.
7
www.mitht.ru/e-library
Для направленного перемещения ионов необходима, во-первых, движущая сила, а во-вторых, возможность перемещения под действием этой силы.
Движущую силу создает электростатическое поле, возникающее в результате появления катионов Ме2+ на границе I и анионов Х2– на границе II. Сила,
действующая в этом поле на катионы, создает тенденцию к их перемещению от
границы I к границе II, а сила, действующая на анионы, – к перемещению от границы
II к границе I, что и нужно для построения новых плоскостей кристаллической решетки продукта.
Возможность перемещения ионов в кристаллической решетке обеспечивается их тепловым движением. Ионы, находящиеся в узлах кристаллической решетки,
колеблются, причем энергия тепловых колебаний перераспределяется между ними случайным образом и соответственно случайным образом меняется амплитуда колебаний. Время от времени ион получает энергию, достаточную для того, чтобы перейти из своего узла в другое возможное место. При отсутствии движущей силы
направления перемещения ионов случайные, и их блуждания хаотичны; эти
блуждания лежат в основе диффузии – процесса выравнивания состава кристалла при наличии катионов и анионов разных видов. Но к образованию твердого продукта
при взаимодействии металла и металлоида приводит только направленное
перемещение ионов в кристаллической решетке продукта; условия,
обеспечивающие возможность именно такого перемещения, рассмотрены ниже.
1.2.ПЕРЕМЕЩЕНИЕ ИОНОВ ПОД ДЕЙСТВИЕМ ЭЛЕКТРИЧЕСКОГО ПОЛЯ
1.2.1.Характер перемещения ионов в идеальной кристаллической решетке
Видеальной кристаллической решетке все катионы и анионы находятся только в узлах соответственно катионной и анионной подрешеток и все узлы заняты.
Вэтом случае перемещение катиона из занимаемого им узла в соседний возможно только путем обмена местами с соседним катионом (рис. 3). Но при этом пространственное расположение катионов не изменяется – т.е. направленное перемещение под действием электрического поля не происходит. Точно так же,
очевидно, нет и направленного перемещения анионов.
Таким образом, несмотря на наличие движущей силы, направленное перемещение ионов в идеальной кристаллической решетке невозможно.
8
www.mitht.ru/e-library

Ме2+ Х2- Ме2+ Х2- Ме2+ Х2-
Х2- Ме2+ Х2-  Ме2+ Х2- Ме2+
Ме2+ Х2- Ме2+
Ме2+ Х2- Ме2+ Х2- Ме2+ Х2-
Х2- Ме2+ Х2-
Х2- Ме2+ Х2- Ме2+ Х2- Ме2+
Сила, действующая на катионы
Рис. 3. Перемещение катионов в идеальной кристаллической решетке
1.2.2.Перемещение ионов в неидеальной кристаллической решетке
Неидеальный ионный кристалл может содержать следующие точечные
дефекты структуры:
1)не занятые (вакантные) узлы в катионной подрешетке («вакансии в катионной подрешетке», или кратко «вакансии катионов»);
2)вакансии в анионной подрешетке (вакансии анионов);
3)катионы в междоузлиях;
4)анионы в междоузлиях;
5)дефекты антиструктуры (катион, находящийся в узле анионной
подрешетки; анион, находящийся в узле катионной подрешетки).
Дефекты антиструктуры встречаются редко и не участвуют в перемещении ионов (диффузионно не активны), поэтому в дальнейшем обсуждении не рассматриваются.
Возможность направленного перемещения ионов при наличии остальных точечных структурных дефектов – вакансий и ионов в междоузлиях – обсуждается вначале на примере перемещения катионов.
Перемещение катионов при наличии вакансий
в катионной подрешетке
При наличии в катионной подрешетке вакансии в нее под действием
электрического поля может переместиться соседний катион (рис. 4, а). В результате
вакантным окажется узел, из которого ушел катион, и в него сможет переместиться следующий катион (рис. 4, б); после ряда перемещений вакансия окажется в
9
www.mitht.ru/e-library
положении, показанном на рис. 4, в.
Х2- Ме2+ Х2- Ме2+ Х2 -
Ме2+ Х2- Ме2+ Х2- Ме2+ Х2-
Х2-
Сила, действующая на катионы
Х2- Ме2+ |
Х2- Ме2+ |
Х2- |
Ме2+ |
Ме2+ Х2- Ме2+ Х2- |
|
Х2- |
|
Сила, действующая на катионы |
|||
Х2- Ме2+ |
Х2- Ме2+ |
Х2- |
Ме2+ |
Х2- |
Ме2+ Х2- |
Ме2+ |
Х2- |
Сила, действующая на катионы
а
б
в
Рис. 4. Последовательное перемещение катионов при наличии вакансии в катионной подрешетке
Изменение положения вакансии соответствует переходу катиона,
находившегося в крайнем левом положении, в крайнее правое положение – т.е.
направленному перемещению катиона под действием движущей силы (в
направлении от границы I к границе II). Таким образом, наличие вакансий в
катионной подрешетке обеспечивает возможность направленного перемещения катионов.
Перемещение катионов при возможности их нахождения в
междоузлиях
Схема перемещения катионов в направлении движущей силы в случае
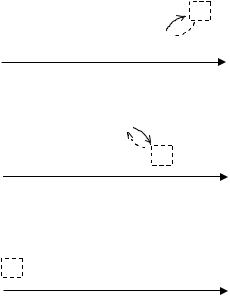
возможности их нахождения в междоузлиях (т.е. при наличии дефекта «катионы в междоузлиях») показана на рис. 5.
На каждом шаге находящийся в междоузлии катион, «подталкиваемый» электрическим полем, вытесняет из ближайшего в направлении движения узла катион в соседнее междоузлие (рис. 5, а, б), а сам становится на его место (в теории
10
www.mitht.ru/e-library
