
Вольдман - фхтс часть 1 (2007)
.pdfА теперь рассмотрим, какие результаты должны получиться в следующем эксперименте: кристалл МеХ стехиометрического состава помещают в герметичный
сосуд с регулируемым давлением металлоида и устанавливают сначала |
P |
=P0 |
||||||
|
|
|
|
|
|
|
X2 |
X2 |
(опыт 1), затем P |
≤P |
<P0 |
(опыт 2), а потом P0 |
<P |
≤P |
(опыт 3), причем в |
||
X2 min |
X2 |
X2 |
X2 |
X2 |
X2 max |
|
|
|
каждом из опытов в системе устанавливается равновесие. |
|
|
|
|||||
Очевидно, в первом опыте состав твердой фазы не изменится – |
кристалл |
|||||||
останется стехиометрическим. Во втором опыте твердая фаза станет нестехиометрической с избытком металла (недостатком металлоида), и это значит,
что некоторое количество металлоида, присутствующего в кристалле в виде
анионов, уйдет из него в газовую фазу, в которой металлоид присутствует в составе
молекул Х2. А в третьем опыте кристалл приобретет избыток металлоида в результате превращения некоторого количества молекул Х2 в дополнительные анионы.
3.2.2. Механизм и равновесие возникновения недостатка
металлоида (избытка металла)
При образовании кристалла из металла (Ме0) и газообразного металлоида (Х2)
металлоид превращался в анионы, принимая электроны, отдаваемые металлом.
Очевидно, при выходе металлоида из кристалла в газовую фазу должен протекать
обратный процесс – анионы превращаются в молекулы Х2, отдавая электроны, при
этом в кристаллической решетке появляются избыточные электроны,
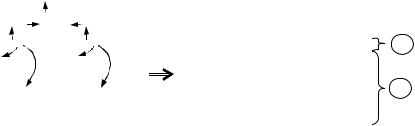
размещающиеся в зоне проводимости. Этот процесс состоит из трех последовательных стадий (рис. 14, а):
1) анионы, находящиеся на поверхности, отдают электроны, которые переходят в объем кристалла, и превращаются в нейтральные атомы; эти атомы выходят из кристаллической решетки в адсорбционный слой:
2X2X2 пов 2X0адс + 4e–;
2) атомы X0адс объединяются в адсорбционном слое в молекулу X02 адс:
2X0адс X02 адс;
3) молекула Х2 десорбируется и уходит в газовую фазу:
X02 адс X02 газ.
41
www.mitht.ru/e-library
Суммарное уравнение процесса имеет вид
2X2X2 пов X02 ↑+ 4e–
или на 1 анион
X2X2 пов |
|
1 |
X20 ↑ + 2e–. |
(45) |
|
||||
|
2 |
|
|
|
В этих уравнениях стрелка, направленная вверх, символизирует переход металлоида из кристалла в находящуюся над ним газовую фазу.
X02 газ
Ме2+ |
Xадс0 |
X20 адс |
Xадс0 |
Ме2+ |
Ме2+ |
|
Ме2+ |
|
Ме2+ |
|
Х2- |
Ме2+ |
Х2- |
e– |
e– |
+ |
|||||
e– |
Ме2+ |
e– |
Ме2+ |
Х2- |
Х2- |
Х2- |
Х2- |
|
||
Х2- |
Х2- |
Ме2+ |
Ме2+ |
– |
||||||
Ме2+ |
e– |
Ме2+ |
e– |
Ме2+ |
e– |
Х2- |
Ме2+ |
Х2- |
e– |
|
Х2- |
Х2- |
Ме2+ |
Ме2+ |
|
а б
Рис. 14. Возникновение избытка металла: процессы, протекающие при уходе металлоида с поверхности кристалла в газовую фазу (а)
исостояние кристалла после ухода металлоида (б)
Врезультате исчезновения анионов в поверхностной плоскости
кристаллической решетки появляется избыток катионов Ме2+ и соответственно
некомпенсированный положительный заряд, а в объеме кристалла в результате
перехода в него электронов – избыточный отрицательный заряд (рис. 14, б).
Возникшее электростатическое поле стремится переместить катионы с
поверхности в объем (в этом случае в объеме появятся межузельные катионы Me2i ),
а анионы из объема на поверхность (с возникновением в объеме вакансий анионов
VX2 ); пока электростатическое поле существует, состояние кристалла остается неравновесным. То, какие из ионов будут перемещаться под действием электростатическое поле, определяется типом разупорядоченности кристалла.
42
www.mitht.ru/e-library
Тип «Френкель»
В кристаллах типа «Френкель» выполняется условие |
f |
f |
, поэтому |
HMei |
< HVX |
||
преобладает переход катионов Ме2+ с поверхности в объем в междоузлия: |
|
||
Me2 |
2 |
Me2 , |
|
|
|
|||
Me |
пов |
|
i |
|
|
|
|
|
и суммарно с уравнением (45) получаем |
|
|||||||
Me2 |
2 X22 |
|
1 |
X20 ↑ + 2e– + Mei2 ; |
(46) |
|||
2 |
||||||||
Me |
|
X |
пов |
|
|
|
||
все стадии процесса обратимы, поэтому обратим и суммарный процесс.
Исключив из уравнения (46) нормальные элементы структуры, получим:
0 |
1 |
X20 ↑ + 2e– + Mei2 . |
(47) |
|
2 |
||||
|
|
|
Константа равновесия этого обратимого процесса (в индексе константы, кроме
типа разупорядоченности, в скобках указывается, какой компонент присутствует в
избытке) имеет вид
KФ(Ме) = |
1/2 |
– 2 |
|
2 |
. |
(48) |
|
PX2 равн (e ) |
Mei |
|
|||||
В дальнейшем |
для |
|
сокращения записей |
индекс «(равн)» опускается – |
|||
равновесное давление металлоида обозначается просто PX2 .
Описание процесса и выражение константы равновесия для более сложных составов кристаллов рассмотрим на примере соединения Ме2Х3, образованного
трехзарядными катионами и двухзарядными анионами.
Уход металлоида в газовую фазу и переход катионов с поверхности в объем
кристалла:
2Me3 |
3 3X22 |
|
3 |
X20 ↑ + 6e– + 2Mei3 |
||
2 |
||||||
Me |
X |
пов |
|
|
||
или, после пересчета на 1 точечный структурный дефект и удаления нормальных структурных элементов,
0 |
3 |
X20 ↑ + 3e– + Mei3 ; |
(49) |
|||
|
||||||
4 |
|
|
|
|
|
|
константа равновесия |
|
|||||
3/ 4 |
– 3 |
3 |
. |
(50) |
||
KФ(Ме) = PX2 |
(e ) |
Mei |
||||
43
www.mitht.ru/e-library
Тип «Шоттки»
В кристаллах типа «Шоттки» выполняется условие |
f |
f |
, поэтому |
HVX |
< HMei |
преобладает переход анионов из объема на поверхность с образованием в объеме кристалла вакансий аниона:
X22 |
|
X22 |
|
|
+ V2 |
; |
|
|
|
|
|
|||||||
X |
об |
|
X |
пов |
|
X |
|
|
|
|
|
|
||||||
суммарно с уравнением (45): |
|
|
|
|
|
|
||||||||||||
Me2 2 |
X22 |
+ |
X22 |
|
|
1 |
X20 ↑ + 2e– +VX2 , |
|||||||||||
|
||||||||||||||||||
|
|
Me |
X |
|
пов |
|
|
X |
об |
2 |
|
|
|
|||||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
0 |
1 |
X20 |
↑ + 2e– +VX2 ; |
|
|
|
|
(51) |
||||||||||
|
|
|
|
|
|
|||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
константа равновесия |
|
|
. |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
1/2 |
|
– 2 |
|
2 |
|
|
|
|
(52) |
|||
KШ(Ме) = PX2 |
|
(e ) |
VX |
|
|
|
|
|||||||||||
Для соединения Ме2Х3: |
|
|
|
|
|
|||||||||||||
2Me3 3 3X22 |
|
+ 3 X22 |
3 |
X20 ↑ + 6e– + 3VX2 , |
||||||||||||||
|
2 |
|||||||||||||||||
|
|
|
|
|
Me |
|
|
X |
пов |
|
X |
об |
|
|||||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
0 |
1 |
X20 |
↑ + 2e– +VX2 . |
|
|
|
|
(53) |
||||||||||
|
|
|
|
|
||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Поскольку одному точечному структурному дефекту – вакансии аниона соответствует один удаленный анион и один образовавшийся нейтральный атом металлоида, т. е. половина двухатомной молекулы, число молекул металлоида X02 ,
переходящих в газовую фазу, в уравнении процесса всегда равно 1/2 независимо от
формулы кристалла. Меняться могут только число электронов и величина заряда вакансии, равные заряду аниона.
Уравнения реакций (53) и (51) совпадают, поэтому выражение константы равновесия не будет отличаться от (52). При величине заряда аниона,
отличающейся от 2, в уравнении (53) изменится число электронов и соответственно в выражении константы равновесия степень при равновесной концентрации электронов (и, конечно, величина заряда вакансии аниона).
44
www.mitht.ru/e-library

3.2.3. Механизм и равновесие возникновения избытка
металлоида (недостатка металла)
Избыток металлоида возникает в результате его перехода из газовой фазы в
кристалл с образованием из молекул Х2 анионов Х2–, для чего требуется
присоединение к каждому атому металлоида 2 электронов. Протекающий процесс
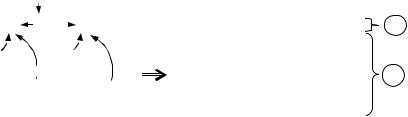
состоит из трех последовательных стадий (рис. 15, а):
1) молекула Х2 , находящаяся в газовой фазе, подходит к поверхности
кристалла и адсорбируется на ней:
X02 газ X02 адс.
2) молекула X02 адс в адсорбционном слое диссоциирует на атомы X0адс :
X02 адс 2X0адс ;
3) атомы металлоида, находящиеся в адсорбционном слое на поверхности кристалла, превращаются в анионы, присоединяя электроны, которые до этого
находились в нормальном положении в валентной зоне (на заполненных р-
орбиталях ионов); уход электронов из валентной зоны приводит к возникновению равного числа дырок. Образовавшиеся анионы занимают положения,
соответствующие анионным узлам новой кристаллографической плоскости,
расположенной над поверхностью кристалла: |
|
2Xадс0 + 4eе 2X2X2 пов + 4е+. |
|
Суммарное уравнение процесса имеет вид |
|
X20 ↓ + 4eе 2X2X2 пов + 4e+ |
|
или на 1 анион |
|
1 X20 ↓ + 2eе X2X2 пов + 2e+. |
(54) |
2 |
|
Вэтих уравнениях стрелка, направленная вниз, символизирует переход металлоида в кристалл из находящейся над ним газовой фазы.
Врезультате появления анионов в новой поверхностной плоскости
кристаллической решетки и отсутствия в ней катионов эта плоскость имеет некомпенсированный отрицательный заряд, а объем кристалла в результате ухода
из него электронов и соответственно образования дырок – избыточный положительный заряд (рис. 15, б).
45
www.mitht.ru/e-library
X02 газ
|
Xадс0 |
X20 адс Xадс0 |
|
|
Х2- |
|
Х2- |
|
– |
|
Х2- |
e |
e |
e |
e |
Х2- |
Ме2+ |
Х2- |
Ме2+ |
Х2- |
|
Ме2+ |
Х2- |
Ме2+ |
Х2- |
|
||||||
Ме2+ |
Х2- |
e |
Х2- |
Ме2+ |
e+ |
Х2- |
Ме2+ |
Х2- |
e+ |
+ |
Ме2+ |
Ме2+ |
Ме2+ |
|
|||||||
|
|
|
|
|
|
e+ |
|
e+ |
|
|
Х2- |
Ме2+ |
Х2- Ме2+ |
Х2- |
Х2- |
Ме2+ |
Х2- Ме2+ |
Х2- |
|
||
|
|
а |
|
|
|
|
б |
|
|
|
Рис. 15. Возникновение избытка металлоида: процессы, протекающие при переходе металлоида из газовой фазы на поверхность кристалла (а) и состояние кристалла
после образования новых анионных узлов (б)
Возникшее электростатическое поле стремится переместить анионы с поверхности в объем (в этом случае в объеме появились бы межузельные анионы
Xi2 ), а катионы из объема на поверхность (с возникновением в объеме вакансий
катионов VМе2 ); пока электростатическое поле существует, состояние кристалла
остается неравновесным. Переход анионов в междоузлия возможен только в
кристаллах с крайне редко встречающимся типом разупорядоченности «анти-
Френкель» и гипотетическим типом «анти-Шоттки», поэтому в реальных кристаллах
(типы разупорядоченности «Френкель» и «Шоттки») возможен только переход
катионов из объема на поверхность с возникновением вакансий катионов:
Me2 |
2 |
|
Me2 |
2 |
+ V2 . |
|
|
|
||
|
|
Me |
об |
|
Me |
пов Me |
|
|
|
|
Суммируя с уравнением (54), получаем |
|
|||||||||
|
1 |
X20 ↓ + 2eе |
+ Me2 |
2 |
Me2 |
2 X22 |
+ 2e+ + VMe2 , |
|||
|
|
|||||||||
2 |
|
|
|
Me |
об |
Me |
X |
пов |
|
|
|
|
|
|
|
|
|
|
|
||
или, после исключения нормальных элементов структуры,
1 |
X20 ↓ 2e+ + VMe2 . |
(55) |
|
2 |
|||
|
|
Выражение константы равновесия для типов разупорядоченности «Френкель»
и «Шоттки» одно и тоже:
KФ(Х) = KШ(Х) = |
(e )2 |
V2 |
. |
(56) |
||
|
Me |
|
||||
P1/2 |
||||||
|
|
|
||||
|
X2 |
|
|
|||
46
www.mitht.ru/e-library
Описание процесса и выражение константы равновесия для соединения
Ме2Х3 2Ме3+·3Х2-:
- уравнение обратимого процесса перехода металлоида из газовой фазы и катионов из объема кристалла на его поверхность в расчете на число образующихся анионов, равное их числу в формуле соединения:
3 |
X02 |
↓ + 6eе +2 Me3 |
3 |
2Me3 |
3 3X22 |
+ 6e+ + 2VMe3 , |
|
|
|||||||
2 |
|
Me |
об |
Me |
X |
пов |
|
|
|
|
|
|
|
|
|
или, после пересчета на 1 точечный структурный дефект и удаления нормальных структурных элементов,
|
3 |
X20 ↓ 3e+ + VMe3 ; |
|
|
|
|
(57) |
||
4 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||
константа равновесия |
|
|
|
|
|
||||
|
|
|
(e )3 VMe3 |
+ 3 |
3 |
3/ 4 |
|
|
|
KФ(Х) = KШ(Х) = |
|
(е ) |
VMe |
PX2 |
. |
(58) |
|||
P3/ 4 |
|
||||||||
|
|
|
X2 |
|
|
|
|
|
|
47
www.mitht.ru/e-library

4.ЗАВИСИМОСТИ КОНЦЕНТРАЦИЙ ДЕФЕКТОВ ОТ ДАВЛЕНИЯ МЕТАЛЛОИДА В ГАЗОВОЙ ФАЗЕ
4.1. ОБЩИЕ ПОЛОЖЕНИЯ
Как было показано в разделе 3.2.1, при P |
= P0 кристалл стехиометрический, |
X2 |
X2 |
в нем присутствуют только тепловые дефекты, и их концентрации выражаются через
соответствующие константы равновесия типа произведений растворимости (KФ, KШ
и Kи).
Если же P ≠ |
P0 , то, кроме тепловых дефектов, в кристалле присутствуют |
|
X2 |
X2 |
|
также дефекты нестехиометрии, и чем значительнее отклонение P от |
P0 , тем |
|
|
X2 |
X2 |
заметнее состав кристалла отличается от стехиометрического и тем выше
концентрация дефектов нестехиометрии. Это легко показать и качественно, и
количественно; |
в |
качестве |
объекта |
используем |
кристалл |
|
Ме2Х3 2Ме3+·3Х2-. |
|
|
|
|
|
|
При P |
<P0 |
состав |
кристалла |
характеризуется |
недостатком |
металлоида |
X2 |
X2 |
|
|
|
|
|
(избытком металла), возникающим в результате ухода некоторого количества
металлоида в газовую фазу. Соответствующие процессы описываются уравнениями
реакций
2Me3 |
3 3X22 |
|
3 |
X20 ↑ + 6e– + 2Mei3 , |
||
2 |
||||||
Me |
X |
пов |
|
|
||
0 3 X02 ↑ + 3e– + Me3i
4
для типа «Френкель» и
2Me3 |
3 3X22 |
+ 3 |
X22 |
|
3 |
X20 ↑ + 6e– + 3VX2 , |
|||
2 |
|||||||||
Me |
X |
пов |
|
X |
об |
|
|
||
0 1 X02 ↑ + 2e– +VX2
2
для типа «Шоттки».
Совместное рассмотрение этих уравнений позволяет сформулировать важные
выводы:
1. Независимо от типа разупорядоченности, избытку металла (недостатку
металлоида) отвечает появление в кристаллической решетке электронов
48
www.mitht.ru/e-library
проводимости, оставляемых анионами при превращении их в нейтральные атомы и затем в молекулы Х2.
2. Вид точечных структурных дефектов, возникающих при уходе металлоида в
газовую фазу, определяется типом разупорядоченности: в кристаллах типа
«Френкель» это катионы в междоузлиях, в кристаллах типа «Шоттки» – вакансии
анионов. Оба вида дефектов характерны именно для избытка металла (недостатка металлоида): катионы в междоузлиях – это «лишние», избыточные катионы, а
вакансии аниона – это недостающие анионы.
3. Концентрации дефектов, характерных для избытка металла (недостатка металлоида), растут при понижении давления металлоида PX2 . Это подсказывает здравый смысл: уходу летучего вещества (в данном случае металлоида) из конденсированной фазы в газовую (т. е. протеканию процесса, подобного
испарению) способствует пониженное давление этого вещества в газовой фазе.
Качественно это же следует из принципа Ле-Шателье: поскольку одним из продуктов реакции является газообразное вещество, понижение давления смещает
равновесие реакции вправо, т. е. в сторону увеличения концентраций электронов
проводимости и точечных структурных дефектов. И, наконец, к тому же выводу
приводят количественные соотношения: из уравнений (50) и (52) следует
– 3 |
3 |
|
3/4 |
, |
(59) |
|
(e ) |
Mei |
|
= KФ(Ме) PX2 |
|||
(e–)2 |
V2 |
|
= K |
P 1/2 , |
|
(60) |
|
X |
|
Ш(Ме) |
X2 |
|
|
т. е. произведение концентраций электронов проводимости и точечных структурных
дефектов и соответственно каждая из этих концентраций растут при уменьшении
PX2 , о чем свидетельствует отрицательная степень давления в правой части уравнения.
Увеличение концентраций электронов проводимости, катионов в междоузлиях или вакансий анионов сопровождается уменьшением концентраций дырок и вакансий катионов. Это непосредственно следует из уравнений констант равновесия тепловой разупорядоченности (36), (32) и (34):
(е ) = Kи/(е );
VMe3- = KФ/ Me3i ;
VMe3 = KШ/ VX2 3 1/2 .
При PX2 >PX2 кристалл содержит избыток металлоида (недостаток металла),
возникающий в результате перехода некоторого количества металлоида из газовой
49
www.mitht.ru/e-library

фазы в кристалл с образованием из молекул Х2 анионов. Протекающий процесс описывается для кристаллов типа «Френкель» и типа «Шоттки» одним и тем же
уравнением квазихимической реакции
3 |
X02 |
↓ + 6eе +2 Me3 |
3 |
2Me3 |
3 3X22 |
+ 6e+ + 2VMe3 , |
|
|
|||||||
2 |
|
Me |
об |
Me |
X |
пов |
|
|
|
|
|
|
|
|
|
3 X02 ↓ 3e+ + VMe3
4
и соответственно с одинаковым для обоих типов выражением константы равновесия:
|
|
|
(e )3 VMe3 |
+ 3 |
3 |
3/ 4 |
|
||
KФ(Х) = KШ(Х) = |
|
|
(е ) |
VMe |
PX2 |
, |
|||
|
P3/ 4 |
|
|||||||
|
|
|
|
X2 |
|
|
|
|
|
из которого следует |
|
|
|
|
|
|
|
||
+ 3 |
3 |
= KФ(Х) |
3/4 |
|
|
|
|
(61) |
|
(е ) |
VMe |
PX2 |
|
|
|
||||
или |
V3 |
= K |
|
|
|
|
|
|
|
(е+)3 |
|
P3/4 . |
|
|
|
(62) |
|||
|
Me |
Ш(Х) |
X2 |
|
|
|
|
||
Анализ этих уравнений позволяет сформулировать важные выводы:
1.Избытку металлоида (недостатку металла) всегда отвечает присутствие в кристаллической решетке дырок, возникших в процессе превращения молекул Х2 в
нейтральные атомы и затем в анионы.
2.Независимо от того, относится данный кристалл к типу «Френкель» или типу
«Шоттки», при избытке металлоида (недостатке металла) он содержит нестехиометрические вакансии катионов, возникшие в результате перехода катионов из объема в катионные узлы новой плоскости, анионные узлы которой заняты анионами, образовавшимися из нейтральных молекул Х2. Этот вид дефектов
характерен именно для недостатка металла (избытка металлоида): вакансии
катиона – это недостающие катионы.
3. Концентрации дефектов, характерных для избытка металлоида (недостатка металла), растут при повышении давления металлоида PX2 . Это соответствует
здравому смыслу: переходу летучего вещества (в данном случае металлоида) из
газовой фазы в твердую (т. е. протеканию процесса, подобного конденсации)
способствует повышенное давление этого вещества в газовой фазе. Это же следует из принципа Ле-Шателье: поскольку газообразное вещество является исходным реагентом, равновесие реакции смещается вправо, т. е. в сторону увеличения концентраций дырок и вакансий катионов, при увеличении давления. И, наконец, к
50
www.mitht.ru/e-library
