
0250 / Педиатрия_Майданник
.pdfявляется количественное определение антитриптической активности сыворотки, для чего используется метод В.А. Шатерникова (норма 300— 500 ед.). Концентрацию собственно А1-АТ измеряют методом встречной иммунодиффузии или другими иммунохимическими методами. Генетическое титрование проводится методом перекрестного электрофореза в кислом крахмальном геле.
Дифференциальный диагноз проводят с бронхиальной астмой, эмфиземой, обусловленными пороками развития (дефицит хрящей бронхов, бронхиолоэктатическая эмфизема).
ЛЕЧЕНИЕ. В связи с отягощающим действием раздражающих ингалянтов следует полностью оградить больного от табачного и иного дыма, вплоть до смены жительства. Любые проявления бактериального процесса должны подавляться антибактериальными средствами. Постуральный дренаж и вибромассаж показаны больным с признаками хронического бронхита. При выраженной гипоксии применяется кислородотерапия, спазмолитики назначают при спастическом компоненте.
Некоторые авторы отмечают некоторое улучшение после применения глюкокортикоидов и ингибиторов протеаз (трасилол и др.).
Что касается специфической терапии, при поражении легких назначают заместительную терапию синтетическим ферментом или А1АТ, выделенным из плазмы. Однако вследствие короткого периода полувыведения заместительная терапия альфа-1-фракцией глобулинов неэффективна. Ведется разработка синтетических антиэластаз, а также методов мобилизации накопляемого в гепатоцитах антитрипсина.
Недостаточность А1-АТ — второе по частоте заболевание в детском возрасте, при котором выполняют трансплантацию печени. Выживаемость и осложнения после трансплантации аналогичны таковым при других заболеваниях.
По мере уточнения молекулярных механизмов повреждения гепатоцитов могут появиться новые подходы к лечению, например применение пептидов, предотвращающих ZZ-полимеризацию путем заполнения щели в А-складке; пока эти подходы носят лишь предположительный характер.
ПРОГНОЗ. Выявление ребенка с дефицитом А1-АТ становится поводом для обследования родственников и проведения профилактических мероприятий. Всем выявленным гетерозиготам следует запретить курение, использование протеолитических ферментов. Необходима соответствующая профориентация: исключаются специальности, связанные с ингаляционным воздействием (шахты, горячие металлургические цехи, цементное производство и др.). Вакцинация против кори, гриппа обязательна. ОРЗ у этих лиц должны лечиться особенно энергично.
Г л а в а 3
ЗАБОЛЕВАНИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА
Врожденный порок сердца — это патологическое состояние, характеризующееся аномалиями развития сердца и магистральных сосудов, возникшее вследствие нарушения эмбриогенеза в период 2—8-й недель беременности под влиянием неблагоприятных факторов внешней (вирусы, токсические вещества и др.) и внутренней (продукты измененного обмена веществ и др.) среды на фоне наследственной (полигенной) предрасположенности.
Врожденные пороки сердца представляют сложную проблему современной клинической педиатрии как в медицинском, так и в социальном плане. Это связано, прежде всего, с тем, что распространенность врожденных пороков сердца достаточно высока и составляет среди новорожденных в разных странах мира 0,8—1%. Причем врожденные пороки сердца составляют 30% от числа всех врожденных пороков развития. Для детей с врожденными пороками сердца характерна высокая летальность: от 55 до 70% детей с врожденными пороками сердца без хирургической коррекции не доживают до ) года.
Врожденные пороки сердца отличаются сложностью диагностики, особенно в первые месяцы жизни ребенка. В частности, при рождении врожденные пороки сердца диагностируются только у 47% детей, а в течение первого года жизни — у 93%.
ЭТИОЛОГИЯ. Врожденные пороки сердца формируются в результате нарушения эмбриогенеза в период 2—8-й недели беременности. Среди причин врожденных пороков сердца можно выделить следующие:
1) хромосомные нарушения — 5%; 2) мутация одного гена — 2—3%;
3)факторы среды (алкоголизм родителей, краснуха, медикаменты и др.) — 1—2%; 4) полигенно-мультифакториальное наследование — 90%.
Врожденные пороки сердца, в частности, дефекты межжелудочковой и межпредсердной перегородок и др., наиболее часто возникают при хромосомных аберрациях, связанных с трисомией по 21, 18 и 13-й парам хромосом (табл. 25). При аномалиях половых хромосом врожденные пороки сердца бывают значительно реже. При этом пороки сердца, которые ассоциируются с хромосомными аномалиями, всегда являются частью синдрома полисистемных пороков развития, а не изолированными дефектами.
162
Таблица 25
Врожденные пороки сердца у детей с хромосомными аберрациями
Заболевания |
Частота, % |
Врожденные пороки сердца |
|
|
|
5p-(Chi du Chat syndrome) |
25 |
ДМЖП, ОАП, ДМПП |
Трисомия D (13) |
90 |
ДМЖП, ОАП, декстрокардия |
Трисомия Е (18) |
99 |
ДМЖП, ОАП, СЛА |
Трисомия 21 (болезнь Дауна) |
50 |
ДМЖП |
Turner's syndrome (XO) |
35 |
КА, АС, ДМПП |
Синдром Клайнфельтера (XXXY) |
15 |
ОАП, ДМПП |
|
|
|
Примечание. ДМЖП — дефект межжелудочковой перегородки; ОАП — открытый артериальный проток; ДМПП — дефект межпредсердной перегородки; АС — стеноз аорты; КА — коарктация аорты;
СЛА — стеноз легочной артерии
При мутации единичных генов врожденные пороки сердца сочетаются с аномалиями развития других органов. Пороки развития сердеч- но-сосудистой системы являются частью синдрома с аутосомно-доми- нантным (синдромы Холта-Орама, Нунана, Крузона, Марфана и др.), аутосомно-рецессивным (синдромы Гурлера, Картагенера и др.) типами наследования.
Наряду с этим имеет значение наследственная (полигенно-мулти- факториальная) предрасположенность, для некоторых врожденных пороков сердца характерна генетическая основа.
К повреждающим факторам внешней среды, которые могут приводить к формированию врожденных пороков сердца, относят воздействие рентгеновского и ионизирующего излучения некоторых лекарственных препаратов (амфетамины, противосудорожные препараты, триметадион, литий и др.), инфекционных и вирусных агентов (краснуха и др.), алкоголя и др.
Кроме указанных этиологических факторов, выделяют факторы риска рождения ребенка с врожденным пороком сердца, которыми являются возраст матери, эндокринные нарушения, токсикоз в 1 триместре и угроза прерывания беременности, мертворождение в анамнезе, наличие в семье других детей с врожденными пороками развития и др.
При семейных формах врожденных пороков сердца и сочетании их с хромосомными болезнями обязательно обследование ребенка и родственников в медико-генетическом центре. При этом с целью пренатальной диагностики используют амниоцентез.
При медико-генетическом консультировании по поводу хромосомных аномалий, ассоциирующихся с врожденными пороками сердца, необходимо учитывать, что если у пробанда диагностирована трисомия, то риск развития врожденного порока сердца у ребенка равен 1%, а при наличии у родителя сбалансированной транслокации — 2—10%.
163
При медико-генетическом консультировании по поводу менделирующих нарушений супружескими парами, относящимися к группе риска, необходимо сообщить об относительно высокой вероятности наследования мутантного гена: 50% для аутосомно-доминантных нарушений (наличие врожденного порока сердца у родственников I степени — родители, братья, сестры) и 25% для аутосомно-рецессивных (врожденный порок сердца у родственников II степени — дедушки, бабушки, дяди и тети), при наличии врожденного порока сердца у родственников III степени (двоюродные братья и сестры) вероятность составляет 13%.
В случаях мультифакторных врожденных пороков сердца возможность рождения здорового ребенка в семье, в которой уже есть ребенок с врожденным пороком сердца, составляет 97%. При медико-генетиче- ском консультировании необходимо учитывать риск возникновения врожденного порока сердца у сибса: при тетраде Фалло он составляет 2,5%, при транспозиции магистральных сосудов — 2%, при общем артериальном стволе — 1%, при дефекте межжелудочковой перегородки — 3%, при коарктации аорты — 2%. При этом риск развития патологии выше, если порок у матери, а не у отца.
Клиническая симптоматика и патофизиология гемодинамики порока зависят от имеющихся анатомических нарушений, которые определяются сообщениями между правыми и левыми камерами сердца или магистральными сосудами, а также величиной давления в камерах сердца и магистральных сосудах (табл. 26).
Таблица 26
Давление в полостях сердца и крупных сосудах у детей
|
Давление , мм рт. ст. |
|
|
|
|
|
Систолическое |
Диастолическое |
|
|
|
Правое предсердие |
2 - 3 |
- 2 — + 2 |
Правый желудочек |
30 |
3 - 5 |
Легочная артерия |
30 |
10 |
Левое предсердие |
8 |
5 |
Левый желудочек |
100 |
8—10 |
Аорта |
100 |
60 |
|
|
|
КЛАССИФИКАЦИЯ. Поскольку в настоящее время известно более 200 разновидностей врожденных пороков, то создание единой их классификации имеет определенные трудности. Однако более 80% всех врожденных пороков сердца составляют 8 пороков: дефект межжелудочковой перегородки, дефект межпредсердной перегородки, открытый артериальный проток, коарктация аорты, стеноз аорты, транспозиция магистральных сосудов, стеноз легочной артерии и болезнь Фалло. Данные о частоте встречаемости врожденных пороков сердца в разных возрастных группах представлены в таблице 27.
164
Таблица 27
Частота встречаемости (%) врожденных пороков сердца в разных возрастных группах
|
Дети |
Дети |
Дети старших |
Вид порока |
грудного |
старшего |
возрастных |
|
возраста |
возраста |
групп |
|
|
|
|
Дефект межжелудочковой |
25 |
24 |
15 |
перегородки |
|
|
|
Дефект межпредсердной |
10 |
12 |
15 |
перегородки |
|
|
|
Открытый артериальный проток |
12 |
15 |
15 |
Тетрада Фалло |
7 |
10 |
15 |
Транспозиция магистральных |
8 |
3 |
2 |
сосудов |
|
|
|
Атрезия правого атриовентрику- |
1 |
1,5 |
1 |
лярного клапана |
|
|
|
Стеноз легочной артерии |
6 |
10 |
15 |
Стеноз аорты |
3 |
6 |
5 |
Коарктация аорты |
9 |
4 |
8 |
Другие |
12 |
10 |
7 |
|
|
|
|
В настоящее время в клинической практике наиболее часто используют классификацию, предложенную B.C. Morgan в 1978 году. В основу данной классификации положен патофизиологический принцип с разделением врожденных пороков сердца по нарушению гемодинамики в большом и малом круге кровообращения, а также возможность клинического распознавания врожденных пороков сердца на основании доступных клинических и инструментальных методов исследования.
Первоначально врач определяет наличие цианоза при осмотре больного в состоянии покоя или при физической нагрузке (плач, физическая нагрузка). Далее уточняется состояние малого круга кровообращения (гипоили гиперволемия) с помощью аускультации (характер II тона над легочной артерией) и рентгенографии сердца. Эти данные сопоставляются с результатами электрокардиографического исследования, что позволяет уточнить характер гипертрофии и перегрузки камер сердца.
Классификация врожденных пороков сердца у детей представлена в таблице 28.
КЛИНИЧЕСКАЯ КАРТИНА. Клиника врожденных пороков сердца весьма многогранна и определяется тремя основными факторами: анатомическими особенностями порока, степенью компенсации и возникающими осложнениями порока. Существует определенная периодичность в течении врожденных пороков сердца, что позволяет выделить три фазы.
Первая фаза (первичной адаптации) характеризуется приспособлением организма ребенка к нарушениям гемодинамики, вызванным по-
165
Таблица 28
Классификация врожденных пороков сердца у детей
Нарушение
гемодинамики
Собогащением малого круга кровообращения
Собеднением малого круга кровообращения
Собеднением большого круга кровообращения
Без нарушений гемодинамики
Без цианоза |
С цианозом |
Открытый артериальный |
Комплекс Эйзенменгера, |
проток, дефекты межпред- |
транспозиции магист- |
сердной и межжелудочко- |
ральных сосудов, общий |
вой перегородок, атриовен- |
артериальный ствол |
трикулярная коммуникация |
|
Изолированный стеноз |
Болезнь Фалло, атрезия |
легочной артерии |
трехстворчатого клапана, |
|
транспозиция магист- |
|
ральных сосудов со сте- |
|
нозом легочной артерии, |
|
общий ложный артери- |
|
альный ствол, болезнь |
|
Эбштейна |
Изолированный аортальный |
|
стеноз |
|
Коарктация аорты |
|
Истинная и ложная декстрокардия, аномалии положения дуги аорты и ее ветвей, небольшой дефект межжелудочковой перегородки (в мышечной части)
роком. Эта фаза определяется временем приспособления сердечно-со- судистой системы и организма в целом к условиям неадекватной гемодинамики. Реакции адаптации и компенсации у ребенка раннего возраста находятся в состоянии неустойчивого равновесия или относительной слабости. Сердечная деятельность в этой фазе характеризуется неустойчивым равновесием, и на фоне нарастающих физических нагрузок в процессе роста ребенка или интеркуррентных заболеваний легко развивается недостаточность (декомпенсация) кровообращения. При небольших нарушениях гемодинамики клинические проявления болезни могут быть мало выражены. При значительных нарушениях гемодинамики возникает нестойкая гиперфункция миокарда, поэтому легко развивается декомпенсация. В раннем возрасте сравнительно несложный анатомический порок (открытый артериальный проток, дефекты перегородок сердца и др.) может протекать очень тяжело и привести к смерти больного. Продолжается фаза адаптации при неосложненном течении 2—3 месяца, при наличии осложнений — до 1,5—2 лет.
Если дети с врожденным пороком сердца не гибнут в первой фазе болезни, то обычно после 2—3 лет жизни наступает значительное улучшение их состояния и развития. Это улучшение связано с компенсацией организмом ребенка вызванных пороками нарушений гемодинамики
166
и газообмена. Наступает вторая фаза — фаза относительной компенсации. Она наступает в связи с включением всех компенсаторных механизмов организма, в том числе и гипертрофии миокарда. В этот период наблюдается устойчивость сердечной деятельности, субъективные жалобы уменьшаются или отсутствуют, несмотря на тяжелое заболевание, улучшается физическое развитие и моторная активность больного, отмечается резистентность к инфекциям. Продолжительность фазы относительной компенсации — от нескольких месяцев до 20—30 лет.
Вслед за второй фазой, независимо от ее длительности, неизбежно развивается третья фаза течения порока — терминальная. Она обусловлена появлением выраженных дистрофических изменений в миокарде и наступает при исчерпании компенсаторных возможностей. В этой фазе развивается хроническая (поздняя, вторичная) сердечная недостаточность кровообращения. Развитие сопутствующих заболеваний и осложнений способствуют возникновению этой фазы болезни, которая неизбежно заканчивается смертью больного. Успехи кардиоревматологии и кардиохирургии обусловили значительное уменьшение числа больных детей в данной фазе течения.
Этим можно объяснить разнообразие в лечении одного и того же анатомического порока, когда наблюдается то тяжелое течение с ранними осложнениями и даже смертью ребенка, то более мягкое течение, когда порок длительное время не диагностируется и даже при распознавании не вызывает большой тревоги у родителей и врачей, пока нарушение сердечной деятельности или тяжелые осложнения не приводят к развитию угрожающего состояния. Поэтому даже точное распознавание формы порока еще не определяет прогноз.
Особенности клинического течения фаз врожденных пороков сердца нашли патофизиологическое объяснение в работах Ф.З. Меерсона и соавторов о компенсаторной гиперфункции, гипертрофии и недостаточности сердца. Авторы выделили три стадии компенсаторной гиперфункции сердца. Первая, аварийная, стадия развивается непосредственно после возникновения порока и характеризуется увеличением интенсивности функционирования структур миокарда. Эта стадия процесса нередко сопровождается признаками острой сердечной недостаточности: снижением максимальной силы и скорости сокращения миокарда, развитием отеков и асцита. Увеличивается интенсивность функционирования структур миокарда, что вызывает изменения обмена и гипертрофию.
При второй стадии завершающейся гипертрофии и относительно устойчивой гиперфункции отмечается нормальная интенсивность функционирования структур миокарда. Гиперфункция относительно устойчива, но исподволь развиваются в данной стадии нарушения обмена, структуры и регуляции сердца.
Третья стадия прогрессирующего кардиосклероза и постепенного истощения проявляется снижением интенсивности синтеза нуклеиновых кислот и белков в гипертрофированном миокарде. Наряду с изнашиванием сердца, по-видимому, прогрессирует изнашивание и его регулирующих механизмов.
167
ДИАГНОСТИКА. Клиническая диагностика врожденного порока сердца имеет следующие этапы: L) подверждение наличия врожденного порока сердца у ребенка; 2) определение основных гемодинамических нарушений, вызванных пороком, т.е. распознавание синдромной принадлежности порока; 3) уточнение анатомического варианта порока; 4) выяснение функционального диагноза, т.е. уточнение фазы течения порока; 5) выявление имеющихся осложнений.
Цианоз при врожденных пороках сердца наблюдается в случае увеличения количества восстановленного гемоглобина эритроцитов до 50 г/л. На увеличение содержания восстановленного гемоглобина влияют следующие факторы: 1) степень использования кровью кислорода в легких (последнее имеет значение при возникновении препятствия току крови, например, при стенозе легочной артерии либо при развитии склероза сосудов малого круга); 2) увеличение количества венозной крови, поступающей в большой круг кровообращения при наличии сброса крови из правых отделов сердца в левые; 3) степень использования кислорода тканями.
Развитие цианоза, как правило, сопровождается изменениями периферической крови — полицитемией и гипергемоглобинемией. Хроническая кислородная недостаточность приводит к изменению ногтевых фаланг — они приобретают форму «барабанных палочек».
При подозрении на врожденный порок сердца необходимо сопоставление клинических признаков с АД (измеренным на руках и ногах), дополнительное проведение рентгенологического исследования, регистрация ЭКГ и клинического анализа крови, что позволяет в 90% случаев распознать анатомический вариант порока без применения специальных методов исследования — ангиокардиографии, зондирования сердца и т.д. Значительно помогает в уточнении анатомического диагноза врожденного порока сердца эхокардиография.
ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА С ОБОГАЩЕНИЕМ МАЛОГО КРУГА КРОВООБРАЩЕНИЯ
Для данной группы пороков характерны сходные нарушения гемодинамики, когда в малый круг кровообращения поступает больше крови, чем в большой. Клинические особенности при этих нарушениях гемодинамики определяются развитием гиперволемии в малом круге кровообращения и ранней сердечной недостаточностью, склонностью к затяжным и повторным пневмониям или респираторным инфекциям.
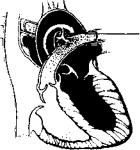
ОТКРЫТЫЙ АРТЕРИАЛЬНЫЙ ПРОТОК. Это врожденный порок сердца, обусловленный функционированием артериального (боталлова) протока, который соединяет начальную часть нисходящей дуги аорты с легочной артерией в области ее бифуркации, по истечении срока его закрытия (рис. 16).
У большинства новорожденных артериальный проток прекращает функционирование в первые часы или дни после рождения. Анатоми-
168
ческая облитерация артериального протока заканчивается к 6—8-й неделе внеутробной жизни ребенка.
Открытый артериальный проток считается врожденным пороком сердца, если он продолжает функционировать более 3—4 недель после рождения ребенка.
Открытый артериальный проток является одним из наиболее распространенных пороков: по клиническим данным, его частота составляет 10—18%-всех врожденных пороков сердца. Причем частота встречаемости открытого артери-
ального протока у новорожденных имеет прямую зависимость от массы тела при рождении и наличия синдрома дыхательных расстройств.
ГЕМОДИНАМИКА. Гемодинамические нарушения заключаются в сбросе крови из аорты в легочную артерию. Это происходит как во время систолы, так и диастолы, поскольку давление в аорте значительно выше (100/60 мм рт. ст.), чем в легочной артерии (30/10 мм рт. ст.), в обеих фазах сердечного цикла. Исключение составляют дети первых месяцев жизни, у которых отсутствует диастолический градиент давления, и поэтому сброс происходит только в систолу. Это приводит к переполнению малого круга кровообращения и перегрузке левых камер сердца, которые расширяются, а стенки гипертрофируются.
В результате переполнения малого круга кровообращения, а также передачи давления из аорты через проток развивается легочная гипертензия. При этом наблюдается перегрузка правого желудочка. В большой круг кровообращения поступает уменьшенное количество крови.
Если сопротивление в малом круге кровообращения превышает таковое в большом, то возникает обратный веноартериальный сброс и появляется цианоз.
КЛИНИКА И ДИАГНОСТИКА. У большинства детей при небольших и средних размерах открытого артериального протока клинические проявления заболевания выявляются в конце первого года или на 2— 3-м году жизни. Обычно эти дети до появления клинических симптомов порока хорошо развиваются физически и психомоторно.
При осмотре выявляется бледность кожных покровов, выражена пульсация сосудов шеи, особенно при большом объеме шунта. Может наблюдаться цианоз нижней половины тела при крике, натуживании, исчезающий тотчас после прекращения нагрузки. При высокой легочной гипертензии и веноартериальном сбросе крови (из легочной артерии в аорту) может наблюдаться стойкий цианоз кожи и слизистых оболочек. Деформация грудной клетки наблюдается редко, но постепенно может формироваться парастернальный «сердечный горб».
169
Пальпаторно ощущается усиление верхушечного толчка, который смещен влево и книзу. Он разлитой и приподнимающийся. Определяется систолодиастолическое дрожание, максимально выраженное во II межреберье слева у грудины. Систолическое дрожание отсутствует у больных с небольшим протоком или при развитии высокой легочной гипертензии. Для открытого артериального протока характерен высокий и быстрый пульс. Систолическое АД несколько повышено, а диастолическое АД резко снижено (до 30—40 мм рт. ст.). При этом увеличивается пульсовое давление.
С помощью перкуссии выявляется смещение границ относительной тупости сердца влево, которое происходит в результате гипертрофии левых отделов сердца.
При аускультации для больных с открытым артериальным протоком типичным является грубый систолодиастолический шум, который описывают как «машинный шум» (или «шум мельничного колеса», или шум «раската грома»). Punctum maximum этого шума находится во II межреберье слева у грудины. Шум проводится в левую подключичную область и на спину (в межлопаточное пространство). При задержке дыхания он ослабевает, а при глубоком вдохе усиливается.
По мере развития легочной гипертензии диастолический компонент шума уменьшается, а затем вовсе исчезает. Это указывает на развитие легочной гипертензии, когда выравнивается давление в большом и малом круге кровообращения. Затем одновременно с появлением одышки и цианоза вновь возникает систолический шум над областью легочной артерии, свидетельствующий об изменении направления или возникновении венозно-артериального шунта крови. Ослабление шума при открытом артериальном протоке является угрожающим симптомом, свидетельствующим о приближении терминальной фазы порока.
Для аускультативной картины открытого артериального протока типичным является резко усиленный II тон над легочной артерией за счет закрытия пульмонального клапана, что указывает на наличие легочной гипертензии.
При больших размерах протока (относительно диаметра аорты) клиническая картина характерна уже с первых дней жизни и проявляется признаками сердечной недостаточности (одышка, тахикардия, гепатоспленомегалия), отставанием в физическом и моторном развитии, снижением толерантности к физической нагрузке (при кормлении, ходьбе, беге). При этом на верхушке выслушивается грубый среднедиастолический шум.
Для подтверждения диагноза открытого артериального протока используют ЭКГ, ФКГ, ЭхоКГ и рентгенографию.
На ЭКГ электрическая ось сердца расположена нормально или отклонена влево. Имеют место признаки гипертрофии левого желудочка, из которых самым ранним является увеличение амплитуды зубца R и появление зубца Q в отведениях V5-V6. Признаки гипертрофии левого предсердия появляются при большом диаметре протока. Отклонение электрической оси вправо и признаки гипертрофии обоих желудочков или правого желудочка возникают при развитии легочной гипертензии. Систолический показатель часто увеличен.
170
