
3 курс / Патологическая физиология / Патофизиология_крови,_Фред_Дж_Шиффман
.pdf
358 |
Глава 9. Злокачественные опухоли кроветворной |
ани | |
||
ткани |
|
|
|
|
|
|
|
|
|
нительно необходимо КТ-сканирование живота и таза для определения степени увеличения лимфатических узлов в этих областях. Вопрос 2. При рентгеновском исследовании грудной клетки и КТ обнаружено образование приблизительно 3 см в диаметре в области корня левого легкого. Стандартныйанализкрови, мочииКТ-обследованиеживотаитаза не выявили никаких аномалий. Нужно ли начинать лечение этого пациента?
Ответ. Из-за возможности распространения палогического процесса ниже диафрагмы, особенно на селезенку (что бывает в 30 % случаев), многие рекомендовали бы проведение лапаротомии для выявления "скрытого" процесса в брюшной полости. Этот вид агрессивного обследования ("стадиро-вания") выполняют только при условии, что оно может изменить схему планируемой терапии, а терапия должна привести к изменениюрезультатов(обычными критериями эффективности являются общая выживаемость и излечение от болезни). Если стадирование не показало распространения болезни ниже диафрагмы, тогда можно проводить только лучевую терапию. При обнаружении лимфомы необходимо рассмотреть различные радиотерапевтические и/или химиотерапевтические подходы. Если из-за неполностью проведенного стадирования субдиафрагмальная лимфома была первоначально не выявленаивыбранаменееинтенсивнаясхематерапии, ещеневсепотеряно. Даже если произошел рецидив, можно "подкрепить" пациента дополнительной терапией и обеспечить ему долгосрочную выживаемость. Однако большинство специалистов предпочитают гипердиагностику и, соответственно, проведение максимально интенсивного лечения, которое минимизирует риск возникновения рецидива и осложнений.
У данного пациента при одном стандартном диагностическом вмешательстве необходимо выполнить лапаротомию и спленэктомию. Если никакого проявления ЛГМ ниже диафрагмы не будет найдено, следует назначить лучевую терапию на поверхностные (подкожные) и верхние парааорталь-ные лимфатические узлы. Продолжениенаблюдения При КТ брюшной полости и таза не выявлено признаков лимфаденопатии.
Сканирование галлием показало увеличенную активность в области средостения. Пациент получил вакцины против Haemophilus influenzae,
Streptococcuspneumoniae, Neisseria meningitidis. Затем была выполнена диаг-
ностическая лапаротомия и спленэктомия, при этом никаких признаков заболевания не найдено. Проведена лучевая терапия на поверхностные и па-рааортальные области. Пациент находится в состоянии ремиссии в течение 5 лет после курса лечения.
Хотя этот пациент, очевидно, был вылечен, в дальнейшем требуется всестороннее наблюдение для определения последствий болезни и лечения, которые могут развиваться спустя многие годы. К ним относят гипотиреоз или карциному щитовидной железы после лучевой терапии и постспленэкто-мический сепсис, вызванный инкапсулированными микроорганизмами, упомянутыми ранее (несмотря на иммунизации). Вызывать проблемы могуттакже другиебактерии, малярийныйплазмодий и бабезия. Кроме того, увеличивается вероятность развития вторичных новообразований, особен-

Лимфомы
35
9
новоблученных областях, через5, 10 и15 летпослелучевойтерапии. Молодые женщины особенно предрасположены к развитию рака молочной железы после облучения.
Клинический пример
77-летний мужчина пришел на прием из-за плохого анализа крови. Он хорошо себя чувствовал в последнее время, хотя 7 лет назад перенес аорто-коронарное шунтирование из-за стенокардии, резистентной к лекарственной терапии. В настоящее время принимает только блокатор кальциевых каналов и чувствует себя прекрасно. При ежегодном обследовании 2 недели назад у него обнаружено повышение СОЭ и содержания общего белка в плазме крови. Последующий электрофорез сывороточных белков показал моноклональный "пик" в области у-глобулинов при их концентрации 26 г/л (нормальное содержание у-глобулина — 7-17 г/л); уровень других иммуноглобулинов был в пределах нормы. Необходимо рассмотреть возможность диагноза множественной миеломы. Пациент встревожен, особенно потому, что от этой болезни недавно умер его друг, у которого были переломы костей, кровотечения и инфекции. При физикальном осмотре пациент выглядит здоровым, но испуганным. Каких-либо аномалий, кроме хорошо зажившего рубца от срединного разреза грудной клетки, не найдено.
Вопрос 1. Может ли у этого пациента быть множественная миелома? Ответ. Постановка диагноза множественной миеломы возможна только в том случае, если имеющиеся данные соответствуют нескольким критериям. У данного пациента, как мы надеемся, пик в у-области (моноклональная парапротеинемия) указывает на то, что он страдает только доброкачественной моноклональной гаммапатией (ДМГ), известной также как моноклональная гаммапатия неизвестного значения (МГНЗ). Дальнейшие действия должны быть направлены на классификацию его заболевания. Вопрос 2. Каковы следующие диагностические шаги? Ответ. Анализ крови, выполненный за 2 недели до осмотра, показал, что кроме высокого уровня белка все биохимические параметры сыворотки нормальны, включая уровень кальция. Это хорошо, потому что отсутствие анемии, азотемии или гиперкальциемии является благоприятным признаком для исключения множественной миеломы. Назначается анализ мочи с определением наличия легких цепей (белков Бенс-Джонса), даже если общий скрининговый тест определения белка в моче будет отрицательным. Легкие цепи не найдены. Предпринята дальнейшая попытка охарактеризовать аномальный сывороточный белок. Иммуноглобулин принадлежит к классу IgG, при этом в сыворотке имеется лишь небольшое количество свободных легких цепей, но все подтипа X. Вопрос 3. Нужно ли еще что-либо делать?
Ответ. Да. Чтобы полностью успокоить пациента (и, возможно, сначала убедить самого себя), необходимо провести рентгенографию черепа и длинных костей. При множественной миеломе можно обнаружить диффузное истощение костной ткани или, чаще, повреждения в виде пробоин (кости напоминают швейцарский сыр).

360Глава 9. Злокачественные опухоли кроветворной ткани
Вотличие от некоторых других новообразований костной ткани, при которых сканирование кости (с использованием радиоактивного технеция) позволяет выявить дефекты, не заметные на простых рентгенограммах, при множественной миеломе сканирование кости обычно дает отрицательный результат ("холодные" образования) даже там, где имеется патология. Это происходит из-за того, что в отсутствии остеобластной активности на фоне преобладания остеокластной активности при большинстве форм миеломы не идет процесс неоваскуляризации. Поскольку основой для поглощения радиоактивного технеция служат новые кровеносные сосуды, связанные с опухолью (это приводит к положительному ["горячему"] результату при сканировании кости), при этой методике изображения кости выглядят нормальными даже при наличии костных плазмоцитом. Хотя на обычных рентгенограммах видны повреждения в виде пробоин.
Вопрос 4. На рентгенограммах не выявлено никаких нарушений. Можно ли сообщитьпациенту теперь, чтоу него нет множественной миеломы? Ответ. Чтобыисключатьприсутствие"тлеющеймножественноймиеломы", прикоторыйболезнь, какправило, ограниченатолькокостныммозгом, необходимовыполнитьаспирациюибиопсиюкостногомозга. Этиисследования показали, что костный мозг не изменен, то есть содержит меньше 5 % плазматических клеток. Вопрос 5. Каков вывод?
Ответ. Хорошее самочувствие пациента в настоящее время и нормальные показатели клинического анализа крови, ее химического состава, рентгенограммы костей и аспирата костного мозга при относительно низком уровне парапротеина и неизмененном уровне других иммуноглобулинов убедительно подтверждают наличие в данном случае доброкачественной моноклональной гаммапатии. Кроме того, запись в истории болезни, сделанная при проведении хирургического вмешательства 7 лет назад, показывает, что содержание белка в сыворотке было повышено уже в то время, что свидетельствует об отсутствии прогрессирования заболевания. Продолжение
наблюдения
После 3-х лет наблюдения у пациента не выявлено изменения уровня иммуноглобулинов и каких-либо клинических признаков развития множественной миеломы. Приблизительно 25-30 % пациентов с доброкачественной моноклональной гаммапатией или моноклональной гаммапатией неизвестного значения прогрессируют до развития полной картины множественной миеломы в течение 20 лет, но этот пациент, по-видимому, пока может просто находиться под наблюдением. Однако ему следует обращать особое внимание на появление болей в костях, которые могут свидетельствовать об остеолитическом повреждении, и отслеживать результаты каждого электрофоретического исследования сывороточных белков, которые могли бы быть первым индикатором прогрессирования болезни.
Клинический пример
78-летняя женщина посещает врача для планового обследования. Она чувствует себя хорошо, но врач обнаруживает несколько эластичных мягких лимфатических узлов размером 1 X 2 см в области шеи слева
1
Лимфомы
______________________________________________________________________ 36 1
ивправойподмышечнойвпадине. Вклиническоманализекрови: лейкоцитов 26 000/мкл, 69 % лимфоцитов, 13 % нейтрофилов, 10 % моноцитов, 5 % атипичных лимфоцитов и 3 % эозинофилов. Гемоглобин — 128 г/л, гематокритное число — 37,5 %, количество тромбоцитов — 353 000/мкл.
Вопрос 1. Каков вероятный диагноз?
Ответ. Картина сопоставима схроническим лимфолейкозом (ХЛЛ). Вопрос 2. Что должно быть выполнено далее?
Ответ. Диагноз может быть подтвержден исследованием иммунофенотипи-ческих маркеров методом проточной цитометрии и цитогенетическим анализом, но сначала необходимо исследовать мазок периферической крови. Вопрос 3. Просмотр мазка периферической крови показал типичные черты хронического лимфолейкоза. Что они включают?
Ответ. Красный ряд клеток морфологически не изменен. Нет полихрома-зии, что позволяет предполагать отсутствие повышения количества рети-кулоцитов. (Если полихромазия и повышение количества ретикулоцитов выявлены при анемии, это позволяет предположить активную потерю крови или гемолиз с последующей компенсаторной реакцией костного мозга.) Морфология тромбоцитов нормальна. В мазке обнаружено несколько нейтрофилов. Лимфоциты находятся в изобилии, большая их часть представлена малыми и зрелыми клетками. Присутствует несколько клеток с нечеткими очертаниями (хрупкие лимфоциты при хроническом лимфолейкозе способны разрушаться в процессе приготовления мазка крови). Вопрос 4. Какой иммунофенотипический профиль является типичным для хронического лимфолейкоза?
Ответ. Большинство маркеров относится к В-клеточным, но имеется двойная экспрессия В-клеточных антигенов CD 19, CD20, CD21, CD24 с Т-кле-точным антигеном CD5 на клетках, что обычно является диагностическим признаком В-клеточного ХЛЛ. Особенно важна для диагностики коэксп-рессия CD20 и CD5. В большинстве случаев на поверхности клетки выявляются моноклональные иммуноглобулины. Иногда обнаруживаются сывороточные парапротеины и/или гипогаммаглобулинемия. Вопрос 5. Какие события в течении заболевания можно прогнозировать? Ответ. Повышение восприимчивости к инфекции, аутоиммунную тромбо-цитопению или гемолитическую анемию, прогрессирующую лимфаденопа-тию и спленомегалию. Не исключен переход в более агрессивную форму лимфомы.
Вопрос 6. Когда пациентка должна начатьлечитьсяпо поводу ХЛЛ? Ответ. Каждая из проблем, упомянутых в пункте 5, является поводом для начала терапии. Кроме того, причиной для начала медикаментозной или лучевой терапии могут служить значительный лейкоцитоз или органные нарушения, обусловленные лимфаденопатией. Продолжениенаблюдения С гематологической точки зрения состояние пациентки не внушает опасе-
ний. Хотя имеется умеренный лейкоцитоз, не отмечено ни одного из грозных осложнений хронического лимфолейкоза, включая трансформацию в агрессивную крупноклеточную лимфому. К сожалению, через 5 лет после постановки диагноза больная погибла в автомобильной катастрофе.
362 |
Глава 9. Злокачественные опухоли кроветворной ткани |
Избранная литература
Canellos G. P. et al. Chemotherapy of advanced Hodgkin's disease with MOPP, ABVD, or MOPP alternating with ABVD. N. Engl.J. Meet., 1992: 327: 1478.
РезультатыбольшогомультицентровогообследованияпациентовсЛГМ, лечившихся с использованием трех наиболее распространенных режимов химиотерапии. ABVD, оказавшийся наиболее эффективным приминимальной токсичности, признан терапией выбора для этих пациентов.
Canellos G. P., Lister Т. Н., Sklar J. L. The Lymphomas. Philadelphia: W. В. Saunders, 1998.
Современныйвсестороннийобзорполимфомам.
Clavell L. A. et al. Four-agent induction and intensive asparaginase therapy for the treatment of childhood acute lymphoblastic leukemia. N. Engl.J. Med., 1986; 315: 657.
Встатье проанализированы результаты лечения острого лимфобластного лейкоза
удетей. Показано, что использование комбинированной химиотерапии существенноповышаетвероятностьизлечения.
Fisher R. I. et al. Comparison of a standard regimen (CHOP) with three intensive chemotherapy regimens for advanced non-Hodgkin's lymphoma. N. Engl. J. Med., 1993;328:1002.
Встатьесравнивается СНОР-химиотерапия сболее сложнымиитоксичными режимами лечения пациентов с крупноклеточной лимфомой. СНОР-терапия столь жеэффективна, какидругиевариантылечения, нопереноситсялучше.
Foon К. A., Rai К. R., Gale R. P. Chronic lymphocytic leukemia: New insights into biology and therapy. Ann. Intern. Med., 1990; 113: 525.
Великолепныйобзорпобиологии, патофизиологииилечениюХЛЛ.
French Cooperative Group on Chronic Lymphocytic Leukemia. Effects of chlorambucil and therapeutic decision in initial forms of chronic lymphocytic leukemia (Stage A): Results of a randomized clinical trial on 612 patients. Blood, 1990; 75: 1414.
Результаты большого рандомизированного исследования показывают, что лечение ХЛЛнараннихстадияхзаболеваниянеповышаетвыживаемости. Целесообразно начинать его только тогда, когда болезнь прогрессирует и появляются симптомыилиорганныенарушения.
Gahrton et al. Allogeneic bone marrow transplantation in multiple myeloma. N. Engl.J. Med., 1991; 325:1267.
Исследование результатов трансплантации костного мозга у пациентов с множественной миеломой показывает, что этот метод имеет ограниченное применениеутакихбольных.
Harris N. et al. A revised European-American classification of lymphoid neoplasms: a proposal from the International Study Group. Blood, 1995; 84: 1361.
Представлена пересмотренная и достаточно полная классификация злокачественныхлимфом, котораянашлаширокоепризнание.
Hjorth M. et al. Initial treatment in multiple myeloma: No advantage of multidrug chemotherapy over melphalan-prednisone. Br.J. Haematoi, 1990; 74: 185.
Показано, что интенсивная химиотерапия не обеспечивает никаких преимуществ перед"мягким" мелфаланомипреднизалономприлечениибольныхмиеломой.

364
■илучеваятерапияявляютсямутагеннымиивызываютлейкозисолидныеопухоли
уперенесших эту болезнь. Представлен отчет о 1500 пациентах с подробным анализомэффектовсовременноголечения.
Warrell Jr. R. P. et al. Differentiation therapy of acute promyelocytic leukemia with tretinoin (All-trans-retinoic acid). N. Engl.J. Med., 1991; 324:1385.
Одно из первых указаний на способность ATRA вызвать дифференцировку клеток острого промиелоцитарного лейкоза, что ведет к клинической ремиссии. Это также наиболее наглядный пример связи между хромосомной аномалией и специфическимвмешательством, нацеленнымнаеекоррекцию.
Zittoun R. et al. Alternating v repeated postremission treatment in adult acute myelogenous leukemia: A randomized phase III study (AML6) of the EORTC Leukemia Cooperative Study. Blood, 1989; 73: 896.
Результаты крупного исследования по сравнению стандартной химиотерапии салло-генной и аутологичной трансплантацией костного мозга у пациентов с ОМЛ. Показано, что дополнительное интенсивное лечение, которое является частьюпроцедурытрансплантации, способноповышатьвыживаемость.

Глава 10
Гематологические проявления ВИЧ-инфекции
Бхарат Рамратнан, Джанти Парамесваран, Тимоти П. Фланиган, Джеймс А. Хокси
Синдром приобретенного иммунодефицита (СПИД), вызываемый вирусом иммунодефицита человека (ВИЧ), впервые был зарегистрирован в 1983 г. Несмотря нато, чтоВИЧ, принадлежащийкгрупперетровирусов, выделяетсяиз многихжидкихсредорганизма, распространениезаболеванияможетпроисходить только при половом (гомоили гетеросексуальном) контакте, парентерально (трансфузия зараженной крови и ее продуктов или внутривенное введение наркотиков) и вертикально (от зараженной матери к ребенку). По приблизительным оценкам, на сегодняшний день этим вирусом инфицированы более20 млн человек по всему миру. ВСШАежегодно инфицируется около40 тыс. человек. В 1996 г. СПИД стал основной причиной смерти мужчин в возрасте от 25 до 44 лет.
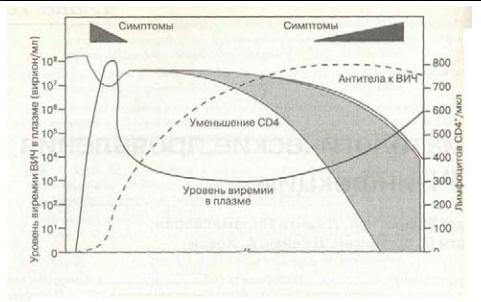
Отдельные фазы ВИЧ-инфекции определяются в соответствии с лабораторными и клиническими данными (рис. 10-1). Механизмы, с помощью которых ВИЧ-инфекция приводит к состоянию иммунной недостаточности, продолжают интенсивно исследоваться и, по-видимому, являются отражением комплексного взаимодействия между вирусом и его носителем. ВИЧ способен поражать множество клеток, однако максимальные разрушения он производит в CD4-лимфоцитах и макрофагах. Именно количественные и качественные патологические изменения СО4-лимфо-цитов представляются центральным звеном развития иммунной дисфункции при СПИД. Предполагаются 2 механизма истощения этих клеток: прямое уничтожение и разрушение, опосредованное клеточным или гуморальным ответом на ВИЧ-инфицирование. Задолго до того, как СО4-клетки гибнут, они теряют свою способность к стимуляцииэффективногоиммунногоответанаВИЧидругиеинфекции.
Гематологические проявления ВИЧ-инфекции обширны и включают анемию, лейкопению, тромбоцитопению и нарушения свертываемости. Патогенетические механизмы разнообразныи могут содержать следующие звенья:
-прямое поражение клеток костного мозга или других клеток, необходимых для гемопоэза;
-нарушениерегуляциииммуннойсистемы, приводящеекразрушениюилиугне тениюгемопоэтическихклетокипродукциианомальныхиммуноглобулинов;
-осложнения антиретровирусной терапии;
-вторичные осложненияпри оппортунистических инфекциях, малигнизации и/или лечении этих заболеваний (табл. 10-1,10-2).
366Глава 10. Гематологические проявления ВИЧ-инфекции
i
I |
I I I |
i " I |
I i |
I I I " |
1 |
234562468 |
10 |
12 |
Годы от момента |
Месяцы от момента |
|
|
||
|
инфицирования |
|
инфицирования |
|
Рис. 10-1. Течение ВИЧ-инфекции. (По: Flanigan Т. P. et al. Update of HIV and AIDS in North America. R. I. Med., 79(5): 181; 1996.)
Патология клеток красной крови
Анемия является обычной для ВИЧ-инфицированных пациентов, причем ее выраженность увеличивается при развитии заболевания. На ранней стадии заболевания умеренное, но значимое уменьшение гематокрита наблюдается у 15-20 % пациентов и у 75-90 % больных — в случаях, когда ВИЧ-инфекция осложняется другими оппортунистическими инфекциями. Однако анемия у пациентов, не принимающих зидовудин, как правило, носит нормоцитарный и нормохромный характер. Макроцитоз встречается у большинства пациентов, получающих терапию зидову-дином в течение двух и более недель. Макроцитоз, обусловленный действием зидо-вудина, не связан с дефицитом витамина В12 или фолатов. Анемия может быть результатом депрессии или неэффективности эритропоэза, острой или хронической кровопотери, а также периферической деструкции красных кровяных клеток.
Депрессия или неэффективность эритропоэза при анемии, вызванной ВИЧ-инфекцией, сопровождается низким или неадекватным уровнем ретикулоцитов. Часто при исследовании костного мозга не обнаруживаются специфические гис-топатологические изменения, аотмечается возрастание числа эритроидных клеток-предшественников на фоне дисэритропоэза различной степени тяжести. Подавление активности костного мозга происходит из-за применения лекарственных препаратов, оппортунистических инфекций, злокачественных новообразований, алиментарной недостаточности и, наконец, прямого действия ВИЧ.
Большинство лекарственных средств, используемых для лечения СПИД и его осложнений, подавляютэритропоэз(табл. 10-2). Антиретровирусныйпрепарат зидовудин вызывает макроцитарную анемию. Ее тяжесть зависит от дозы зидову-дина. Если последний изначально применяется в высоких дозах (> 1000 мг/сут), то приблизительно у 1/3 ВИЧ-инфицированных пациентов развивается резкая анемия (содержание гемоглобина < 80 г/л). Это особенно характерно для про-

Патология клеток красной крови |
367 |
ТАБЛИЦА 10-1. Гематологические проявления некоторых ВИЧ-ассоциированных инфекций
Нозологическая Постановка диагноза |
|
Гематологические Лечение |
|||||||
форма |
|
|
|
|
|
|
и клинические проявления |
||
Вирусные |
Выявление антител |
IgM |
кПоражение |
|
Назначение внут- |
||||
Парвовирус |
|
||||||||
В19 |
В19 (могут отсутствовать в предшественни- |
ривенных препа- |
|||||||
|
прогрессирующей |
стадии ков эритроцитов и |
ратов иммуно- |
||||||
|
заболевания) |
Выявление симптомы тяжелой |
глобулина |
||||||
|
наличия |
вирусной |
ДНК анемии |
|
Оптимизация ан- |
||||
|
методом ПЦР в сыворотке Количество |
|
тивирусной тера- |
||||||
|
крови или костном мозге |
рети-кулоцитов |
пии |
||||||
|
Выявление |
парциальной |
|
|
|
||||
|
красноклеточной аплазии и |
|
|
|
|||||
|
наличия |
|
гигантских |
|
|
|
|||
|
пронор-моцитов в костном |
|
|
|
|||||
|
мозге |
|
|
|
|
|
|
|
|
Цитомегало- |
Выявление внутриядерных Цитопения, |
колит, |
Применение ган- |
||||||
вирус |
включений в клетках костзрительные расцикловира или |
||||||||
|
ного мозга или гастроинстройства |
|
фоскарнета |
||||||
|
тестинальном биоптате |
|
|
|
|
||||
|
Исследование сетчатки |
|
|
|
|
||||
Бактериальная |
Выделение |
культуры |
из |
|
Комбинирован- |
||||
Диссеминирован-Mycobacterium костного мозга либо изоная |
ное лечение |
||||||||
avium |
лированной гемокультуры |
CD4 < 50 |
|
активной формы |
|||||
intracellulare |
и/или визуализация кис- |
Инфильтрация ко- |
заболевания с |
||||||
|
лотоустойчивых организ- |
стногомозгаспри- |
использованием |
||||||
|
мов в биоптате костного |
знаками анемии и |
макролидных |
||||||
|
мозга |
|
|
|
|
|
нейтропении |
|
антибиотиков |
|
|
|
|
|
|
|
|
|
(кларитромицин |
|
|
|
|
|
|
|
|
|
или азитромицин) |
Грибковые |
Выделение культур из раз- |
Цитопения на |
Применение |
||||||
|
личных |
сред |
организма, |
фоне инфильт- |
антигрибковых |
||||
|
включая |
аспираты |
кост- |
рации костного |
средств, включая |
||||
|
ного мозга, и/или выявле- |
мозга при |
|
триазолы |
|||||
|
ние возбудителя в биопта- |
диссе-минирован |
(флу-коназол, |
||||||
|
те костного мозга при со- |
ном заболевании |
итрако-назол), |
||||||
|
ответствующем |
гистохи- |
|
|
или |
||||
|
мическом окрашивании |
|
|
|
амфотерицина В |
||||
Протозойные |
Выделение |
культур |
из Цитопении на фо- |
Сочетание |
|||||
Leishmania |
крови, костного мозга, пене гиперсплениз- |
противопарази- |
|||||||
species |
чени, лимфатических уз- |
ма, инфильтрации тарных средств и |
|||||||
|
лов или селезенки |
|
|
|
костного мозга и амфотерицина В |
||||
|
Гистохимическое |
исслевозможного ауто- |
|
||||||
|
дование |
|
|
|
|
|
иммунного |
про- |
|
|
|
|
|
|
|
|
цесса |
|
|
