- •Физико-химия и технология полимеров, полимерных композитов
- •Введение
- •ГлаВа 1. Основные определения и понятия высокомолекулярных соединений
- •Номенклатура полимеров
- •Классификация вмс
- •Сополимеры
- •Основные отличия вмс от низкомолекулярных соединений
- •Значение вмс в природе, технике, технологии
- •Вопросы для самоподготовки
- •Глава 2. Методы получения полимеров
- •Синтез полимеров реакцией цепной полимеризации
- •Мономеры реакции полимеризации
- •Радикальная полимеризация
- •Кинетические закономерности
- •Регуляторы и ингибиторы
- •Влияние различных факторов на процесс радикальной полимеризации
- •Ионная полимеризация
- •Катионная полимеризация (кп)
- •Катализаторы катионной полимеризации. Сокатализаторы
- •Механизм и кинетика катионной полимеризации
- •Факторы, влияющие на процесс катионной полимеризации
- •Анионная полимеризация
- •Механизм и кинетика анионной полимеризации
- •Анионно-координационная полимеризация
- •Полимеризация полиеновых соединений
- •Полимеризация с раскрытием цикла
- •Ступенчатая полимеризация
- •Поликонденсация
- •Факторы, влияющие на процесс поликонденсации
- •Способы проведения полимеризации и поликонденсации
- •Вопросы для самоподготовки
- •Глава 3. Физико-Механические свойства полимеров
- •Гибкость цепи полимеров
- •Термодинамическая и кинетическая гибкость
- •Параметры, определяющие гибкость цепи
- •Факторы, влияющие на термодинамическую гибкость цепи
- •Факторы, влияющие на кинетическую гибкость цепи
- •Физические состояния полимеров
- •Вопросы для самоподготовки
- •Глава 4. Растворы высокомолекулярных соединений
- •Сравнительные особенности золей и растворов высокомолекулярных соединений
- •Термодинамика растворения вмс
- •Набухание вмс
- •Свойства растворов вмс
- •Вязкость растворов вмс
- •Изоэлектрическая точка полиамфолитов
- •Мембранное равновесие
- •Устойчивость растворов вмс
- •Коллоидная защита
- •Пластификация и применение растворов вмс
- •Вопросы для самоподготовки
- •Глава 5. Химические превращения полимеров
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Макромолекулярные реакции
- •Реакции концевых групп
- •Реакции деструкции
- •Химическая деструкция полимеров
- •Физическая деструкция полимеров
- •Добавки, снижающие скорость старения полимеров
- •Вопросы для самоподготовки
- •Глава 6. Композиционные материалы
- •Факторы, влияющие на процессы образования и свойства композиционных материалов
- •Совместимость компонентов композита
- •Переработка полимерных материалов
- •Некоторые представители композиционных материалов, применяемых в строительстве
- •Понятие адгезии, работа адгезии
- •Теории адгезии
- •Пленкообразующие и лакокрасочные материалы
- •Вопросы для самоподготовки
- •Лабораторные работы
- •Синтез высокомолекулярных соединений
- •Экспериментальная часть Получение полимеров методом полимеризации
- •Получение полимеров методом поликонденсации
- •Контрольные вопросы и упражнения
- •Физико-механические свойства полимеров
- •Массы полимеров
- •Экспериментальная часть
- •Контрольные вопросы и упражнения
- •Экспериментальная часть
- •Контрольные вопросы и упражнения
- •Экспериментальная часть
- •Контрольные вопросы и упражнения
- •Химические превращения полимеров
- •Экспериментальная часть Полимераналогичные превращения или реакции звеньев цепи
- •Макрореакции полимеров
- •Контрольные вопросы и упражнения
- •Научно-исследовательская работа
- •Темы рефератов
- •План и порядок оформления рефератов
- •Темы нир по полимерным композиционным материалам
- •Примерный развернутый план проведения исследований
- •Итоговое тестирование
- •Словарь терминов (глоссарий)
- •Библиографический список рекомендуемой литературы Основная литература
- •Дополнительная литература
- •Оглавление
- •3 94006 Воронеж, ул. 20-лет Октября, 84
Получение полимеров методом поликонденсации
Опыт 1.3. Получение новолачной фенолоформальдегидной смолы
Взаимодействие фенолов с альдегидами представляет собой реакцию поликонденсации, условием протекания которой является полифункциональность реагирующих молекул. Реакция характеризуется большим значением константы равновесия (К ~ 10000), и вследствие этого кинетика и степень поликонденсации практически зависят от концентрации катализатора, температуры и времени реакции. Характер и свойства получаемого продукта реакции поликонденсации фенола с альдегидами определяются химическим строением реагирующих молекул, их молярным соотношением и реакцией среды. В зависимости от этих факторов могут быть получены либо термопластичные (новолаки), либо термореактивные (резолы) олигомеры.
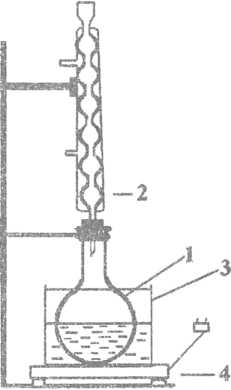
Поместите в колбу (рис. 2) 5 г фенола, 4 мл 40 % формалина, внесите кусочки керамики. Нагрейте смесь на водяной бане до образования однородной жидкости и осторожно кипятите ее 1-2 мин. Затем влейте (из пипетки или из пробирки) 0,4 мл (несколько капель) концентрированной соляной кислоты. При встряхивании через 1-2 мин горячая смесь начинает кипеть без подогревания. Реакционная смесь мутнеет и внизу отслаивается тяжелое, непрозрачное масло. Если кипение прекращается, снова подогрейте смесь на огне в течение 1-2 мин. Затем разберите установку, из реакционной колбы осторожно слейте верхний мутный слой и добавьте примерно такой же объем воды, слейте воду, а смолу с остатками воды вылейте на часовое стекло. Остывшую светло-сиреневую смолу снимите со стекла, высушите ее в фильтровальной бумаге, снимите комочек и произведите взвешивание, рассчитайте выход полимера. При хранении смола постепенно твердеет и делается хрупкой тем быстрее, чем дольше продолжалось кипячение.
Опыт 1.4. Получение резольной фенолоформальдегидной смолы
В круглодонную колбу с обратным холодильником внесите 3 г фенола, 5 мл 40 %-го формалина и 2 мл 25%-го водного раствора аммиака. Содержимое колбы нагревайте на кипящей водяной бане в течение 1 часа. В процессе поликонденсации реакционная смесь мутнеет и разделяется на два слоя: верхний – водный и нижний – густой, светло-желтый продукт поликонденсации. Для более быстрого и равномерного хода реакции реакционную колбу периодически встряхивайте и приливайте ~ по 0,5 мл раствора аммиака.
|
Рис. 2. Схема установки для получения фенолоформальдегидной смолы: 1 – реакционная колба, 2 – обратный холодильник, 3 – водяная баня, 4 – электроплитка
|
По окончании процесса выключите обогрев, отсоедините холодильник, снимите колбу и перенесите ее содержимое в фарфоровую чашку. Водный слой слейте, а смолу, оставшуюся в чашке, несколько раз промойте водой (для удаления исходных продуктов). Нагрейте смолу на плитке и наблюдайте за переходом ее из твердого в вязкое, а затем жидкое состояние, которое при дальнейшем нагревании снова твердеет и меняет цвет желтый на красно-коричневый (резит). Последнюю операцию проводите в вытяжном шкафу!
Напишите уравнения реакций получения новолака, резола и перехода их в резит.
Представьте полную классификацию полученных полимеров, особые условия образования каждого из них.
Укажите возможности использования названных продуктов.
Опыт 1.5. Конденсация карбамида с формальдегидом
(опыт проводить в вытяжном шкафу)
Смесь, состоящую из 3 г карбамида (мочевина, СО(NН2)2) и 8 мл формалина (40%-й водный раствор формальдегида СН2О), осторожно нагрейте в фарфоровой чашке на плитке, добавив несколько капель 2 н. раствора гидроксида натрия. После полного растворения карбамида смесь нагревайте еще несколько минут до превращения ее в вязкую массу (карбамидный клей).
Часть клея перенесите в другую чашку, добавьте 1 – 2 мл воды (можно подкрашенной органическим красителем), нагрейте на плитке до кипения и проведите отверждение с помощью нескольких кристалликов щавелевой кислоты (Н2С2О4).
Напишите уравнения реакций получения и отверждения карбамидо-формальдегидного полимера.
Опыт 1.6. Получение глифталевой смолы
Поместите в широкую пробирку 2 г фталевого ангидрида и 1 г глицерина. Закройте пробирку пробкой с вставленной в нее вертикальной трубкой и нагревайте на плитке, поддерживая непрерывное кипение смеси в течение 1,5 – 2 часов. Жидкость в пробирке постепенно густеет и в конце нагревания желтеет. С увеличением продолжительности нагревания и температуры увеличивается вязкость продукта.
Объясните происходящие со временем изменения в системе и напишите уравнение реакции поликонденсации глицерина и фталевого ангидрида.
Укажите основные направления использования глифталя.
Выводы
1. Назовите основные методы получения полимеров и укажите принципиальные различия между ними.
2. Приведите основные способы получение полимеров и укажите их достоинства и недостатки.
3. Укажите основные стадии процессов образования полимеров и возможности влияния на строение и свойства полимера на каждой из них.
4. Отметьте факторы, влияющие на состав, строение и свойства образующихся полимеров.