
- •Физико-химия и технология полимеров, полимерных композитов
- •Введение
- •ГлаВа 1. Основные определения и понятия высокомолекулярных соединений
- •Номенклатура полимеров
- •Классификация вмс
- •Сополимеры
- •Основные отличия вмс от низкомолекулярных соединений
- •Значение вмс в природе, технике, технологии
- •Вопросы для самоподготовки
- •Глава 2. Методы получения полимеров
- •Синтез полимеров реакцией цепной полимеризации
- •Мономеры реакции полимеризации
- •Радикальная полимеризация
- •Кинетические закономерности
- •Регуляторы и ингибиторы
- •Влияние различных факторов на процесс радикальной полимеризации
- •Ионная полимеризация
- •Катионная полимеризация (кп)
- •Катализаторы катионной полимеризации. Сокатализаторы
- •Механизм и кинетика катионной полимеризации
- •Факторы, влияющие на процесс катионной полимеризации
- •Анионная полимеризация
- •Механизм и кинетика анионной полимеризации
- •Анионно-координационная полимеризация
- •Полимеризация полиеновых соединений
- •Полимеризация с раскрытием цикла
- •Ступенчатая полимеризация
- •Поликонденсация
- •Факторы, влияющие на процесс поликонденсации
- •Способы проведения полимеризации и поликонденсации
- •Вопросы для самоподготовки
- •Глава 3. Физико-Механические свойства полимеров
- •Гибкость цепи полимеров
- •Термодинамическая и кинетическая гибкость
- •Параметры, определяющие гибкость цепи
- •Факторы, влияющие на термодинамическую гибкость цепи
- •Факторы, влияющие на кинетическую гибкость цепи
- •Физические состояния полимеров
- •Вопросы для самоподготовки
- •Глава 4. Растворы высокомолекулярных соединений
- •Сравнительные особенности золей и растворов высокомолекулярных соединений
- •Термодинамика растворения вмс
- •Набухание вмс
- •Свойства растворов вмс
- •Вязкость растворов вмс
- •Изоэлектрическая точка полиамфолитов
- •Мембранное равновесие
- •Устойчивость растворов вмс
- •Коллоидная защита
- •Пластификация и применение растворов вмс
- •Вопросы для самоподготовки
- •Глава 5. Химические превращения полимеров
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Макромолекулярные реакции
- •Реакции концевых групп
- •Реакции деструкции
- •Химическая деструкция полимеров
- •Физическая деструкция полимеров
- •Добавки, снижающие скорость старения полимеров
- •Вопросы для самоподготовки
- •Глава 6. Композиционные материалы
- •Факторы, влияющие на процессы образования и свойства композиционных материалов
- •Совместимость компонентов композита
- •Переработка полимерных материалов
- •Некоторые представители композиционных материалов, применяемых в строительстве
- •Понятие адгезии, работа адгезии
- •Теории адгезии
- •Пленкообразующие и лакокрасочные материалы
- •Вопросы для самоподготовки
- •Лабораторные работы
- •Синтез высокомолекулярных соединений
- •Экспериментальная часть Получение полимеров методом полимеризации
- •Получение полимеров методом поликонденсации
- •Контрольные вопросы и упражнения
- •Физико-механические свойства полимеров
- •Массы полимеров
- •Экспериментальная часть
- •Контрольные вопросы и упражнения
- •Экспериментальная часть
- •Контрольные вопросы и упражнения
- •Экспериментальная часть
- •Контрольные вопросы и упражнения
- •Химические превращения полимеров
- •Экспериментальная часть Полимераналогичные превращения или реакции звеньев цепи
- •Макрореакции полимеров
- •Контрольные вопросы и упражнения
- •Научно-исследовательская работа
- •Темы рефератов
- •План и порядок оформления рефератов
- •Темы нир по полимерным композиционным материалам
- •Примерный развернутый план проведения исследований
- •Итоговое тестирование
- •Словарь терминов (глоссарий)
- •Библиографический список рекомендуемой литературы Основная литература
- •Дополнительная литература
- •Оглавление
- •3 94006 Воронеж, ул. 20-лет Октября, 84
Вязкость растворов вмс
Основными факторами, определяющими структуру и реологические свойства дисперсной системы, является концентрация частиц дисперсной фазы и энергия взаимодействия частиц. В разбавленных агрегативно устойчивых дисперсных системах частицы сохраняют полную свободу взаимного перемещения, или, как говорят, определенная структура отсутствует. Такие системы относятся к ньютоновским. Их вязкость описывается законом Эйнштейна: вязкость дисперсной системы (золя, суспензии) увеличивается с ростом содержания частиц дисперсной фазы. Эта связь выражается уравнением:
(η − η0) / η0 = k·φ, (4.7)
где η и η0 − вязкости коллоидного раствора и дисперсионной среды соответственно; φ = Vd/V − объемная доля дисперсной фазы (Vd) в общем объеме системы (V); k − константа, зависящая от формы частиц.
Физический смысл этого закона заключается в том, что относительное приращение вязкости прямо пропорционально относительному содержанию в системе дисперсной фазы. Чем больше объемная доля дисперсной фазы в системе, тем сильнее выражено тормозящее влияние частиц на поток жидкости (прямая 1 на рис.4.4).
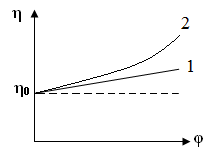
Рис. 4.4. Зависимость вязкости от объемной доли дисперсной фазы для:
1 – бесструктурной (ньютоновcкой) дисперсной системы;
2 – структурированной (неньютоновской) дисперсной системы
Структурированные коллоидные системы не подчиняются закону Эйнштейна. Для них значение вязкости увеличивается с ростом содержания дисперсной фазы значительно сильнее, чем следует из уравнения Эйнштейна (кривая 2 на рис. 4.4). Согласно современным представлениям, достаточно гибкие молекулы ВМС в растворе находятся в виде статистических клубков, пропитанных растворителем. Наличие таких клубков, а также образование структур в растворе обусловливает аномальную зависимость вязкости растворов полимеров от их концентрации, не подчиняющуюся уравнению Эйнштейна. Растворы ВМС – неньютоновские жидкости.
Зависимость удельной вязкости не слишком концентрированных растворов полимеров от концентрации обычно удовлетворительно описывается уравнением, предложенным Хаггинсом:
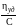 = [η] + k1[η]2С,
(4.8)
= [η] + k1[η]2С,
(4.8)
ηуд = (η − η0) / η0 − удельная вязкость (см. табл. 4.1);
где [η] − характеристическая вязкость (см. табл. 4.1); С − концентрация раствора, г/100 мл; k1 − коэффициент называемый константой Хаггинса.
Коэффициент k1 служит характеристикой взаимодействия макромолекул в системе полимер − растворитель. Его значение практически не зависит от молярной массы полимера и меняется лишь в зависимости от природы растворителя. Во взаимодействующих с ВМС растворителях значение константы Хаггинса составляет 0,2 − 0,3.
Таблица 4.1
Обозначения и названия величин, принятых в вискозиметрии
растворов полимеров
Обозначение величины |
Название |
ηотн = η/η0 |
Относительная вязкость |
ηуд = (η − η0)/η0 = ηотн− 1 |
Удельная вязкость |
ηпр = ηуд/С |
Приведенная вязкость |
ln ηотн /С |
Логарифмическая приведенная вязкость |
[η] = (ηуд/С)С→0 == (ln ηотн /С) С→0 |
Характеристическая вязкость |
Характеристическая вязкость, отражающая гидродинамическое сопротивление молекул полимера потоку жидкости, может быть определена для разбавленных растворов полимеров, в которых взаимодействием макромолекул можно пренебречь. Для нахождения характеристической вязкости устанавливают зависимость приведенной вязкости от концентрации в узком интервале малых концентраций и полученные результаты экстраполируют к нулевой концентрации (рис.4.5).
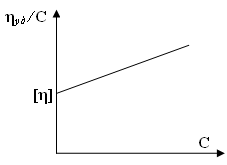
Рис. 4.5. График для определения характеристической вязкости раствора ВМС
Связь между характеристической вязкостью раствора ВМС и молярной массой полимера удовлетворительно описывается эмпирическим уравнением Марка –Хаувинка:
[η] = К·Мα, (4.9)
где α – постоянная (как и «К») для данного полимергомологического ряда в конкретном растворителе при определенной температуре.
Постоянная «α» отражает степень свертывания молекул полимера и гибкость цепи. Для жестких палочкообразных молекул α ≈ 1, для гибких молекул, свернутых в глобулу α ≈ 0,5.
Зная характеристическую вязкость раствора ВМС, по уравнению Марка –Хаувинка можно определить молярную массу полимера:
Мα
=
[η]/
К или lgM
=
 .
(4.10)
.
(4.10)
Следует напомнить, что полученное значение молярной массы является среднестатистическим, поскольку любой реальный полимер (как указывалось выше) представляет собой полидисперсную смесь макромолекул.
