
- •Кислотные и основные свойства органических соединений
- •1. Кислоты и основания Бренстеда
- •Кислоты Бренстеда
- •Кислотность по Бренстеду
- •Факторы, влияющие на силу кислот
- •• Природа атома в кислотном центре
- •• Структурное окружение кислотного центра
- •Электронные эффекты заместителей
- •Стабилизация пара-нитрофенолят-аниона за счет –М-эффекта нитрогруппы
- •Основания Бренстеда
- •Основность по Бренстеду
- •Факторы, влияющие на силу оснований
- •Увеличение электроотрицательности
- •• Структурное окружение основного центра
- •Ароматические амины
- •Электронные эффекты заместителей
- •Снижение основности пара-нитроанилина под действием –М-эффекта нитрогруппы
- •Основность гетероциклических соединений
- •2. Кислоты и основания Льюиса
- •Жесткие и мягкие кислоты и основания
- •Структурное окружение кислотного центра
- •Факторы, влияющие на силу оснований
- •Структурное окружение основного центра
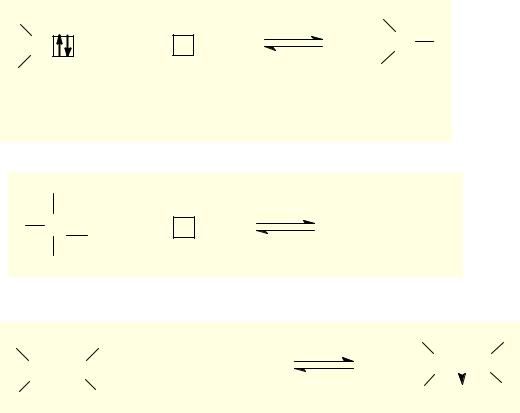
2. Кислоты и основания Льюиса
Основания Льюиса – это доноры пары электронов.
Кислоты Льюиса – это акцепторы пары электронов, т.е. частицы, имеющие вакантную орбиталь (катионы: H+, Na+, Mg2+, Ag+; галогениды: BF3, AlCl3, FeCl3)
R
O
..
R
îñí î âàí èå
äî í î ð
H
RN  H
H
R R
C  C
C
HH
+ |
H+ |
кисло та
акцеп то р
+ |
BF3 |
+ Ag+
R +
O H
..
R
|
|
H |
- |
|
|
|
|||
|
|
|
|
+ |
|
|
|
||
|
|
|
|
||||||
R |
|
N |
|
|
BF |
||||
|
|
|
|||||||
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
||||
|
|
H |
|
|
|
|
|||
|
|
|
|
R |
|
|
|
R |
|
|
|
|
|
H |
C |
|
|
C |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
|
|
|
|
Ag+ H |
|||||

Жесткие и мягкие кислоты и основания
Жесткие |
Промежуточные |
Мягкие |
||
|
|
Кислоты |
|
|
H , Na , K , Mg2 , |
Cu2 , |
Fe2 , |
Zn2 , |
Ag , Hg2 , I2 |
Ca 2 , Al3 , Fe3 , BF , |
R 3C |
|
|
|
3 |
|
|
|
|
AlCl , R C O |
|
|
|
|
3 |
|
|
|
|
|
|
Основания |
|
|
Н2О, OH , F , ROH, |
ArNH2 , Br , C5 H5 N |
R 2S, RSH, RS-, I , H , |
||
RO , R 2О, NH3 , RNH2 |
|
|
|
C2 H4 , C6 H6 |
Принцип ЖМКО:
Жесткие кислоты лучше взаимодействуют с жесткими основаниями, а мягкие кислоты - с мягкими основаниями.
2 RS- + |
Hg2+ |
|
(RS)2Hg |
|
|||
ì ÿãêî å |
м ягкая |
|
|
î ñí î âàí èå |
кисло та |
|
|

Структурное окружение кислотного центра
ROH |
HOH |
ArOH |
RCOOH |
pKa 16-17 |
15,7 |
8-11 |
4-5 |
Увеличение кислотности
|
|
|
O |
|
|
|
O |
+ |
H+ |
CH |
|
C |
|
|
CH3 |
|
C - |
||
|
|
|
|||||||
|
|
|
|
||||||
|
|
||||||||
3 |
|
|
OH |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
||
Карбо н о вая кисло та |
Карбо ксилат-ан ио н |
|
|
||||||
Стабилизации за счет p- сопряжения

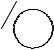
 OH
OH 
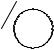
 O- + H+
O- + H+
Ôåí î ë |
Ôåí î ëÿò-àí èî í |
Стабилизации за счет p- сопряжения
R |
|
OH |
|
R |
|
O- |
+ H+ |
|
|
||||||
|
|
|
|||||
|
|
||||||
ñï èðò |
|
àëêî ãî ëÿò |
|
||||
|
|
|
àí èî í |
|
|||
нет стабилизации
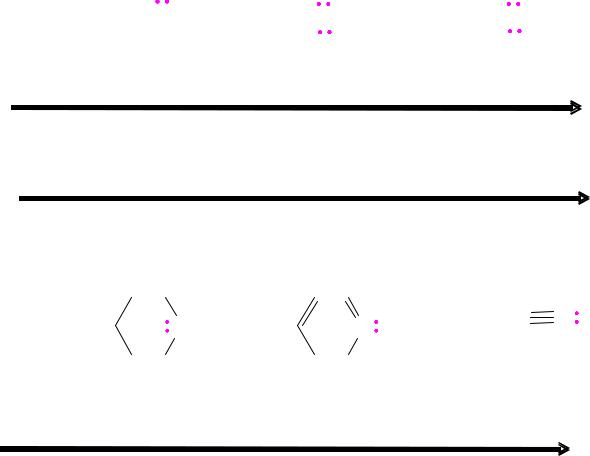
Факторы, влияющие на силу оснований
Природа атома в основном центре
аммониевые > оксониевые > сульфониевые
|
RNH2 |
ROH |
RSH |
pKBH+ |
10-11 |
-2 |
-7 |
Уменьшение основности
Увеличение электроотрицательности
|
|
|
sp3 |
|
sp2 |
sp |
||
|
|
|
NH |
N |
CH3C N |
|||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
pKBH+ 11,2 |
5,2 |
|
|
-4,3 |
||||
Уменьшение основности
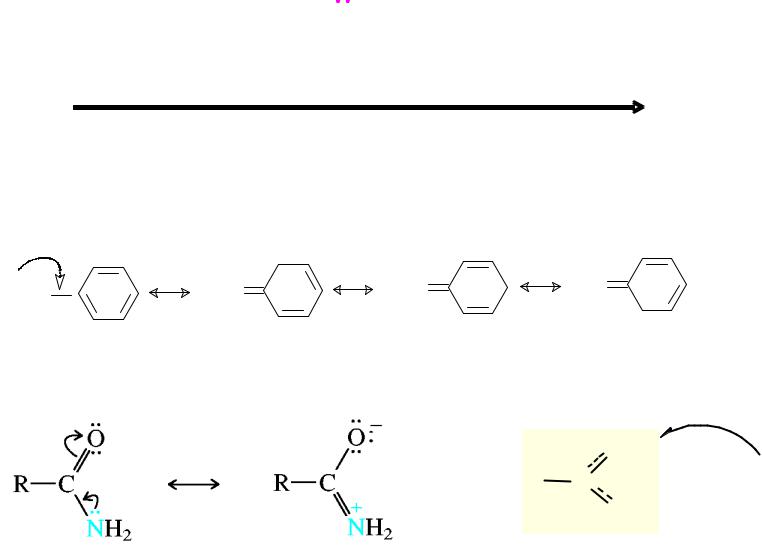
Структурное окружение основного центра
|
RNH2 |
ArNH2 |
RCONH2 |
pKBH+ |
10-11 |
3-5 |
-1,5 -0,5 |
Уменьшение основности Ароматические амины
.. |
-.. |
+ |
.- |
+ |
+ |
NH2 |
|||
|
NH |
NH |
. |
|
NH2 |
2 |
|
-.. |
|
2 |
|
|
||
|
|
|
|
Амиды
O |
H+ |
R C |
|
NH2 |
|
