
2293
.pdfПример. Определить радиус критического зародыша диоксида углерода при Т = 180 К и переохлаждении потока Т = 12,5 К.
По пункту 6 приложения определяем свободную поверхностную энергию образования зародыша:
= 0,5065·10-3 – 0,80854·10-2(180/304) + 0,36925·(180/304)2 –0,49622·(180/304)3 = 0,022166 Н/м.
Плотность твердой фазы СО2 находим по пункту 1 приложения:
Т = 1501 + (216,58 – 180)·103 / [4,8·(216,58 – 180) + 247] = 1587,6 кг/м3.
Удельную теплоту кристаллизации СО2 рассчитываем по пункту 5 приложения:
L = 691942,88 – 56822,64·(180/100) – 3049,55·(180/100)2 + + 75,06·(180/100)3 = 584200 Дж/(кг·К).
Радиус критического зародыша СО2 определяем по (4.24):
r |
2 0,022166 180 |
0,688 10 9 м. |
|
1587,6 584200 12,5 |
|||
КР |
|
Каждый зародыш состоит из некоторого числа единичных молекул. Если полагать, что расстояние между ними не зависит от их числа, то число молекул в зародыше критического радиуса можно определить по формуле
n V КР/VМ ,
где V КР 4 rКР3 /3 – объем зародыша критического радиуса;
VМ C / T NA – объем молекулы.
Для твердого диоксида углерода при плотности Т = 1600 кг/м3 объем молекулы VМ = 45,7∙10-30 м3, а радиус – 2,22∙10-10 м. На рис. 4.27 представлены зависимости числа молекул СО2 в зародышах критического радиуса от степени переохлаждения. При Т = 12,5 13 К зародыш радиуса rКР состоит из 4 5 десятков молекул.
Пример. Определить число молекул в радиусе критического зародыша
rКР = 0,688·10-9 м.
Объем зародыша критического радиуса
V КР 4 rКР3 /3= 4 (0,688·10-9)3 / 3 = 1,364·10-27 м3.
При объеме молекулы СО2 VМ = 45,7·10-30 м3 число молекул в зароды-
ше
n = VКР / VМ = 1,364·10-27 / 45,7·10-30 ~ 30 молекул.
Известные значения свободной поверхностной энергии образования зародыша относятся к плоской поверхности раздела фаз и справедливы для
100
сравнительно крупных частиц. Для зародышевых частиц, состоящих из ограниченного числа молекул, понятие о свободной поверхностной энергии образования зародыша является условным, тем не менее его необходимо вводить в теоретические формулы. Поэтому по аналогии с теорией конденсации влажно-паровых турбин [20] предлагается ввести поправку следующего вида:
|
|
|
|
|
r |
|
|
, |
(4.25) |
|
||||
|
|
1 2 / r |
|
|
где r – свободная поверхностная энергия для частицы радиусом r ; поправка ~ 10-10 м.
Образование новой фазы возможно только при более высокой температуре частичек, чем температура окружающего газа. Это необходимо для отвода теплоты фазового перехода с поверхности частичек. А. Стодола исходя из условий роста капель водяного пара, уравнений теплообмена и баланса энергии для всего двухфазного потока установил, что в расчетах температуру капли ТК с достаточной точностью можно принять равной ее равновесной температуре для капли данного радиуса при данном давлении, т.е. ТК = ТSr .
На основании этого на данном этапе развития теории процесса расширения парогазовой смеси в турбодетандере полагаем, что температура частичек диоксида углерода
|
|
2 r |
|
|
|
TH TSr |
|
|
(4.26) |
||
|
|||||
TS 1 |
|
. |
|||
|
|
T Lr |
|
||
При образовании твердого диоксида углерода из продуктов сгорания топлива возникает вопрос о скорости изменения температуры внутри частицы СО2 . А. Стодола, рассматривая теплопроводность капли водяного пара малого радиуса, показал, что температурное поле внутри нее выравнивается очень быстро, и за это время капля может сместиться лишь на малый отрезок вдоль сопла. И.И. Кириллов и Р.М. Яблоник [20], решая дифференциальное уравнение теплопроводности в шаре применительно к капле водяного пара радиусом 10-8 м, показали, что температурное поле внутри капли малого радиуса выравнивается чрезвычайно быстро, и за это время капля жидкости может сместиться лишь на малое расстояние в процессе движения. Исходя из этого, полагаем, что температура в центре и на поверхности мелких частиц СО2 , образовавшихся при расширении ПСТ в турбодетандере, одинаковая.
Теоретическое описание течений с конденсацией основывается на использовании выражения для скорости образования зародышей. Вывод такого выражения является одной из наиболее сложных проблем кинетики конденсации. Классическая теория образования зародышей была предло-
101

жена Фольмером и Вебером и развита в работах Беккера и Деринга, Зельдовича и Френкеля. Описание ряда процессов, основанное на этой теории, согласуется с экспериментом.
Число зародышей критического радиуса как для каплеобразных зародышей, так и для кристаллов определяется по формуле ФренкеляЗельдовича [20]:
|
2 |
1 |
p |
П |
2 |
|
П |
|
|
|
4 |
r2 |
|
|
|||||
I |
|
|
|
|
|
|
|
|
|
|
exp |
|
|
, |
(4.27) |
||||
|
|
|
|
|
|
|
NA |
3kT |
|||||||||||
|
|
|
|
H kT |
|
|
|
|
КР |
|
|||||||||
где k – постоянная Больцмана; рП и Т – давление и температура пара; П – молекулярная масса пара; Н – плотность новой фазы; NА – число Авогадро.
С учетом (4.24) и того, что число k = П RП / NA, после преобразований (4.27) получим формулу скорости образования зародышей критического размера, возникающих в единицу времени в единице объема:
|
|
|
|
|
|
|
|
|
|
|
1,5 |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
2 |
П |
|
рП |
|
NA |
|
|
|
16 NA |
||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
I |
|
|
|
|
|
|
|
|
|
2 |
|||||||||
|
|
|
|
|
|
|
exp |
3 |
П RПТ |
|
, (4.28) |
||||||||
|
|
|
Н RПT |
П |
|
|
Н Lln TS /T |
|
|||||||||||
где П – плотность пара; RП – газовая постоянная пара.
Скорость ядрообразования – функция давления, температуры и переохлаждения T. Последнее оказывает особенно сильное влияние, так как критический радиус частиц, согласно (4.24), приблизительно обратно пропорционален T.
Классическая теория неоднократно подвергалась критике за применение формулы Кельвина к малым зародышам, состоящим из нескольких молекул, для которых понятие о поверхностном натяжении весьма условно. Кроме того, при выводе уравнения (4.27) не брался во внимание важный вклад в энергию образования зародыша поступательного и вращательного движений небольших молекулярных комплексов (кластеров). Еще одним недостатком теории является обязательное выполнение условия квазистационарности, которое заключается в том, что время создания перенасыщения в системе должно быть намного больше времени установления равновесного распределения зародышей по размерам. Многочисленные попытки уточнить формулу Френкеля-Зельдовича не подтверждались экспериментом, тогда как конденсация, рассчитанная по (4.27), удовлетворительно совпадала с результатами опытов.
В данном случае влиянием посторонних частиц как центров образования новой фазы пренебрегаем, считая, что рабочее вещество тщательно
102

очищено, а масса паров, способных конденсироваться или кристаллизоваться на более высоком температурном уровне, ничтожно мала.
Скорость образования зародышей критического размера является определяющим фактором кристаллизации СО2 из продуктов сгорания топлива и определяется по формуле Френкеля-Зельдовича (4.28), которая для скорости ядрообразования СО2 из ПСТ примет вид
|
|
|
0,5 |
|
|
|
1,5 |
|
|
2 |
|
|
|
|
|
|
3 |
|
2 |
|
NA |
pП |
|
|
|
|
16 NA |
||||||||||
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
I |
|
|
|
|
|
|
|
2 |
|
|
2 |
|||||||
|
|
|
|
|
T |
|
|
exp |
|
,(4.29) |
||||||||
|
|
|
|
C |
|
|
|
T RC |
|
|
3 CRCТ T Lln TS /T |
|
||||||
где С и RС – молекулярная масса и газовая постоянная СО2 ; рП = rС р – парциальное давление паров СО2 в ПСТ; р – давление ПСТ.
С учетом (4.24) и того, что число Авогадро NА = 6,0221169∙1026 кмоль-1;С = 44 кг/кмоль; RC = 188,96 Дж/(кг∙К), уравнение (4.29) запишется в виде
2
I 1,13153 1033 rC p  exp 3,03407 1023 rКР2 /T . (4.30)
exp 3,03407 1023 rКР2 /T . (4.30)
T T
Скорость ядрообразования СО2 является функцией парциального давления паров СО2 и степени переохлаждения Т. Переохлаждение оказывает влияние на показатель степени в уравнении (4.30), так как критический радиус зародыша, согласно (4.24), приблизительно обратно пропорционален Т. В области малых переохлаждений (рис. 4.28, а) кристаллизация протекает очень медленно и увеличивается с ростом Т. При больших переохлаждениях происходит бурное образование зародышей критического радиуса. При Т = 12,5 13 К; rС = 0,03 0,14 и р = 0,2 МПа скорость ядрообразования I = 1022 1024 1/(м3∙с).
lgI, |
rC = 0,138 |
|
р = 0,8 МПа |
lgI, |
р = 0,8 МПа |
|
|
|
|
1/(м3 c) |
|
|
|
1/(м3 c) |
|
|
|
||
30 |
|
|
|
|
30 |
|
|
|
|
|
|
|
rC = 0,033 |
|
|
|
р = 0,2 МПа |
||
20 |
|
|
|
|
20 |
|
|
|
|
|
|
р = 0,2 МПа |
|
|
|
|
rC = 0,138 |
||
10 |
10 |
20 |
30 |
Т, К |
10 |
10 |
20 |
30 |
Т, К |
0 |
0 |
||||||||
|
|
a |
|
|
|
|
б |
|
|
Рис. 4.28. Влияние степени переохлаждения потока ПСТ на скорость ядрообразования: – с учетом влияния rКР на ;  – без учета влияния rКР на
– без учета влияния rКР на
103

Пример. Определить скорость образования зародыша критического размера при переохлаждении потока Т = 12,5 К, давлении ПСТ р = 2·105 Па, температуре Т = 180 К и объемной концентрации СО2 rС = 0,138.
По условиям примера |
|
|
Т = 1587,6 кг/м3 ; |
= 0,022166 Н/м; rКР = |
||||||
= 0,688·10-9 м. |
|
|
|
|
|
|
|
|
|
|
Скорость ядрообразования находим по формуле (4.29) |
||||||||||
|
|
|
|
0,138 2 105 |
2 |
|
|
|
||
|
33 |
|
0,022166 |
|
|
|||||
I 1,13153 10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
180 |
|
|
1587,6 |
|
||||
|
|
|
|
|
|
|
||||
exp[ 3,03407 1023 0,022166 0,688 10 9 2 /180] 1,3 1023 1/(м3·с).
На рис. 4.28, б пунктирными линиями показаны зависимости скорости ядрообразования, полученные без учета поправки влияния радиуса частиц на свободную поверхностную энергию образования кристалла. Учет влияния r на заметно повышает скорость ядрообразования зародышей, то есть можно ожидать бурное образование зародышей при меньших значениях переохлаждения по сравнению с вычисленными без учета зависимости от радиуса частиц.
Процесс ядрообразования является только составной частью процесса кристаллизации диоксида углерода. Возникшие зародыши начинают расти. Увеличение зародыша обусловлено кристаллизацией пара на поверхности частиц и отводом теплоты фазового перехода.
Для выяснения процесса роста частиц и их движения важное значение имеет соотношение между радиусом частиц и средней длиной l свободного пробега молекул парогазовой среды. Последнюю величину можно определить по формуле
l |
|
|
9 RT |
, |
|
p |
8 |
||||
|
|
||||
где , R и р – соответственно динамическая вязкость, газовая постоянная и давление продуктов сгорания топлива.
Отношение длины свободного пробега молекулы к диаметру частицы носит название числа Кнудсена:
Kn l /(2r).
С помощью этого критерия можно разграничить период устойчивого роста частиц на две стадии. В начальной (микроскопической) стадии, когда размеры частиц малы по сравнению с длиной свободного пробега молекулы (Kn > 1), рост частиц обуславливается законами молекулярного переноса, в соответствии с которыми увеличение радиуса частицы определяется числом сталкивающихся с частицами молекул и долей тех молекул, которые покидают частицу и отводят теплоту фазового перехода. В этом слу-
104

чае рост частиц за время d может быть описан формулой, предложенной Булером:
dr |
c |
PП |
|
|
П |
|
RП T |
|
Т |
T |
Т |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
, |
(4.31) |
|||
|
|
L T |
|
2 |
1 2 r / T rL |
||||||||||
d |
|
|
|
|
|||||||||||
где сРП – теплоемкость пара.
Так как |
dr |
c |
dr |
, где с – абсолютная скорость потока, то из (4.31) по- |
|
d |
dx |
||||
|
|
|
лучаем следующую формулу, описывающую рост частицы диоксида углерода вдоль каналов проточной части турбодетандера:
dr |
|
cPП |
|
П |
|
RПT |
|
ТT |
Т |
|
. |
(4.32) |
|
|
|
2 1 2 r |
/ T rL |
||||||||
dx cL T |
|
|
|
|||||||||
Когда размер частицы превышает среднюю длину свободного пробега молекулы (Kn < 1), рост частиц определяется законами тепломассообмена, то есть физическими свойствами новой фазы и градиентом температуры в парогазовой смеси, окружающей частицу. В этом случае рост частицы диоксида углерода вдоль канала проточной части детандера описывается уравнением
dr |
|
|
ТT |
Т |
|
||
|
|
|
|
|
|
, |
(4.33) |
|
c T L |
|
|
|
|||
dx |
|
|
r |
|
|||
где – коэффициент теплопроводности продуктов сгорания топлива. Приведенные соотношения могут быть использованы для расчета
процесса кристаллизации диоксида углерода из ПСТ, расширяющейся в турбодетандере.
4.5. Математическая модель течения ПСТ с образованием твердой фазы диоксида углерода в проточной части турбодетандера
Для полной характеристики процесса образования твердой фазы диоксида углерода в проточной части турбодетандера необходимо знать изменение состояния продуктов сгорания топлива, скорости ядрообразования и роста частиц новой фазы. Для решения этой задачи рассмотрим одномерное течение парогазовой смеси, которое подчиняется общим законам сохранения массы и энергии, состояния и количества движения в сочетании с кинетическими представлениями о процессах формирования и роста устойчивых центров кристаллизации. В основе вывода уравнений, описывающих связи между характерными параметрами потока, лежит ряд допу-
105
щений. К числу их относятся представления о стационарности и однородности в поперечных сечениях потока полей давлений, температур, а также скоростей каждой из фаз.
Уравнение неразрывности. При установившемся течении через любое сечение проточной части турбодетандера проходит одна и та же масса G рабочего вещества. Если масса газа GГ , а твердой фазы GТ , то сумма масс должна быть постоянной для любого сечения проточной части:
GГ + GТ= G = const
или |
|
G = FГ Г wГ + FТ Т wТ , |
(4.34) |
где FГ и FТ – условная площадь поперечного сечения канала, занимаемая |
|
газообразной и твердой фазами рабочего вещества; Г и wГ , |
Т и wТ – |
плотность и относительная скорость газообразной и твердой фаз соответственно.
Введем допущения о том, что частицы новой фазы, возникающие в перенасыщенном газовом потоке, весьма малы и скорость их близка к скорости газовой составляющей потока (коэффициент скольжения wТ / wГ ~ 1). Предположим, что масса твердой фазы, выпадающей в зоне перенасыщенного состояния, мала, а в рассматриваемом диапазоне температур плотность твердой фазы существенно превышает плотность газа. Тогда доля сечения канала, занимаемая новой фазой, столь мала, что допустимо считать FГ равной площади поперечного сечения канала F. Для этих условий уравнение неразрывности (4.32), записанное в дифференциальной форме, примет вид
w |
dF |
|
Fw |
d |
F |
dw |
|
dGT |
0, |
(4.35) |
dx |
dx |
|
dx |
|||||||
|
|
|
dx |
|
|
|
||||
где и w – плотность и |
относительная |
скорость парогазовой |
смеси; |
|||||||
х – расстояние, проходимое потоком по элементам проточной части турбодетандера.
Разделив последнее уравнение на G = F w и введя массовую концен-
трацию новой фазы gТ = GТ / G, получим |
|
|
|
|
|
||||||||||||
|
1 |
|
dF |
|
1 |
|
d |
|
1 |
|
dw |
|
1 |
|
dgT |
0. |
(4.36) |
|
|
|
|
|
|
|
1 gT |
|
|||||||||
|
F dx |
|
dx |
w dx |
|
dx |
|
||||||||||
Последний член уравнения (4.36) отражает изменение концентрации твердой фазы вдоль проточной части детандера.
Вканале соплового аппарата относительная скорость потока совпадает
сабсолютной скоростью. В рабочем колесе такого совпадения нет. Для
106
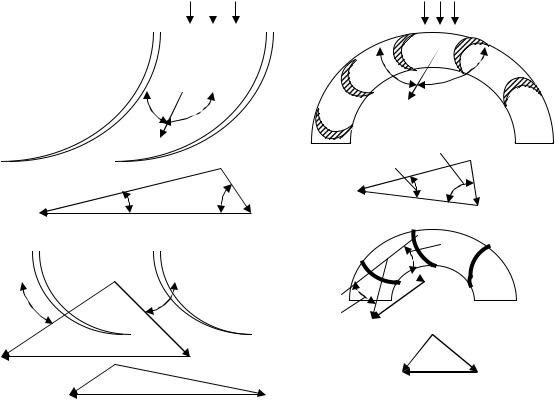
получения одного общего уравнения неразрывности, как для соплового аппарата, так и рабочего колеса, выразим относительную скорость потока в канале рабочего колеса через абсолютную. Для осевого турбодетандера (рис. 4.29, а) из треугольника скоростей в некотором сечении канала рабочего колеса имеем
w u ccos /cos ; |
(4.37) |
cos u w/cos /c; |
(4.38) |
w csin /sin , |
(4.39) |
где с, u – абсолютная и переносная скорости потока; и – углы между векторами скоростей соответственно с и u и w и u.
|
|
|
0 |
|
|
|
c0 0 |
|
|
|
|
c0 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
c w |
|
|||
|
|
|
|
|
|
|
|
|
|
CА |
|||||
|
|
|
c w |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
1 |
1 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
с1 |
|
|
|||
1 |
с1 |
|
|
|
1 |
1 |
|
w1 |
|||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
||||||||
ОЗ |
|
|
|
w |
u1 |
|
|
||||||||
|
|
u |
1 |
|
|
|
1 |
|
|
|
|
|
|||
1’ |
|
|
|
|
|
1’ |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
РК |
|
|
|
|
|
РК |
|||
|
|
|
|
|
|
|
|
c |
|
w |
|||||
2 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
2 |
|
u |
|
|
|
||||||
c |
|
|
|
|
w |
|
|
|
|
c2 |
|
w2 |
|||
u |
|
|
|
|
w2 |
|
|
|
|
||||||
c2 |
u |
|
|
|
|
|
u2 |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
а |
|
|
|
|
|
|
|
|
б |
|
|
Рис. 4.29. Течение парогазовой смеси в ступени осевого (а) и радиального (б) турбодетандеров
Дифференцируя уравнения (4.38) и (4.39) по х, получим
d cos |
1 du |
|
u |
|
dc |
|
cos dw |
|
wcos dc |
|
wsin d |
; (4.40) |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
c dx |
c |
2 |
|
dx |
c dx |
c |
2 |
|
dx |
c |
|
dx |
||||||||||
dx |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
107
dw |
|
sin |
|
dc |
|
ccos sin |
|
d |
|
c |
|
d cos |
. |
(4.41) |
|
|
|
dx |
sin2 |
|
sin tg |
|
|||||||
dx sin |
|
|
|
dx |
|
dx |
||||||||
Подставляя выражения (4.39) и (4.41) в уравнение (4.40) и учитывая, что для осевого турбодетандера изменение окружной скорости на цилиндрической поверхности du = 0, получим
|
|
|
|
|
|
d cos |
E8 |
d |
E9 |
dc |
, |
|
|
(4.42) |
||||||||||
|
|
|
|
|
|
|
|
dx |
|
|
|
|
|
|
|
|
||||||||
где |
|
|
|
|
|
|
|
|
|
|
|
|
dx |
|
|
|
dx |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
sin |
|
|
|
|
|
|
|
|
u |
|
|
E |
|
1 |
1 |
. |
|||||
E |
8 |
sin |
|
|
|
|
|
/ E |
7 |
; |
|
E |
9 |
|
|
|
|
; |
|
7 |
|
|||
|
2 |
|
|
|
|
2 |
|
|
|
|||||||||||||||
|
|
tg |
|
|
|
|
|
|
|
c |
E7 |
|
|
|
|
tg tg |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Для радиального турбодетандера (рис. 4.29, б) треугольники скоростей в некотором сечении канала рабочего колеса подобны треугольникам скоростей осевой машины (см. рис. 4.29, а). Поэтому уравнения (4.37) – (4.39) применимы и для радиального детандера.
Подставляя (4.39) и (4.41) в уравнение (4.40), после несложных преобразований получим для радиального детандера
|
|
d cos |
|
1 |
|
|
du |
|
E8 |
d |
E9 |
dc |
. |
(4.43) |
||
|
|
|
cE7 |
|
|
dx |
|
dx |
|
|||||||
|
|
|
dx |
|
|
|
|
|
dx |
|
||||||
Производная |
d |
находится |
из |
заданного закона изменения |
угла |
|||||||||||
dx |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
вдоль проточной части турбодетандера.
Подставляя (4.37) и (4.39) в (4.36), получим обобщенное неразрывности для осевого и радиального турбодетандеров:
|
d |
|
B |
dc |
B |
dF |
B |
d cos |
B |
d |
B |
dgT |
, |
||
|
dx |
|
dx |
|
dx |
|
|||||||||
|
1 dx |
2 |
3 |
|
dx |
4 |
5 |
dx |
|||||||
где |
cos u ccos ; |
|
c/ u ccos ; |
||||||||||||
|
B1 |
B3 |
|||||||||||||
|
B2 / F ; |
B4 tg ; |
|
B5 / 1 gT . |
|||||||||||
уравнение
(4.44)
Уравнение состояния. При расчете газовых течений в проточной части турбодетандера в области низких давлений и относительно высоких
108

температур, т.е. в области, далеко отстоящей от состояния насыщения, обычно допускают, что поведение газа подчиняется уравнению состояния идеального газа
p RT,
где р и Т – давление и температура газа; R – газовая постоянная.
Иногда применяют модель "идеализированного" газа с учетом постоянного, среднего для рабочей области, коэффициента сжимаемости z:
p z RT.
Однако в области, близкой к состоянию насыщения, поведение реального газа заметно отклоняется от свойств идеального и "идеализированного" газов, и введение постоянного среднего коэффициента сжимаемости может не обеспечить достаточной точности расчетов. Расчет по таблицам и тепловым диаграммам состояния даже на ЭВМ становится громоздкой задачей, так как требуется вводить большое количество числовых данных в память машины. Поэтому наиболее подходящим для расчетов является аналитическое уравнение состояния реального газа.
Наиболее распространенными уравнениями состояния реальных газов являются уравнения Боголюбова-Майера и Битти-Бриджмена. Уравнение Боголюбова-Майера представляет собой наиболее общую форму уравнения с вириальными коэффициентами, позволяющего получить высокую степень точности р - - Т зависимостей. Недостатком этого уравнения является отсутствие пригодной для практического применения методики комбинирования коэффициентов для расчета термических параметров смесей реальных газов.
Уравнение Битти-Бриджмена позволяет с достаточной точностью определить параметры смеси реальных газов в паровой фазе при плотностях ниже критической [11]:
p 2RT 1 1/ B 2 A, |
(4.45) |
здесь А, В, коэффициенты, являющиеся функциями плотности и температуры,
A A 1 ; |
B B 1 ; |
c/T3, |
|
|
0 |
0 |
|
где А0 , , В0 , |
, с – константы, зависящие от свойств веществ. |
||
Константы смесей выражаются через константы уравнения состояния чистых компонентов:
|
|
mi |
|
|
2 |
A0СМ |
|
; |
|||
|
A0i |
||||
|
|
i |
|
|
|
СМ mi i ; |
B0CМ mi B0i ; |
||||
i |
|
|
|
|
i |
109
