
Фармакогностическое изучение растений рода тимьян (Thymus L.) как перспективного источника получения фитопрепаратов
.pdf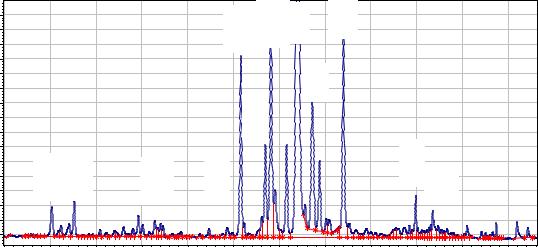
них 7 фенолокислот, 5 оксикоричных кислот, 11 флавоноидных соединений
(таблица 8).
В траве тимьяна Палласа определено 11 фенольных веществ, из них впервые 9: 5 фенолокислот, 2 оксикоричные кислоты, 2 флавоноида; в траве тимьяна мелового определено - 13 (10 из них впервые: 6 фенолокислот, 1 оксикоричная кислота, 3 флавоноидных соединения); в траве тимьяна
ползучего определено - |
14 |
(10 из них |
впервые: 6 фенолокислот, |
3 оксикоричные кислоты, |
1 |
флавоноид); |
в траве тимьяна блошиного |
определено - 14 (7 из них впервые: 6 фенолокислот и 1 флавоноид); в траве тимьяна Маршалла определено - 15 (12 – впервые: 6 фенолокислот, 2 оксикоричные кислоты, 4 флавоноида); в траве тимьяна двуликого определено - 14 (10 – впервые: 6 фенолокислот, 2 оксикоричные кислоты, 2 флавоноида); в траве тимьяна Черняева определено - 12 (12 – впервые: 7 фенолокислот, 4 оксикоричные кислоты, 1 флавоноид).
mAU |
|
|
|
|
|
|
|
|
|
|
|
|
|
330nm,4nm (1.00) |
|
|
|
|
|
|
|
|
|
|
|
|
|
37.5 |
|
|
|
|
|
|
54.890 |
|
56.910 |
|
|
|
|
35.0 |
|
|
|
|
47..720 |
49.000 |
|
|
|
|
|
||
32.5 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
30.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
27.5 |
|
|
|
|
|
|
|
53.500 |
|
|
|
|
|
25.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
22.5 |
|
|
|
|
|
48.390 |
|
|
|
|
|
|
|
20.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
17.5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
15.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
12.5 |
|
|
|
|
|
|
|
|
|
64.810 |
|
|
|
10.0 |
25.080. |
27.530 |
32.920 |
|
44.230 |
|
|
|
|
66.700 |
|
|
|
7.5 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||||||
5.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
2.5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
20.0 |
25.0 |
30.0 |
35.0 |
40.0 |
45.0 |
50.0 |
|
55.0 |
60.0 |
65.0 |
70.0 |
75.0 |
min |
Рисунок 15 – Хроматограмма результатов ВЭЖХ анализа фенольных |
|
||||||||||||
соединений сырья тимьяна мелового |
|
|
|
|
|
|
|
|
|||||
121
|
mAU |
|
|
|
|
|
|
|
|
|
|
|
|
330nm,4nm (1.00) |
|
|
|
|
|
|
|
|
|
|
|
27.5 |
|
|
|
|
|
|
|
|
|
|
|
|
25.0 |
|
|
|
|
48.250 |
51.813 |
53.410 |
56.850 |
|
|
|
|
22.5 |
|
|
|
|
65.500 |
|
|
|
||||
20.0 |
|
|
|
|
|
|
|
|||||
17.5 |
|
|
|
|
|
|
|
|
|
|
|
|
15.0 |
|
|
|
|
|
|
|
|
|
|
|
|
12.5 |
|
|
|
|
|
|
|
|
|
|
|
|
10.0 |
|
|
|
|
|
|
|
|
|
|
|
|
7.5 |
25.018 |
|
34.470 |
|
|
49.510 |
|
|
|
|
|
|
5.0 |
|
|
|
55.250 |
|
|
|
|
|
|||
|
32.860 |
|
|
|
|
|
|
|
||||
2.5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
25.0 |
30.0 |
35.0 |
40.0 |
45.0 |
50.0 |
55.0 |
60.0 |
65.0 |
70.0 |
75.0 |
min |
|
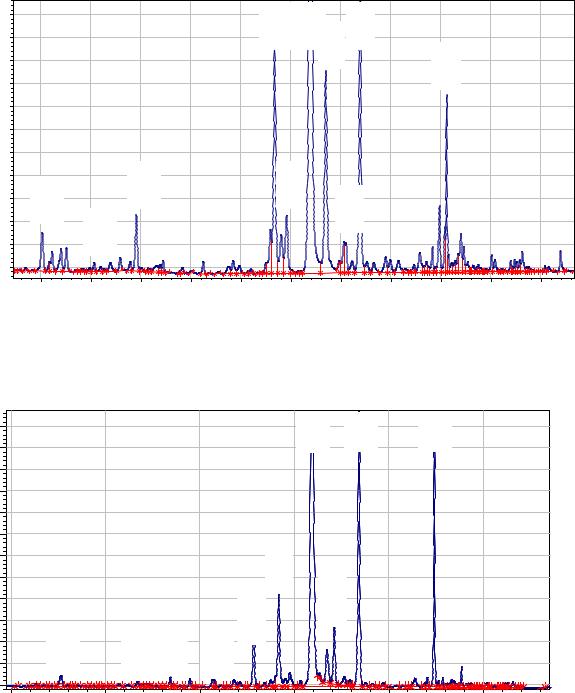
Рисунок 16 – Хроматограмма результатов ВЭЖХ анализа фенольных |
|
||||||||||
|
соединений сырья тимьяна Маршалла |
|
|
|
|
|
|
|
||||
|
mAU |
|
|
|
|
|
|
|
330nm4nm (1.00) |
|
|
|
|
|
|
120 |
|
|
|
51.770 |
56.770 |
64.760 |
|
110 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
90 |
|
|
|
|
|
|
|
80 |
|
|
|
|
|
|
|
70 |
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
|
50 |
|
|
|
48.280 |
|
|
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
54.160 |
|
|
|
|
|
|
48.279 |
|
|
|
30 |
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
25.207018 |
2533.018.910 |
2536.018.800 |
|
|
|
|
|
10 |
41.430 |
|
|
|
|||
|
|
|
|
||||
0 |
|
|
|
|
|
|
|
|
20 |
30 |
40 |
50 |
60 |
70 |
min |
|
Рисунок 17 – Хроматограмма результатов ВЭЖХ анализа фенольных |
||||||
|
соединений сырья тимьяна блошиного |
|
|
|
|||
122
mAU |
|
|
|
|
|
|
|
|
|
|
|
|
|
330nm,4nm (1.00) |
|
|
|
|
|
|
|
|
|
|
|
|
|
30.0 |
|
|
|
|
|
|
51.813 |
|
|
|
|
|
|
27.5 |
|
|
|
|
|
44.010 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
25.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
22.5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
20.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
17.5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
15.0 |
|
|
|
|
|
|
|
55.240 |
56.670 |
|
|
|
|
12.5 |
|
|
|
|
|
|
53.310 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
10.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
7.5 |
25.018 |
|
|
|
|
49.410 |
|
|
|
|
65.100 |
66.800 |
|
5.0 |
|
|
|
44.010 |
|
|
58.130 |
62.510 |
|
||||
2.5 |
|
32.800 |
|
|
|
|
|||||||
|
|
|
|
|
|
||||||||
0.0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
20.0 |
25.0 |
30.0 |
35.0 |
40.0 |
45.0 |
50.0 |
55.0 |
|
60.0 |
|
65.0 |
70.0 |
75.0 min |
|
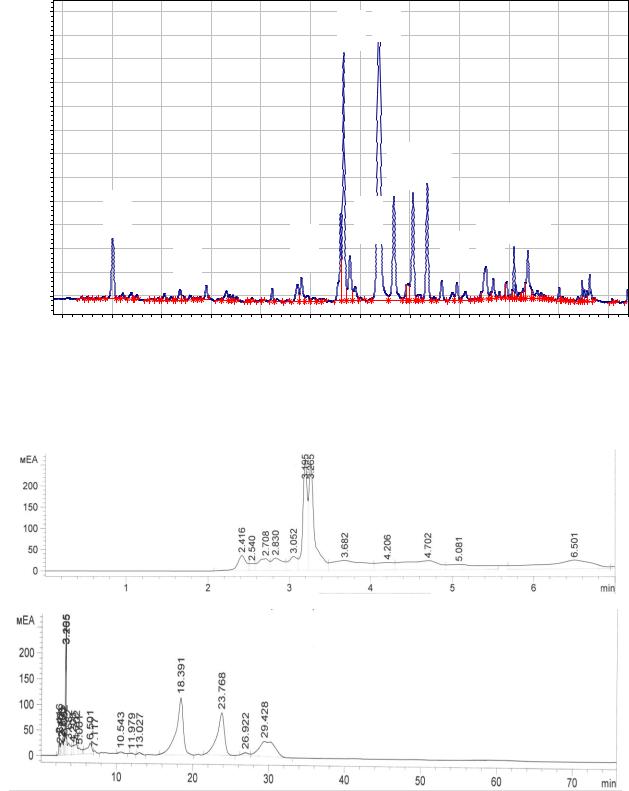
Рисунок 18 – Хроматограмма результатов ВЭЖХ анализа фенольных |
||||||||||||
|
соединений сырья тимьяна двуликого |
|
|
|
|
|
|
|
|
||||
Рисунок 19 – Хроматограмма результатов ВЭЖХ анализа фенольных соединений сырья тимьяна Палласа
123
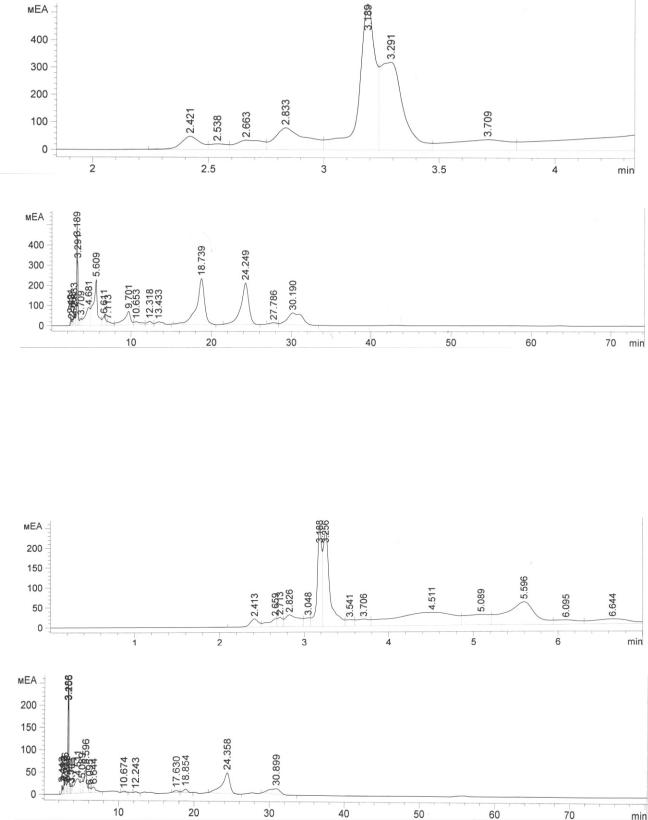
Рисунок 20 – Хроматограмма результатов ВЭЖХ анализа фенольных соединений сырья тимьяна ползучего
Рисунок 21 – Хроматограмма результатов ВЭЖХ анализа фенольных соединений сырья тимьяна Черняева
124
Методами высокоэффективной и газожидкостной хроматографии определено содержание фенольных веществ в исследуемых видах тимьянов.
Подтверждены результаты хроматографического анализа, что из оксикоричных кислот во всех видах преобладает розмариновая кислота. Ее содержание варьирует от 2343,40 мг/кг (тимьян двуликий) до 14351,74 мг/кг (тимьян блошиный). Среди флавоноидов преобладает цинарозид (лютеолин-7-
глюкозид) содержание, которого колеблется от 586,39 мг/кг (тимьян меловой)
до 1564,59 мг/кг (тимьян блошиный). Данные соединения являются маркерами растений рода тимьян и их можно использовать для целей количественного анализа.
3.2.2 Выделение фенольных соединений
С целью подтверждения хроматографического анализа были выделены и исследованы фенольные соединения. Препаративно фенольные соединения выделяли из высушенного растительного сырья (трава), измельченного в порошок вальцеванием с размером частиц менее 1 мм. Для экстрагирования и выделения фенольных веществ перерабатывали от 100,0 г до 1,0 кг сырья растений рода тимьян. Экстракцию сырья проводили спиртом 96%, водно-
спиртовыми смесями и водой очищенной.
Выделение флавоноидных агликонов до и после проведения кислотного
гидролиза
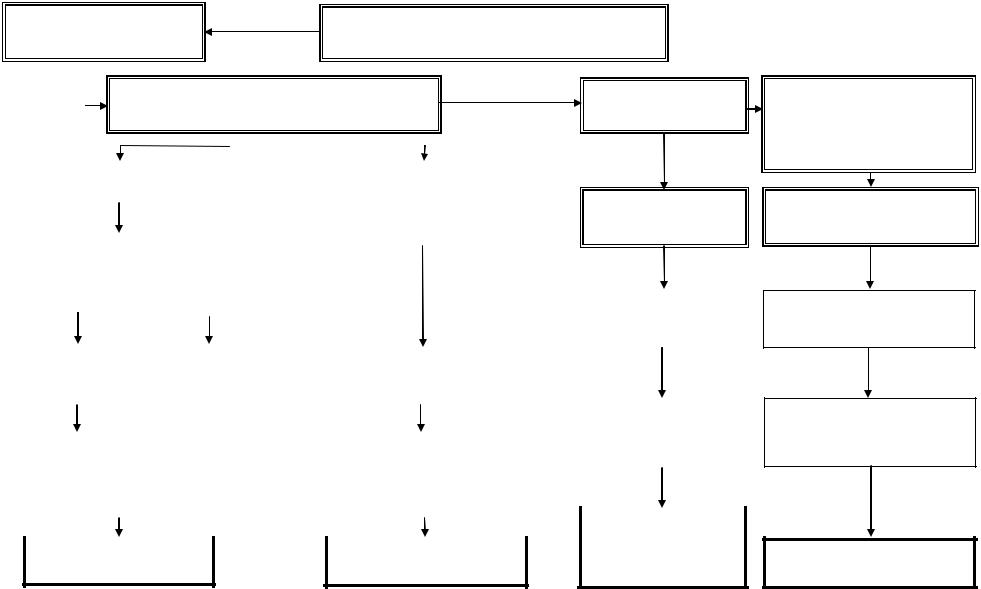
Выделение флавоноидных агликонов до гидролиза проводили на примере травы тимьяна блошиного. Экстракцию флавоноидных агликонов проводили методом фильтрационной экстракции спиртом этиловым 70% из тонкоизмельченного высушенного сырья (300,0 г). Получали 1,8 л извлечения.
Полученное водно-спиртовое извлечение упаривали до водного остатка,
охлаждали, фильтровали. Очищенное водное извлечение обрабатывали 6-ти
125
кратно равными объемами диэтилового эфира. Полученное эфирное извлечение упаривали досуха и использовали для выделения флавоноидных агликонов.
После проведения хроматографии на бумаге в сухом остатке эфирного извлечения были обнаружены вещества 3.10, 3.11, 3.17. Для выделения индивидуальных веществ использовали колоночную хроматографию на полиамидном сорбенте (колонка 2х30 см, полиамидный сорбент в виде суспензии в спирте изопропиловом.
Для этого сухой остаток эфирной фракции (0,36 г) растворяли в 40 мл спирта изопропилового и наносили на подготовленную колонку с полиамидным сорбентом. После того, как раствор осадка войдет в колонку, в
колонку добавляли изопропиловый спирт, которым промывали колонку,
собирая фракции по 50 мл. В полученных фракциях анализировали состав флавоноидов хроматографией на бумаге, которая была импрегнирована формамидом, в системе растворителей: бензол-этилацетат-кислота уксусная
(50:50:1). Во фракциях 7-16 содержались вещества 3.21, 3.20, фракции 17-23 -
вещество 3.20, фракции 23-36 - смесь веществ 3.20 и 3.11, фракции 37-45 -
смесь веществ 3.11, 3.17.
Фракции, в которых содержались индивидуальные вещества (17-23),
объединяли, упаривали в вакууме и кристаллизовали из спирта этилового 50%.
В результате получали вещество 3.20 (86 мг).
Смесь веществ 3.20 и 3.11, 3.11 и 3.17 разделяли, используя повторную хроматографию на колонке с полиамидным сорбентом. Элюэнтом служил хлороформ и смесь хлороформа со спиртом, при увеличении концентрации последнего. В итоге выделили вещества 3.11 (137 мг), 3.17 (98 мг).
Очищенное водное извлечение после отделения агликонов подвергали гидролизу кислотой хлористоводородной 10% в кислоте уксусной 50% в
течение 2-х часов. Полученные агликоны из гидролизатов извлекали эфиром диэтиловым. Эфирное извлечение упаривали досуха и использовали для выделения агликонов после кислотного гидролиза.
126
В составе сухого остатка эфирного извлечения из травы тимьяна блошиного хроматографией на бумаге в системе растворителей бензол-
этилацетат-кислота уксусная (50:50:1), были найдены вещества 3.10 и 3.11. Для их выделения сухой остаток эфирной фракции растворяли в 30 мл спирта метилового, смешивали с 10,0 г полиамидного сорбента, далее сорбент высушивали на воздухе при температуре 22-250С. Для разделения флавоноидных агликонов, полученных после кислотного гидролиза использовали полиамидный сорбент (колонка 2х40 см, суспензия полиамида в хлороформе). Сумму агликонов разделяли, используя смесь хлороформ-спирт этиловый (9:1, 8:2), при этом выделили вещество 3.11 (118 мг) из фракций 5-12
и вещество 3.10 (56 мг) из фракций 16-21.
Выделение оксикоричных кислот и флавоноидных моногликозидов
Для выделения и разделения оксикоричных кислот и флавоноидных гликозидов проводили экстракцию растительного сырья тимьяна двуликого
(500 г) 70% спиртом этиловым методом фильтрационной экстракции.
Полученное водно-спиртовое извлечение (3,0 л) упаривали до водного остатка,
фильтровали для удаления хлорофилла и обрабатывали 6 раз равными объемами этилацетата. Объединенные этилацетатные извлечения упаривали под вакуумом до смолообразного остатка. К полученному остатку приливали минимальное количество спирта метилового при нагревании для растворения.
Полученный раствор быстро охлаждали и смешивали при перемешивании с избытком эфира диэтилового, при этом выпадал осадок, в составе которого хроматографически обнаружены вещества 3.13, 3.17, 3.19, 3.21.
Осадок отделяли и использовали для выделения агликонов и флавоноидных моногликозидов. Разделение обнаруженных веществ осадка проводили хроматографией на колонках с полиамидным сорбентом (диаметр колонки 2,5 смх40 см; суспензия полиамида в спирте этиловом). Полиамидный сорбент смешивали со спиртом этиловым 96% и вносили полученную
127
Водно – спиртовое |
Экстракция |
Трава тимьяна блошиного |
|||||||
извлечение |
|
Спирт |
|
|
|
|
|||
Концентри- |
|
|
этиловый 70% |
|
|
|
|
||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
Водный концентрат |
|
|
|
|
||||
|
|
|
|
Горячей водой |
|||||
рование |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Эфирное извлечение |
|
|
Гидролиз кислотой |
|
|
|
|
||||
|
|
|
|
|
|
|
хлористоводородной 10% в кислоте |
|
|
|
|
||
|
|
|
|
|
|
|
|
Водное |
|
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
уксусной 50 % |
|
извлечение |
|
||
|
|
Хроматография на |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
Концентри- |
||||||
|
|
|
|
|
|
|
|||||||
|
полиамидном сорбенте (элюент |
|
|
|
|
|
|||||||
|
|
|
Диэтиловый |
|
рование |
||||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
изопропиловый спирт) |
|
|
|
|
|
|
|||||
|
|
|
|
эфир |
|
Водный |
|
||||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
концентрат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вещества 3.20- |
|
Вещество |
|
Упаривание эфирного извлечения |
|
|
|
|
||||
3.11, 3,11-3.17 |
|
3.20 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Осаждение (3V) 96% |
|
|
|
|
|
|
|
|
|
|
|
|
|
спирта этилового |
|
|
|
Хроматография на полиамидном |
|
Хроматография на полиамидном |
|
|||||||||
|
|
|
|
|
|
||||||||
|
|
сорбенте (элюент хлороформ, |
|
сорбенте (элюент хлороформ – |
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||||
|
смесь хлороформа со спиртом) |
|
|
спирт этиловый (9:1, 8:2)) |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Водорастворимый |
||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
полисахаридный |
||
|
|
Вещества 3.11, 3.17 |
|
Вещества 3.10, 3.11. |
|
||||||||
|
|
|
|
|
|
|
|||||||
комплекс
Смесь 0,5% растворов кислоты щавелевой и аммония оксалата (1:1)
Кислое извлечение
Концентрирование
Кислый концентрат
Осаждение (5V) 96% спирта этилового
Пектиновый комплекс
Рисунок 22 – А – Выделение фенольных соединений и полисахаридов (схема) из травы тимьяна блошиного
128
|
Трава тимьяна двуликого |
Экстракция спиртом |
Водно – спиртовое |
|
Шрот |
|
|
Шрот |
|
|
|
извлечение |
|
|
|
|
|
||
|
|
этиловым 70 % |
|
|
|
|
|
||
|
|
Концентрирование |
|
|
|
|
Экстракция смесью 0,5% |
||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|||
|
Этилацетатное извлечение |
|
Водный концентрат |
|
Экстракция |
|
|
||
|
|
|
|
|
растворовов кислоты |
||||
|
|
Этилацетат |
|
|
|
горячей водой |
|
|
щавелевой и аммония |
|
|
|
|
|
|
|
|
|
оксалата (1:1) |
|
Концентрирование |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метанольный раст- |
|
|
|
|
|
|
|
Смолообразный остаток |
|
|
Водное извлечение |
|
|
Кислое извлечение |
||
|
этилацетатной фракции |
Растворение в |
вор этилацетатной |
|
|
|
|
|
|
|
фракции |
|
|
|
|
|
|||
|
|
метиловом спирте |
|
|
|
|
|
||
|
|
|
Концентри- |
|
|
|
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Диэтиловый эфир |
|
|
|
|
|||
|
|
|
|
рование |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Осадок
Хроматография на полиамидном сорбенте (элюент спирт этиловый 96% и спирто-водные смеси
5%,10% и т.д.)
Хроматография на бумаге
Вещества |
|
Вещество |
3,12, 3.13 |
|
3.20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Водный концентрат |
|
Кислый концентрат |
|||
|
|
|
|
|
|
|
|
|
|
||||||
Эфирно-метиловый раствор |
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Хроматография на силикагеле |
|
|
Осаждение (3V) 96% |
|
Осаждение (5V) 96% |
||||||||||
(элюент хлороформ, |
|
|
спирта этилового |
|
|
спирта этилового |
|||||||||
хлороформ-спирт этиловый) |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Хроматогра- |
|
|
|
|
|
|
|
|
|||||
|
|
фия на бумаге |
|
|
Водорастворимый |
|
|
Пектиновый комплекс |
|||||||
|
|
|
|
|
|
|
|
|
|
полисахаридный |
|
|
|
|
|
|
Вещество |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
комплекс |
|
|
|
|
||||||
|
|
3.07 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
Хроматография на |
|
|
|
|
|
|||
Вещество |
|
|
|
Вещества |
|
|
|
Вещество |
|
||||||
3.06 |
|
|
3.09,3.06,3.07 |
|
сефадексе (элюэнт вода) |
|
|
3.09 |
|
||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
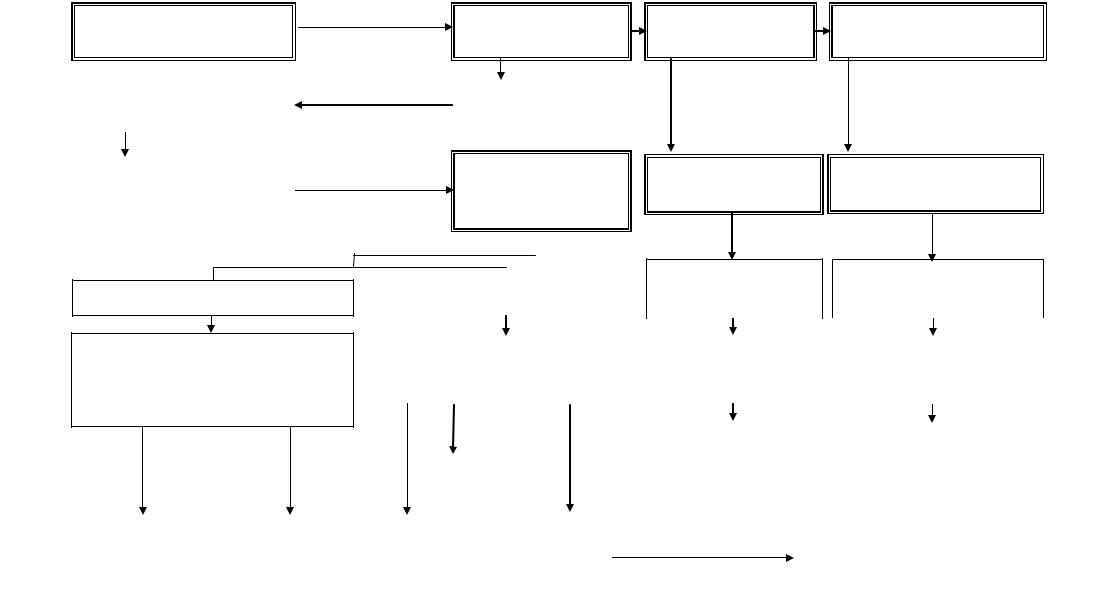
Рисунок 22 – Б – Выделение фенольных соединений и полисахаридов (схема) из травы тимьяна двуликого
129
суспензию в колонку. Далее брали 20 мл спирта этилового 70%, растворяли в нем осадок этилацетатной фракции и полученный раствор смешивали с полиамидным сорбентом (10 г), который высушивали на воздухе. Высушенный с осадком полиамидный сорбент смешивали со спиртом этиловым 96% и
вносили в виде суспензии в подготовленную колонку. Колонку промывали спиртом этиловым 96% и далее спирто-водными смесями (5%, 10% и т.д.).
Собирали фракции по 50 мл. Состав флавоноидов в полученных фракциях анализировали, используя хроматографию на бумаге в системе растворителей:
кислота уксусная 15% и бензол-этилацетат-кислота уксусная (50:50:1) на бумаге, импрегнированной формамидом. Фракции 23-57 содержали смесь веществ 3.12 и 3.13, фракции 61-69 вещество 3.20. Фракции 61-69 объединяли,
упаривали и кристаллизовали из спирта этилового 96%. В результате выделили вещество 3.20 (43 мг). Фракции 23-57, содержащие вещества 3.12 и 3.13
объединяли и использовали для хроматографии на бумаге в системе растворителей кислота уксусная 30%. Пятна веществ 3.12 и 3.13 вырезали,
проводили их элюированием спиртом этиловым 90% и упаривали до минимального объема. В итоге препаративно выделили вещества 3.12 и 3.13.
Эфирно-метанольный раствор, содержащий вещества 3.06, 3.07, 3.08,
использовали для выделения оксикоричных кислот. Для этого упаривали под вакуумом при комнатной температуре для удаления эфира до образования сиропообразного остатка. Полученный остаток смешивали с силикагелем и наносили на подготовленную хроматографическую колонку с силикагелем в хлороформе (высота колонки 50 см, диаметр 4 см). Элюирование вели смесью хлороформ-спирт этиловый 96% в соотношении 90:10, 80:20, собирая фракции по 50 мл. Анализ полученных фракций проводили методом тонкослойной хроматографии на пластинках Sorbfil в системе растворителей: хлороформ-
спирт метиловый-вода очищенная (26:14:3). Фракции 7-18 содержали вещество
3.06, фракции 19-26 смесь веществ 3.06 и 3.07, а начиная с 27 фракции в элюатах появляется вещество 3.09 с примесями веществ 3.06, 3.07.
130
