
Фармакогностическое изучение растений рода тимьян (Thymus L.) как перспективного источника получения фитопрепаратов
.pdf
экстракции определяется целым рядом факторов, в частности измельченностью сырья, температурой экстракции, временем экстракции, типом растворителя,
соотношением сырьѐ-растворитель 198].
Изучение влияния степени измельчѐнности сырья на количественную экстракцию дубильных веществ показало, что максимальное извлечение дубильных веществ из травы тимьяна ползучего достигается при степени измельчения сырья 2,0 мм (таблица 13).
Таблица 13 - Зависимость выхода дубильных веществ от величины измельчѐнности травы тимьяна Маршалла
Степень |
Содержание суммы дубильных веществ, % |
||
измельчѐнности |
Комплексонометрический метод |
Пермангонатометрический метод |
|
сырья, мм |
|||
|
|
||
1 |
8,33 |
12,59 |
|
2 |
13,62 |
15,04 |
|
3 |
8,19 |
10,68 |
|
Литературные данные показывают, что для экстракции дубильных веществ чаще всего в качестве экстрагента применяется кипящая вода очищенная и водно - спиртовые растворы [81, 83]. Для звлечения суммы дубильных веществ, были проведены исследования по выбору оптимального экстрагента.
Таблица 14 - Влияние экстрагента на полноту экстракции дубильных веществ из травы тимьяна Маршалла
Экстрагент |
Содержание суммы дубильных веществ, % |
||
|
|
Комплексонометрический |
Пермангонатометрический |
|
|
метод |
метод |
Спирт этиловый 90% |
4,47 |
9,53 |
|
Спирт этиловый |
6,53 |
12,03 |
|
70% |
|
|
|
Спирт этиловый |
12,09 |
13,33 |
|
50% |
|
|
|
Спирт |
этиловый |
13,62 |
15,04 |
40% |
|
|
|
|
|
|
|
Спирт этиловый 30% |
12,85 |
14,01 |
|
Спирт этиловый |
12,63 |
13,67 |
|
20% |
|
|
|
Вода очищенная |
11,20 |
12,50 |
|
|
|
161 |
|
По результатам проведенных исследований (таблица 14) установлено, что лучшим экстрагентом для дубильных веществ может служить спирт этиловый
40%.
Для экстракции дубильных веществ, применяли экстрагирование до наступления равновесия; при этом экстракцию вели на кипящей водяной бане.
Максимальный выход дубильных веществ наблюдался через 45 минут при соотношении сырье-растворитель 2:250 (таблица 15).
Таблица 15 - Влияние времени экстрагирования на полноту извлечения дубильных веществ из травы тимьяна Маршалла
Время экстракции |
Содержание суммы дубильных веществ, % |
||
|
|
Комплексонометрический |
Пермангонатометрический |
|
|
метод |
метод |
30 |
минут |
8,39 |
9,69 |
45 |
минут |
13,62 |
15,04 |
60 |
минут |
9,34 |
10,70 |
Проведенные нами исследования способствовали разработке методики
количественного определения дубильных веществ в траве растений рода
тимьян.
Методика количественного определения дубильных веществ в траве
растений рода тимьян
К 2,0 г (точная навеска) измельчѐнного до размера частиц 2 мм сырья,
помещенного в колбу объемом 250,0 мл, приливают 250,0 мл спирта этилового
40%. Колбу с содержимым взвешивают на весах с погрешностью ±0,01 г,
соединяют с обратным холодильником. Далее колбу помещают на кипящую водяную баню и выдерживают 45 минут, при этом встряхивают смесь для смывания частиц сырья со стенок колбы. После окончания экстракции колбу охлаждают при комнатной температуре, взвешивают и доводят массу до первоначальной спиртом этиловым 40%. Полученное извлечение, если возникает необходимость фильтруют, при этом отбрасывают первые 10,0 мл фильтрата.
162

10,0 мл полученного извлечения приливают в пробирку для центрифугирования объемом 50,0 мл, добавляют 10,0 мл раствора цинка оксида
1% в аммиачном буферном растворе (реактив осаждения), смесь перемешивают стеклянной палочкой, палочку промывают 5,0 мл воды очищенной, которую присоединяют к основной смеси. По прошествии 30
минут содержимое пробирки центрифугируют 5-10 минут, используя частоту вращения 5-6 тысяч об/мин, сливают жидкость, а к осадку в пробирке приливают 20,0 мл раствора аммиака 0,25%, взмучивают и взвесь присоединяют к центрифугируемой смеси. Промывную жидкость после проведения центрифугирования сливают и отбрасывают. Осадок в пробирке промывают 20,0 мл спирта этилового 96%, а далее его растворяют в 3,0 мл раствора кислоты уксусной 30%. Полученный раствор переносят количественно в колбу объемом 250,0 мл, приливают 100,0 мл воды очищенной, далее жидкость нейтрализуют при помощи 25,0 мл раствора натрия гидрокарбоната 5%, приливают 0,5 мл раствора ксиленового оранжевого и проводят титрование трилоном Б 0,01 (моль/л) до перехода окраски раствора с красно-фиолетовой до желтой.
1,0 мл раствора трилона Б 0,01 (моль\л) соответствует 0,0013 г танина.
Для определения содержания дубильных веществ в абсолютно сухом сырье в процентах (X) используют формулу:
, где
V – объѐм раствора трилона Б, пошедшего на титрование, в миллилитрах;
K – поправка к титру раствора трилона Б 0,01 (моль/л); m – навеска сырья, в граммах;
W – потеря в массе при высушивании сырья в процентах.
Примечание: Приготовление реактива осаждения 1,0 г цинка оксида,
взвешивают с точностью до 0,01 г, помещают в мерную колбу вместимостью
163

100,0 мл, растворяют в смеси 10,0 мл водного раствора аммиака 25% с 2,5 г
аммония хлорида и объем раствора доводят водой очищенной до метки.
Приготовление раствора трилона Б 0,01 (моль/л). 3,9 г трилона Б,
взвешенного с точностью до 0,01 г, растворяют в 250,0 мл воды очищенной,
фильтруют в мерную колбу вместимостью 1,0 л и доводят объем раствора водой очищенной до метки. Титр полученного раствора устанавливают по 0,01 (моль/л) раствора цинка.
Разработанной методикой проанализированы различные образцы растений рода тимьян в сравнении с методом перманганатометрии (таблица 16).
Таблица 16 - Содержание дубильных веществ в растениях рода тимьян
Растение, время |
Содержание дубильных веществ, % |
||
и место сбора |
Пермангонатометрический |
Комплексонометрический |
|
|
|
метод |
метод |
Тимьян Палласа |
14,70 ±0,59 |
9,50±0,39 |
|
Белгородская |
обл. |
|
|
2012 г. |
|
|
|
Тимьян меловой |
13,70±0,59 |
7,60±0,28 |
|
Белгородская |
обл. |
|
|
2011 г. |
|
|
|
Тимьян ползучий |
16,02±0,72 |
11,15±0,48 |
|
Фирма |
|
|
|
«Здоровье»,2011 |
|
|
|
Тимьян блошиный |
22,68±0,30 |
9,10±0,10 |
|
Брянская |
обл. |
|
|
2012 г. |
|
|
|
Тимьян Маршалла |
14,00±0,34 |
8,50±0,02 |
|
Белгородская |
обл. |
|
|
2011 г. |
|
|
|
Тимьян двуликий |
12,04±0,20 |
6,54±0,15 |
|
Курская |
обл. |
|
|
2013г. |
|
|
|
Тимьян Черняева |
12,37±0,22 |
9,34±0,24 |
|
Курская обл. 2014 |
|
|
|
г. |
|
|
|
Содержание дубильных веществ, определѐнное двумя методами показало, что наибольшее содержание дубильных веществ было определено пермангонатометрическим методом (12,04±0,20%-22,68±0,30%), а
комплексонометрический метод, по сравнению с пермангонатометрическим даѐт результаты почти в 2 раза ниже (6,54±0,15%-11,15±%). Указанное
164
расхождение результатов анализа двумя методами можно объяснять различной избирательностью этих методов к дубильным веществам в смеси с сопутствующими веществами. Для того, чтобы показать, что комплексонометрический метод является более объективным в определении дубильных веществ по отношению к пермангонатометрическому, нами было проведено титрование раствором калия перманганата фильтров травы тимьяна Маршалла, полученных после осаждения и отделения дубильных веществ реактивом осаждения. В результате титрования в фильтрате найдено 3,52 %
веществ, не осаждаемых реактивом осаждения. Далее, было интересным исследовать состав центрифугатов после осаждения дубильных веществ в методе комплексонометрии. Получение центрифугаты нейтрализовали кислотой серной до слабокислой реакции и экстрагировали их этилацетатом.
Полученные этилацетатные извлечения и исходные извлечения хроматографировали на бумаге и тонких слоях сорбента в различных системах растворителей. Хроматографический анализ подтвердил, что фенольные соединения (флавоноиды, фенолкарбоновые кислоты, кумарины) остаются в центрифугах и данный метод позволяет определить дубильные вещества в присутствии других фенольных соединений [61].
3.3Тритерпеновые соединения
3.3.1Качественное и количественное изучение тритерпеновых соединений
Результаты качественноего изучения
Результаты качественного определения показали наличие сапонинов во
всех изучаемых растениях на основании (глава 2, раздел 2.2.3) образования
165
белого хлопьевидного осадка при добавлении спиртового раствора холестерина
1% к спиртовому раствору смолообразного остатка бутанольной фракции;
образования малиново-красного окрашивания при прибавлении раствора ванилина 1% в кислоте хлористоводородной к спиртовому раствору бутанольной фракции. В результате реакции Фонтан-Канделя (наблюдали образование пены, которая была равной по объему и стойкости при добавлении к 2-3 каплям водных извлечений из травы исследуемых растений растворов кислоты хлористоводородной (0,1моль/л) и натрия гидроксида (0,1моль/л) и
встряхивании), установили, что сапонины изучаемых растений имеют тритерпеновую природу.
Результаты хроматографического анализа бутанольных фракций водно-
спиртовых и водных извлечений на пластинках Sorbfil в системе растворителей:
хлороформ-этилацетат (5:1) подтвердили наличие в извлечениях из травы растений рода тимьян тритерпеновых соединений (рисунок 22). Со стандартными образцами (фирма «Фитопанацея») в исследуемых извлечениях идентифицированы урсоловая и олеаноловая кислоты. Урсоловая кислота найдена в 6 видах: тимьяне меловом, тимьяне ползучем, тимьяне блошином,
тимьяне Маршалла, тимьяне двуликом, тимьяне Черняева. Олеаноловая кислота в 5 видах: тимьяне Палласа, тимьяне меловом, тимьяне ползучем,
тимьяне Маршалла и тимьяне Черняева.
Количественное изучение тритерпеновых соединений
Фотоэлектроколориметрическое определение тритерпеновых сапонинов
(глава 2, раздел 2.2.3) позволило установить, что их содержание в траве растений рода тимьян колеблется от 0,52±0,02% до 4,62±0,23%, максимальное количество тритерпеновых сапонинов накапливается в траве тимьяна двуликого (4,62±0,23%), тимьяна мелового (2,40±0,11%) и тимьяна Маршалла
(2,10±0,10%) (таблица 5).
166

Rf=0,23
Rf=0,18
А Б В |
Г Д Е Ж |
урсол |
олеано |
|
|||
|
|
овая ловая |
|
Рисунок 48 - Схема
хроматограммы водноспиртовых извлечений из травы растений рода тимьян
А - Т. Палласа Б – Т. меловой В – Т. ползучий
Г – Т. блошиный Д – Т. Маршалла Е - Т. двуликий Ж – Т. Черняева
Система растворителей: хлороформ – этилацетат (5:1)
3.3.2Выделение и исследование тритерпеновых соединений
Всвязи с тем, что тритерпеновые сапонины растений рода тимьян обладают антисклеротическим действием [223] было интересным провести их выделение. Кроме того, представляло интерес подтвердить результаты хроматографического анализа. Примером выделения тритерпеновых соединений из растений рода тимьян является их выделение из травы тимьяна блошиного.
Воздушно-сухую траву тимьяна блошиного (120,0 г) измельчали до размера частиц 2,0 мм и экстрагировали хлороформом в аппарате Сокслета.
Хлороформное извлечение отделяли, упаривали до густого состояния. Далее к густому остатку приливали спирт метиловый для растворения. Полученный метанольный раствор центрифугировали, получали осадок и раствор. Осадок отделяли и многократно перекристаллизовывали из спирта метилового, в
результате получили вещество 3.01. Метанольный раствор упаривали в вакууме досуха и многократно обрабатывали горячим спиртом метиловым.
Полученные метиловым спиртом извлечения объединяли, упаривали до сухого
167

остатка, который многократно перекристаллизовывали из спирта метилового. В
результате получали вещество 3.02 (рисунок 49).
Вещества 3.01 и 3.02 дают положительные реакции Либермана-Бурхарда,
Сальковского, а также реакцию с хлорсульфоновой кислотой [221].
Вещество 3.01 – кристаллический порошок беллого цвета, состава С30Н48О3, Т. пл. 280-2830С.
Максимум поглощения УФ-спектра вещества 3.01 находится при длине волны 310 нм (в кислоте серной).
ЛРС (трава тимьяна блошиного)
Хлороформное
извлечение
Упаривание
Центрифугирование
Осадок |
|
Раствор |
Вещество 3.01 |
|
Вещество 3.02 |
(урсоловая |
|
(олеаноловая |
кислота) |
|
кислота) |
|
|
|
Рисунок 49Схема выделение урсоловой и олеаноловой кислот из травы тимьяна блошиного
168

ИК-спектр вещества 3.01 показывает полосу поглощения при 1714 см-1
(С=0 кислоты), 662,1284 (цис-тризамещения С=С), 1187,1123, 1090, (ОН),
1253,1284,1315,1386,1455 (СН3, СН2, СН), 2870, 2925, 3416 (СН3, СН2, СН), 3694 (ОН) (рисунок 50). Продукт ацетилирования вещества 3.01 показал температуру плавления 284-2860С.
Рисунок 50 – ИК-спектр вещества 3.01
Вещество 3.01 по хроматографической подвижности совпадает с таковой урсоловой кислотой. Таким образом, вещество 3.01 было охарактеризовано как урсоловая кислота [221].
Вещество 3.02 - белый кристаллический порошок белого цвета, состава С30Н48О3. Т. пл. 301-3030С.
Максимум поглощения УФ-спектра вещества 3.02 находится при длине волны 310 нм (в кислоте серной).
В ИК-спектре вещества 3.02 имеется полоса поглощения в области 1714
см -1 (С=0 кислоты), а также полосы поглощения при 1689 см -1, 1620 см -1, 1455
см -1, 1385 см -1, 1272 см -1, 1239 см -1, 1212 см -1, характерные для олеаноловой кислоты (рисунок 51) [221].
169
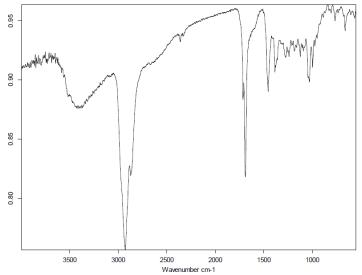
Рисунок 51– ИК-спектр вещества 3.02
Продукт ацетилирования вещества 3.02 показал температуру плавления
260-2610С. Вещество 3.02 по хроматографической подвижности совпадает с таковой олеаноловой кислоты. Таким образом, вещество 3.02 было охарактеризовано как олеаноловая кислота [221].
Урсоловая и олеаноловая из большинства видов выделены впервые: из травы тимьяна Маршалла, тимьяна Палласа, тимьяна блошиного, тимьяна Черняева, тимьяна мелового.
3.4 Исследование жирнокислотного состава
Основой для изучения липофильных веществ, таких как жирные кислоты,
послужило то, что их представители, например полиненасыщенные жирные кислоты: линолевая, линоленовая, арахидоновая относятся к незаменимым факторам питания, т.к. в организме они не синтезируется и должны поступать извне. Эти кислоты по своим биологическим свойствам относятся к жизненно необходимым веществам и называются «Витамины F2». Они нормализуют
170
