
- •Жидкие лекарственные формы часть 2. Неводные растворы, капли, растворы вмс и коллоидные растворы в практике аптек
- •Введение
- •1. Неводные растворы
- •1.1.Неводные растворы как лекарственная форма
- •1.2.Неводные растворители
- •Нелетучие растворители Глицерин (Glycerinum) c3h5(oh) – бесцветная, сиропообразная жидкость, сладкого вкуса, без запаха.
- •1.3. Основные правила изготовления растворов на неводных растворителях
- •1.4. Частная технология неводных растворов Спиртовые растворы
- •Глицериновые растворы
- •Масляные растворы
- •1.5. Основные направления совершенствования качества и технологии неводных растворов
- •Контрольные вопросы
- •Ситуационные задачи с эталонами решений
- •1. В рецепте выписано 120 мл спирта этилового 60%. Как приготовить этот раствор путем разведения спирта этилового 95%?
- •2. Сколько спирта этилового 90% и воды следует взять, чтобы получить 200 мл спирта этилового 40%?
- •Обучающий и контролирующий тест с эталонами ответов
- •1. По массе дозируют:
- •14.Выбирете правильную последовательность технологических операций изготовления раствора борной кислоты на глицерине:
- •15.Выберите правильную технологию изготовления раствора Люголя на глицерине:
- •2. Капли
- •2.1.Капли как лекарственная форма
- •2.2.Основные правила изготовления капель
- •2.3. Калибровка нестандартного каплемера
- •Решение задач по дозированию жидкостей нестандартным каплемером
- •2.4. Частная технология капель
- •Капли для носа (Guttae rhinologicae. Rhinoguttae)
- •Капли ушные (Guttae otologicae. Otoguttae)
- •Капли зубные (Guttae odontalgicae. Odontaguttae)
- •2.5. Случаи нерациональности в прописях капель
- •2.6. Основные направления совершенствования капель
- •Контрольные вопросы
- •2. Студентом по ниже приведенному рецепту:
- •Обучающий и контролирующий тест с эталонами ответов
- •Капли – это:
- •3. Капли обладают всеми достоинствами, присущими жидким лекарственным формам, кроме:
- •5. Наружный диаметр каплеобразующей поверхности стандартного каплемера равен:
- •6. Установите соответствие:
- •7. Правило «2-х цилиндров» заключается в следующем:
- •8. Правило «2-х цилиндров» используется в том случае, если объем капель
- •9.Укажите условия образования эвтектики при смешении 2-х веществ:
- •3. Растворы высокомолекулярных соединений
- •3.1. Характеристика, классификация и номенклатура вмс
- •3.2. Свойства высокомолекулярных соединений
- •3.3. Схема процесса набухания
- •3.4. Общие технологические приемы изготовления ратворов вмс
- •3.5. Изготовление растворов неограниченно набухающих вмс
- •3.6. Изготовление растворов ограниченно набухающих вмс
- •3.7. Случаи несовместимыхсочетаний в прописях растворов высокомолекулярных соединений
- •Контрольные вопросы
- •1. Студентом по ниже приведенному рецепту:
- •2. Студентом по ниже приведенному рецепту:
- •Обучающий и контролирующий тест с эталонами ответов
- •1.Установите соответствие:
- •2.Установите соответствие:
- •3.Укажите свойства вмс:
- •4.Укажите общие технологические приемы изготовления растворов вмс:
- •5.Установите соответствие:
- •4. Коллоидные растворы
- •4.1.Коллоидные растворы как лекарственная форма
- •4.2. Свойства коллоидных систем
- •4.3. Растворы защищенных коллоидов
- •4.4. Растворение препаратов защищенных коллоидов
- •4.5. Фильтрование коллоидых растворов
- •4.6.Частная технология коллоидых растворов
- •4.7. Коллоидные электролиты (полуколлоиды)
- •4.8. Случаи несовместимых сочетаний в прописях растворов коллоидных электролитов
- •Контрольные вопросы
- •1. Студентом по ниже приведенному рецепту:
- •2. Студентом по ниже приведенному рецепту:
- •Обучающий и контролирующий тест с эталонами ответов
- •1.Укажите свойства коллоидных растворов:
- •2.Установите соответствие:
- •3.Для защищенных коллоидов характерна:
- •4.Для ускорения растворения защищенных коллоидов применяют следующие технологические приемы:
- •Литература
- •Приложения
- •Содержание
8. Правило «2-х цилиндров» используется в том случае, если объем капель
А. до 10 мл
Б. до 20 мл
В. до 30 мл
9.Укажите условия образования эвтектики при смешении 2-х веществ:
1. растворимость в друг друге
2. легкоплавкость одного или нескольких веществ
3. высокая криоскопическая постоянная растворителя
4 соответствующее соотношение между взятыми компонентами
5. высокая криоскопическая постоянная растворяемого вещества
Ответ по коду:
А если верно 1,2
В если верно 3,4,5
С если верно 2,3,5
Д если верно 1,2,3,4
Е если верно все
10. Укажите лекарственные вещества, образующие эвтектические смеси:
1. камфора, ментол
2. тимол, хлоралгидрат
3. терпингидрат, салициловая кислота
4. фенилсалицилат, резорцин
5. фенол кристаллический
Ответ по коду:
А если верно 1,2
В если верно 3,4,5
С если верно 1,2,3
Д если верно 1,2,3,4
Е если верно все
3. Растворы высокомолекулярных соединений
3.1. Характеристика, классификация и номенклатура вмс
Высокомолекулярные вещества отличаются большим молекулярным весом и весьма крупными размерами макромолекул, имеющих форму длинных вытянутых или свёрнутых в клубки цепей или сферических глобул. Большинство высокомолекулярных соединений представляют собой аморфные твёрдые стеклообразные или же эластичные каучукоподобные тела. Классификация и номенклатура высокомолекулярных соединений приведена на рис.1.
ВМС
ОРГАНИЧЕСКИЕ
НЕОРГАНИЧЕСКИЕ





ГЛИНЫ БЕНТОНИТЫ СОЕДИНЕНИЯ
СЕРЫ
СИНТЕТИЧЕСКИЕ
ПРИРОДНЫЕ
БЕЛКОВЫЕ СОЕДИНЕНИЯ
НЕБЕЛКОВЫЕ
СОЕДИНЕНИЯ
КАРБОЦЕПНЫЕ
СОЕДИНЕНИЯ
ГЕТЕРОЦЕПНЫЕ
СОЕДИНЕНИЯ
ЭЛЕМЕНТ- ОРГАНИЧЕС-КИЕ
СОЕДИНЕНИЯ
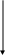
ПЕПСИН ТРИПСИН ЖЕЛАТИН ЛИДАЗА РОНИДАЗА И
Т.Д.
ЦЕЛЛЮЛОЗА КРАХМАЛ
ПОЛИВИНИЛО- ВЫЙ
СПИРТ (пвс)
ПОЛИВИНИЛПИ-РОЛИДОН
(пвп)
МЕТИЛЦЕЛЛЮЛО-ЗА
(мц) КАРБОКСИМЕТИЛ-ЦЕЛЛЮЛОЗА
(кмц) НАТРИЙ-КАРБОКСИМЕТИЛ-ЦЕЛЛЮЛОЗА
(Na-кмц)
ЭСИЛОН
- 4 ЭСИЛОН
- 5
Рис. 1. Классификация и номенклатура высокомолекулярных соединений
3.2. Свойства высокомолекулярных соединений
Высокомолекулярные соединения в фармацевтической технологии используются как в качестве лекарственных (пепсин и др.), так и в качестве вспомогательных веществ (производные целлюлозы, желатин, крахмал и др.)
К ВМС относят обычно соединения с молекулярной массой от нескольких тысяч до миллиона и более. Это гигантские образования, состоящие из сотен или тысяч отдельных атомов, связанных друг с другом силами главных валентностей.
ВМС имеют сферическую (белки) или линейную (МЦ, крахмал и др.) структуру молекулы. ВМС со сферической структурой молекул растворяются в воде подобно низкомолекулярным соединениям. Они легко гидратируются и переходят в раствор, так как дисперсионная связь между такими молекулами невелика. Поскольку стадия набухания этих соединений непосредственно переходит в растворение, их относят к неограниченно набухающим ВМС.
ВМС с линейной структурой молекул имеет нитевидное строение, а длина молекул может достигать 400 – 500 нм, с поперечником 0.3 – 0.4 нм, как, например, в целлюлозе. Такие молекулы очень гибкие, могут свёртываться в спирали или вытянутые цепи. Растворение ВМС протекает в две выраженные стадии: набухание и растворение.
Молекулы воды как наиболее подвижные и имеющие небольшие размеры, диффундируют внутрь ВМС, ориентируются вокруг полярных групп, гидратируют их, образуя молекулярный слой. Ориетировочно каждая карбоксильная группа удерживает 4 молекулы воды, гидроксильная – 3, кето- и альдегидная группы по 2 молекулы воды и т.д. Гидратация полярных групп приводит к ослаблению межмолекулярных связей, разрыхлению соединений. Набухая, ВМС увеличиваются в 10 – 15 раз.
После набухания ВМС связь между их молекулами ослабляется, и они диффундируют в воду (стадия растворения), образуя истинный раствор.
Растворение в воде ВМС со сферической и линейной структурой молекул показано на рис.2.
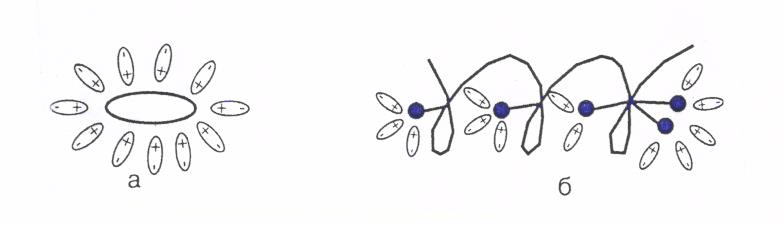
Рис.2. Растворение в воде ВМС со сферической (а) и линейной (б) структурами
Стадия набухания не всегда переходит в стадию растворения, так как ВМС и вода способны смешиваться ограничено, например, желатин и вода при комнатной температуре. После достижения определенной степени набухания процесс прекращается. Однако при изменении условий (нагревании) желатин переходит в раствор.
Таким образом, при ограниченном набухании ВМС поглощает растворитель, а само в нем не растворяется, несмотря на продолжительность контакта. Ограниченное набухание ВМС всегда заканчивается образованием геля. Набухание ВМС носит избирательный характер. Они набухают лишь в жидкостях, которые близки им по химическому строению.
Растворимость ВМС понижается при добавлении этанола, глицерина, электролитов. При добавлении к ВМС солей электролитов возможны явления высаливания и несовместимости. Под действием низких температур и некоторых других факторов возможно так же застудневание или желатирование растворов ВМС, т.е. переход раствора из свободнодисперсного состояния в связнодисперсное (гель), которое сопровождается полной потерей текучести.
Процесс застудневания может продолжаться и в самом геле, который характеризуется явлением «синерезиса» (разделением геля на две фазы и выделением из студня воды). Эти явления необходимо учитывать как при приготовлении, так и при хранении растворов ВМС.
Огромные размеры молекул ВМС определяют своеобразие свойств их растворов. Диффузия в растворах ВМС протекает медленно, они не способны проникать через полупроницаемые мембраны. Эти особенности сближают растворы ВМС и растворы коллоидов, но не позволяют ставить между ними знак равенства. Несмотря на то, что молекулы ВМС не обнаруживаются даже при рассмотрении в ультрамикроскопе, их растворы обладают способностью светорассеивания, приводящей к опалесценции или даже мутности раствора.
Растворы ВМС характеризуются высоким осмотическим давлением, высокой вязкостью и способностью к тиксотропии. Это дает возможность отнести растворы ВМС к структурированным системам.
