
- •Молекула этилена
- •1.2. Гомологический ряд алкенов
- •1.3. Номенклатура алкенов
- •1.4. Изомерия алкенов
- •2. Способы получения алкенов
- •1) Крекинг нефти
- •2) Дегидрогалогенирование алкилгалогенидов
- •3) Дегидратация спиртов
- •4) Дегалогенирование вицинальных дигалогенидов
- •5) Восстановление алкинов
- •3. Свойства алкенов
- •3.1. Физические свойства
- •3.2. Общая характеристика химических свойств
- •3.3. Основные химические реакции
- •1) Реакции присоединения
- •2) Реакции окисления
- •3) Реакции замещения
- •4) Реакции полимеризации
- •4. Основные представители алкенов
- •5. Экологические аспекты химии алкенов
- •Этилен в живой природе
- •Биоразлагаемые полимеры
- •6. Вопросы и задачи по теме «алкены»
- •Литература
2) Реакции окисления
При каталитическом окислении этилена воздухом получается окись этилена (Ткип.=10,50). Метод используется в промышленности:
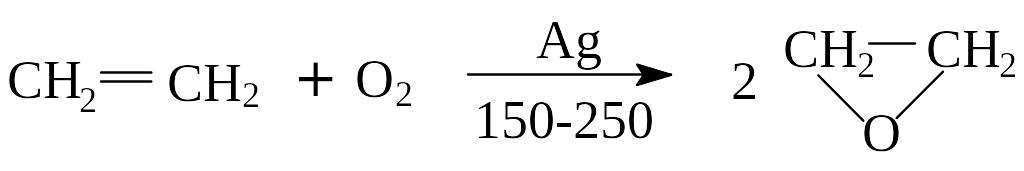
Алкены с перекисью водорода в присутствии катализатора образуют гликоли, двухатомные спирты:
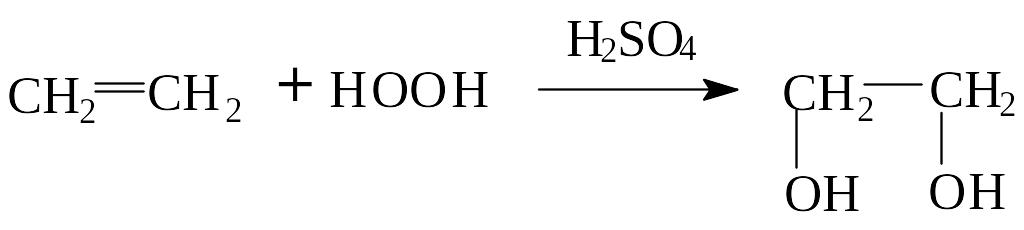
При действии сильных окислителей происходит разрыв молекулы олефина по месту кратной связи с образованием продуктов окисления:
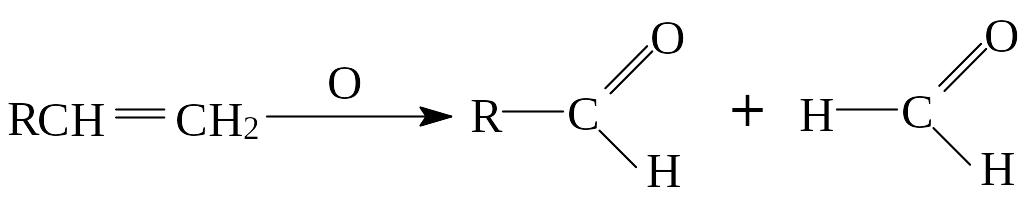
3) Реакции замещения
Алкены, содержащие алкильные группы, вступают в реакции галогенирования с хлором и бромом, которые идут по механизму радикального замещения. Наиболее предпочтительно аллильное замещение. Например,
![]()
4) Реакции полимеризации
Одной из наиболее важных реакций алкенов является реакция полимеризации. При нагревании этилена под давлением с кислородом образуется соединение с большим молекулярным весом около (20000), которое, по существу, является алканом с очень длинной цепью. Это соединение состоит из многих единиц этилена и поэтому называется полиэтиленом. Он известен большинству из нас как материал, из которого делают пленку для упаковки.
Большинство реакций полимеризации алкенов, имеющих промышленное значение, протекают по цепному механизму и могут быть отнесены к анионным, катионным и свободно-радикальным реакциям в зависимости от характера соединения, обусловливающего рост цепи.
Анионная полимеризация
При анионно-цепном механизме полимеризация алкена инициируется атакой нуклеофильного агента по одному из концов двойной связи, что приводит к образованию карбаниона:
У: + СН2=СН2 → У:СН2-СН2:
карбанион
Атака образовавшимся карбанионом другой молекулы алкена приводит к аниону, содержащему четыре углеродных атома: при последующем присоединении карбаниона к молекулам алкена образуется анион более высокого молекулярного веса:
У:СН2-СН2: + СН2=СН2 → У:СН2-СН2-СН2-СН2: →
→ У:СН2-СН2-(СН2-СН2)n-СН2—СН2:
Растущая цепь может оборваться в любой реакции (например, в результате присоединения протона), что приведет к исчезновению анионного центра на конце цепи.
Анионная полимеризация осуществляется легко только для алкенов, замещенных электроноакцепторными группами.
Катионная полимеризация происходит в присутствии серной кислоты. Впервые полимеризацию бутилена наблюдал А.М. Бутлеров. В зависимости от количества кислоты и температуры можно получить димер, тример или полимер. На первой стадии полимеризации протон кислоты присоединяется к алкену, образуя карбониевый катион:
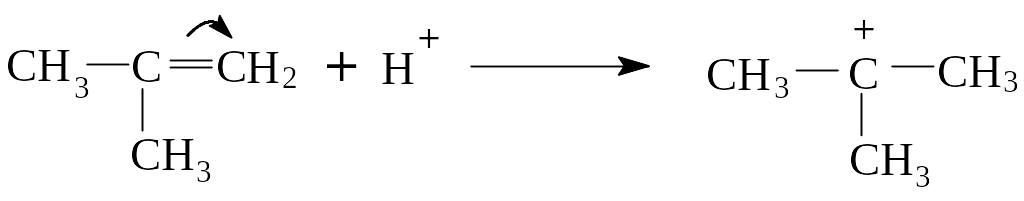
Далее следующая молекула алкена вступает в реакцию за счет электронной пары двойной связи, и образуется катион с более длинной цепью.
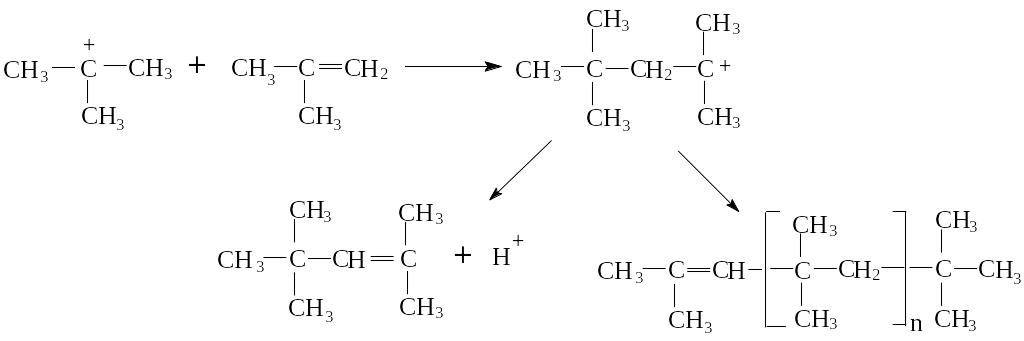
диизобутилен полиизобутилен
Многократное повторение этого процесса может привести к катиону высокого молекулярного веса. Обрыв цепи происходит в результате потери протона.
Катионная полимеризация характерна для замещенных этиленовых углеводородов, поскольку третичные карбкатионы наиболее стабильны.
Свободно-радикальная полимеризация
Этилен может полимеризоваться в присутствии перекиси как катализатора при высоком давлении (1000 атм. и более) и при температуре выше 1000С.
Стадия инициирования цепи состоит в диссоциации органической перекиси на свободные радикалы:
Инициирование: R-O : O-R 2RO.
А рост цепи происходит путем последовательного присоединения радикалов к молекулам этилена:
R-O. +CH2CH2R-O-CH2-CH2-
R-O-CH2-CH2- +n(CH2=CH2)R-O-(-CH2-CH2-)n-CH2-CH2-
Обрыв цепи может быть обусловлен любой реакцией, приводящей к рекомбинации или диспропорционированию свободных радикалов.
Обрыв цепи:
2RO-(-CH2-CH2-)n-CH2-CH2-RO-(CH2-CH2-)n-CH2-CH2-2
RO-(-CH2-CH2-)n-CH=CH+RO-(-CH2-CH2-)n-CH2-CH3
Полиэтилен, получаемый таким образом, содержит в углеводородной цепи 100-1000 звеньев этилена. Пропилен и изобутилен полимеризуются по свободно-радикальному механизму с трудом.
