
- •Строение, номенклатура, изомерия алканов
- •1.2. Характеристика σ – связи
- •1.3. Гомологический ряд алканов
- •1.4. Номенклатура предельных углеводородов
- •1.5. Структурная изомерия алканов
- •1.6. Стереоизомерия (конформационная или поворотная изомерия)
- •2. Способы получения алканов
- •2.1. Промышленные способы получения алканов
- •1) Фракционная перегонка и крекинг нефти.
- •2) Гидрирование угля.
- •2.2. Лабораторные способы получения алканов
- •4) Гидролиз реактива Гриньяра.
- •5) Разложение солей карбоновых кислот.
- •3. Свойства алканов
- •3.1. Физические свойства
- •3.2. Общая характеристика химических свойств
- •3.3. Основные химические реакции
- •1) Галогенирование (реакция металлепсии)
- •2) Нитрование (реакция м.И. Коновалова, 1888 г.)
- •3) Сульфирование
- •4) Сульфохлорирование
- •5) Горение алканов (окисление)
- •4. Отдельные представители алканов
- •5. Экологические аспекты химии алканов
- •6. Вопросы и задачи по теме «алканы»
- •Литература
- •Редактор л.А. Скворцова
1.5. Структурная изомерия алканов
Изомерия - явление, при котором одному и тому же качественному и количественному составу соответствуют несколько соединений, отличающихся друг от друга взаимным расположением атомов, т.е. строением, а следовательно, и свойствами.
Углеводородам с четырьмя и более углеродными атомами свойственно явление структурной изомерии - изомерии углеродного скелета. В ряду алканов формулы изомеров нагляднее всего строить в виде схем углеродного скелета, постепенно наращивая по одному углеродному атому.
Углеродные скелеты трех первых представителей выглядят так:
![]()
Никакого другого порядка химических связей атомов углерода для цепей С1-С3 быть не может.
Для углеводорода с четырьмя углеродными атомами можно построить формулы двух изомеров
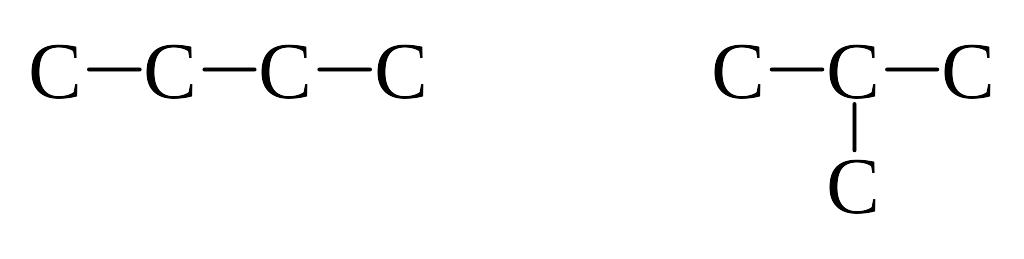
Дополнив схемы нужным числом водородных атомов, получим структурные формулы для двух изомерных алканов:
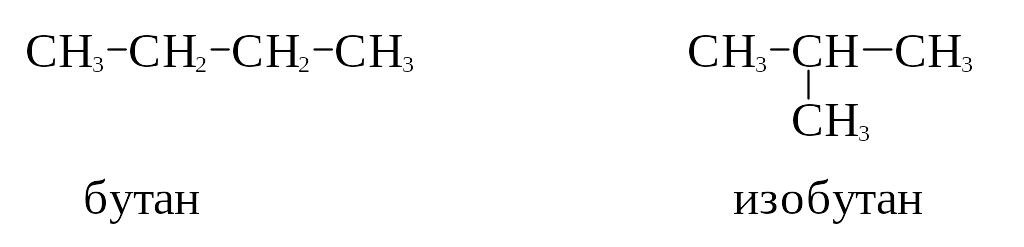
Структурные формулы изображают лишь порядок химической связи атомов, а не их истинное расположение в пространстве или на плоскости (хотя это расположение точно известно). Поэтому представленные ниже формулы отображают одно и то же соединение:
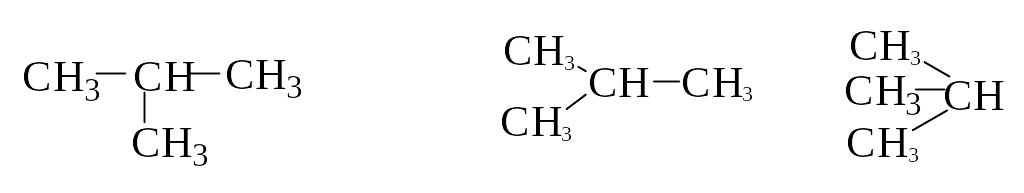
Углеводород с пятью углеродными атомами в молекуле существует в виде трех изомеров:
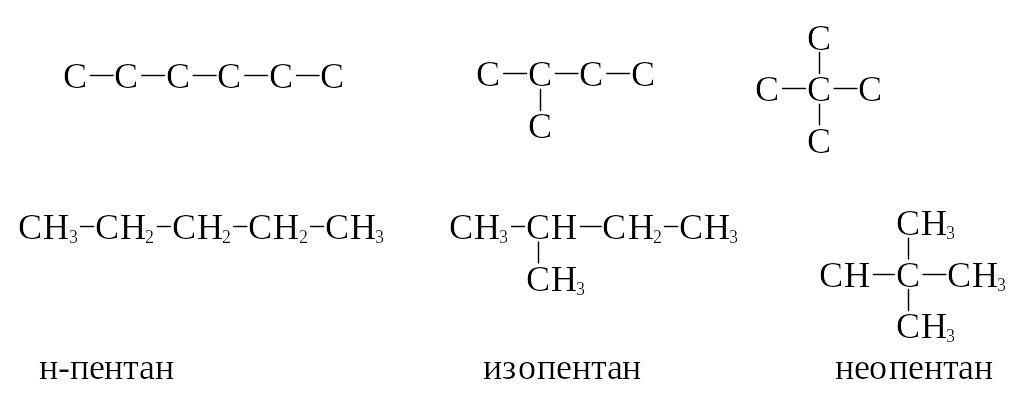
Соединения с неразветвленной углеродной цепью, как, например, бутан, пентан, называют соединениями нормального строения или сокращенно н-углеводородами; если же цепь имеет разветвление, то соединения называют изосоединениями. Приставка изо- используется в названиях соединений, в которых две метильные группы находятся на конце неразветвленной цепи; приставка нео- указывает на наличие трех метильных групп на конце неразветвленной цепи.
Зависимость количества изомеров предельных углеводородов от числа углеродных атомов в молекуле представлена в следующей таблице:
Число углеродных атомов |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
Количество изомеров |
1 |
1 |
1 |
2 |
3 |
5 |
9 |
18 |
25 |
75 |
1.6. Стереоизомерия (конформационная или поворотная изомерия)
В алканах существует свободное вращение вокруг простой углерод-углеродной связи. Различные расположения атомов, которые могут взаимно превращаться друг в друга путем вращения вокруг простых углерод-углеродных связей, называются конформациями.
В этане возможно расположение атомов типа I, в котором атомы водорода находятся друг за другом, и расположение атомов типа II, когда атомы водорода, связанные с одним углеродным атомом, расположены между атомами водорода, связанными с другим атомом углерода. Кроме того, существует неопределенное число промежуточных положений.
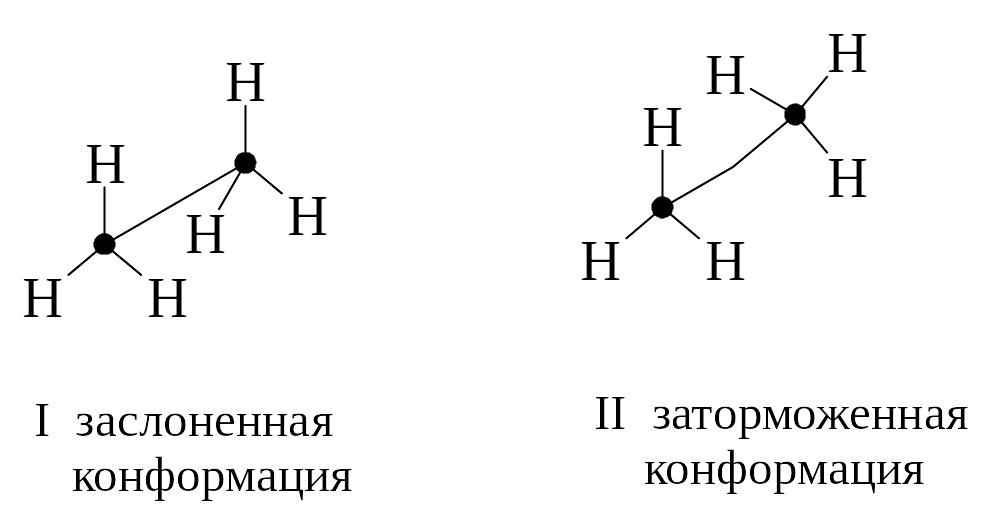
Конформация I называется заслоненной, а конформация II - заторможенной. Промежуточные конформации носят название скошенных. Для изображения различных конформаций удобны так называемые проекции Ньюмена.
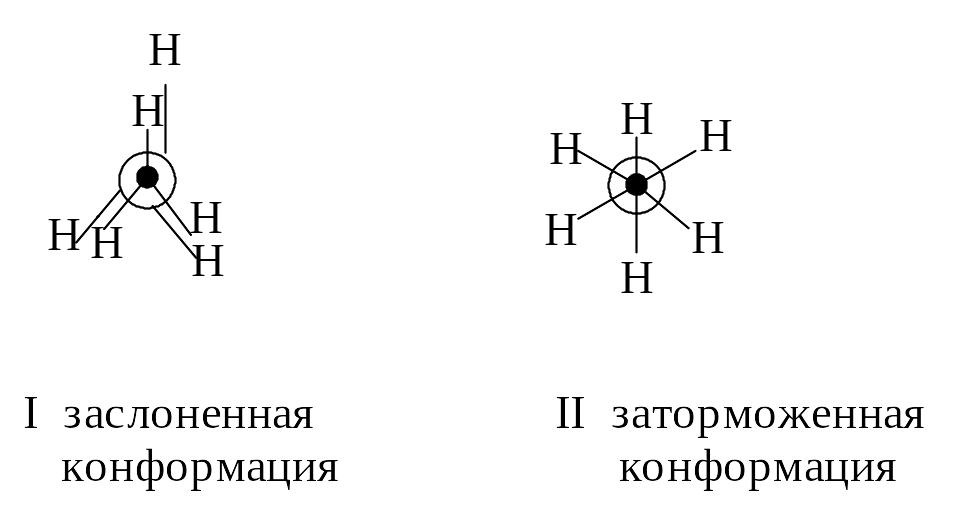
Потенциальная энергия молекулы минимальна для заторможенной конформации. Она возрастает при вращении вокруг углерод-углеродной связи и достигает максимума для заслоненной конформации. Энергия, необходимая для вращения вокруг углерод-углеродной связи, называется торсионной энергией. Фактически различные конформации находятся в динамическом равновесии, и возможность перехода одной заторможенной конформации в другую через заслоненную конформацию определяется барьером вращения, который составляет 3 ккал/моль (12,56103 Дж/моль).
Барьер этот не очень высокий, и считается, что в этане вокруг простой углерод-углеродной связи существует свободное вращение и быстрое взаимопревращение заторможенных конформаций.
При замене атомов водорода в этане на другие атомы или группы атомов возникают иные факторы, влияющие на относительную устойчивость конформеров: вандерваальсовы силы, диполь-дипольные взаимодействия, водородная связь. Но тенденция связей соседних атомов углерода находиться в заторможенной конформации остается, и любое отклонение от заторможенной конформации приводит к появлению торсионного напряжения.
Рассмотрим молекулу н-бутана вдоль связи С2-С3. Молекула аналогична молекуле этана, но у каждого атома углерода один атом водорода замещен на метильную группу. Благодаря наличию метильных групп существует несколько заторможенных конформаций. Существует анти-конформация (I), в которой метильные группы максимально удалены друг от друга (угол 180 0). Существуют две скошенные или гош-конформации (II и III), в которых метильные группы образуют угол 600; они представляют собой несовместимые зеркальные изображения.
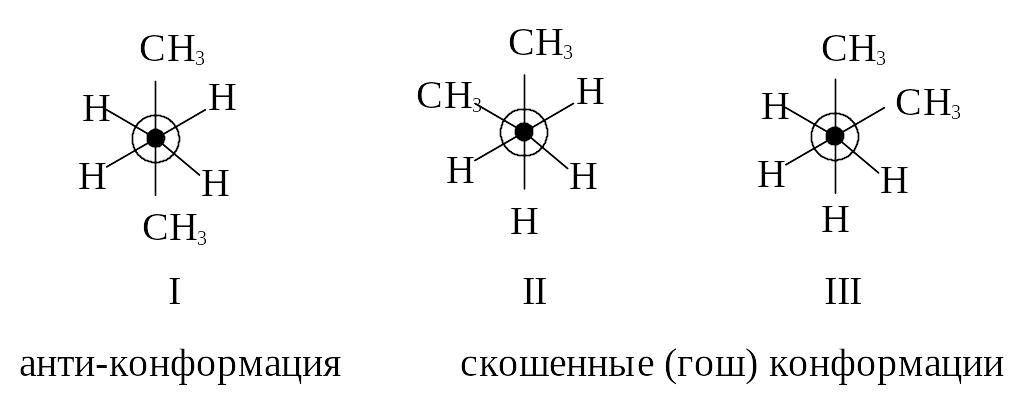
Установлено, что анти-конформация более устойчива (на 0,9 ккал/моль), чем скошенная. В обоих скошенных конформациях торсионное напряжение отсутствует.
