
- •Предисловие
- •Тема 1 общие понятия о химическом производстве
- •1.1. Химическая технология как наука
- •М акрокинетика
- •1.2. Связь химической технологии с другими науками
- •Химическая технология
- •1.3. История отечественной химической технологии
- •Контрольные вопросы
- •Тема 2 компоненты химического производства
- •2.1. Сырье в химическом производстве
- •Химическое сырье, классификация
- •Кларки наиболее распространенных в земной коре элементов
- •2.2. Энергия в химической технологии
- •Энергетические ресурсы
- •2.4. Воздух в химической технологии
- •Химический состав сухого воздуха в приземном слое
- •Структура вредных выбросов промышленности России
- •Контрольные вопросы
- •Тема 3 критерии оценки эффективности химического производства
- •3.1. Технико-экономические показатели (тэп)
- •3.2. Структура экономики химического производства
- •Контрольные вопросы
- •Тема 4 системный подход в изучении химико-техноло-гического процесса
- •4.1. Общие понятия и определения
- •4.2. Химико-технологическая система как объект моделирования
- •4.3. Операторы
- •Типовые технологические операторы
- •4.4. Матричное представление моделей
- •Матрица инценденций
- •Матрица смежности (связи)
- •4.5. Подсистемы хтс
- •4.6. Связи
- •4.7. Классификация технологических схем
- •4.8. Системный подход к разработке технологии производства
- •4.9. Оптимизация производства
- •Контрольные вопросы
- •Тема 5 общие закономерности химических процессов
- •5.1. Понятие о химическом процессе
- •5.2. Классификация химических реакций
- •5.3. Интенсификация гомогенных процессов
- •5.4. Интенсификация гетерогенных процессов
- •5.5. Интенсификация процессов, основанных на необратимых реакциях
- •5.6. Интенсификация процессов, основанных на обратимых реакциях
- •Контрольные вопросы
- •Тема 6 гетерогенный катализ
- •6.1. Общие положения катализа
- •6.2. Процессы абсорбции и хемосорбции в гетерогенном катализе
- •6.3. Механизм гетерогенных каталитических процессов
- •6.4. Основные требования к гетерогенным катализаторам
- •6.5. Основные структурные параметры гетерогенных катализаторов
- •6.6. Технологические свойства гетерогенных катализаторов
- •6.7. Классификация гетерогенных катализаторов
- •6.8. Состав катализаторов
- •6.9. Приготовление катализаторов
- •Контрольные вопросы
- •Тема 7 гомогенный катализ
- •7.1. Кислотный (основной) катализ
- •7.2. Металлокомплексный катализ
- •7.3. Ферментативный катализ
- •Контрольные вопросы
- •Тема 8 химические реакторы
- •8.1. Принципы классификации химических реакторов
- •8.2. Принципы проектирования химических реакторов
- •8.3. Химические реакторы с идеальной структурой потока в изотермическом режиме
- •8.3.3. Примеры аналитического решения математической модели (8.22) и (8.23) для частных случаев.
- •8.4. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения
- •8.5. Конструкции реакторов
- •Контрольные вопросы
- •Тема 9 производство серной кислоты
- •9.1. Способы производства серной кислоты
- •8.2. Сырье процесса
- •8.3. Промышленные процессы получения серной кислоты
- •Влияние параметров процесса на степень превращения so2 в so3
- •9.4. Пути совершенствования сернокислотного производства
- •Динамика использования различных источников сырья
- •Контрольные вопросы
- •Тема 9 производство аммиака
- •10.1. Проблема связанного азота
- •10.2. Получение азота и водорода для синтеза аммиака
- •10.3. Синтез аммиака
- •Контрольные вопросы
- •Тема 11 переработка нефти
- •11.1. Общие сведения о нефти
- •11.2. Классификация нефтей
- •11.3. Состав нефти
- •11.4. Нефтепродукты
- •11.5. Подготовка нефти на нефтепромыслах
- •11.6. Первичная переработка нефти
- •11.7. Пиролиз
- •11.8. Коксование
- •11.9. Каталитический крекинг
- •11.10. Каталитический риформинг
- •11.11. Гидроочистка
- •11.12. Производство нефтяных масел
- •Контрольные вопросы
- •Тема 12 переработка каменного угля
- •12.1. Показатели качества каменных углей
- •12.2. Классификация углей
- •12.3. Коксование каменных углей
- •Коксование
- •Тушение
- •Разгонка
- •12.4. Состав прямого коксового газа и его разделение
- •11.5. Переработка сырого бензола
- •12.6. Переработка каменноугольной смолы
- •12.7. Газификация твердого топлива. Процесс Фишера – Тропша
- •Контрольные вопросы
- •Тема 13 производство стирола
- •13.1. Получение этилбензола
- •13.2. Производство стирола дегидрированием этилбензола
- •13.1.3. Технологическая схема производства стирола дегидрированием этилбензола
- •Контрольные вопросы
- •Тема 14 производство этанола
- •Контрольные вопросы
- •Библиографический список
- •Содержание
- •Тема 5. Общие закономерности химических процессов……………………..54
- •Тема 6. Гетерогенный катализ ……………………………………….................64
- •Тема 7. Гомогенный катализ……………………………………………………93
- •Тема 8. Химические реакторы…………………………………………………101
- •Тема 9. Производство серной кислоты……………………………………….123
- •Тема 10. Производство аммиака………………………………………………137
- •Тема 11. Переработка нефти…………………………………………………...146
- •Тема 12. Переработка каменного угля………………………………………..204
- •Тема 13. Производство стирола……………………………………………….213
- •Тема 14. Производство этанола………………………………………………..218
11.7. Пиролиз
Это наиболее жесткая форма термического крекинга газообразного или жидкого сырья с целью получения низших олефинов (этилена, пропилена, бутиленов), бутадиена и некоторых других продуктов. В зависимости от исходного сырья температура процесса составляет от 700 до 900 оС при времени контакта 0,1–0,5 с и давлении в несколько превышающем атмосферное.
Первое промышленное внедрение процесса пиролиза относится к началу 50-х годов ХХ века, которое было осуществлено почти одновременно в США и СССР. Оно имело своей целью получение этилена. Производительность первых установок пиролиза составляла 30–60 тыс. т. этилена в год. В сере-дине 60-х г.г. обычными стали установки мощностью 100–150 тыс. т/год. Современные установки пиролиза имеют производительность 500–600 тыс. т/год по этилену. В настоящее время мировое производство этилена состав-ляет многие десятки миллионов т/год. Соотношение производства этилена и пропилена составляет 1,8: 1.
Сырьем процесса пиролиза могут служить самые разнообразные углево-дороды и их фракции. Это и индивидуальные алканы (этан, пропан, бутан) и их смеси, а также низкооктановые бензиновые фракции, керосино-газойле-вые фракции и даже нефтяные остатки и сырая нефть. Максимальный выход этилена имеет место при пиролизе этана. В общем случае при выборе источника сырья необходимо принимать во внимание наличие его ресурсов.
11.7.1. Химизм процесса пиролиза. Процесс пиролиза имеет сложный механизм. Протекающие в нем реакции делят на первичные и вторичные.
Первичные реакции – это реакции расщепления (крекинга) парафино-нафтеновых углеводородов, в результате которых образуются непредельные и парафиновые углеводороды с меньшей молекулярной массой, чем у исходного сырья. При пиролизе нафтенов получают также диеновые углеводороды. К продуктам первичных реакций относят этилен, пропилен, метан, этан, а также водород.
Вторичные реакции – это в основном процессы полимеризации и конденсации, в результате которых образуются диены и далее ароматические углеводороды все большей сложности и молекулярной массы. В результате многостадийных последовательных процессов конденсации, полимеризации и ароматизации на стенках реакторов образуются и частично осаждаются также богатые углеродом вещества (содержащие 99,0–99,7 % углерода), такие как пиролизный кокс и сажа. В ходе как первичных, так и вторичных процессов образуется также водород, являющийся продуктом реакций дегидрирования. Реакции пиролиза протекают по радикально-цепному механизму.
Результат таких реакций можно выразить стехиометрическими уравнениями. Ниже приведены подобные уравнения на основе реакций пиролиза н-гексана и циклогексана.
Разложение н-гексана (С6Н14):
Первичные реакции
СН3 – (СН2)4 – СН3 СН3 – СН2 – СН3 + СН2 = СН – СН3; (11.1)
СН3 – (СН2)4 – СН3 СН2 = СН2 + СН3 – (СН2)2 – СН3; (11.2)
СН3 – (СН2)4 – СН3 СН2 = СН – (СН2)3 – СН3 + Н2; (11.3)
СН3 – (СН2)4 – СН3 СН2 = СН – СН2 – СН3 + СН3 – СН3. (11.4)
Далее низкомолекулярные алканы также разлагаются:
СН3 – СН2 – СН3 СН4 + СН2 = СН2; (11.5)
СН3 – СН2 – СН3 СН2 = СН – СН3 + Н2; (11.6)
СН3 – (СН2)2 – СН3 СН2 = СН2 + СН3 – СН3; (11.7)
СН3 – (СН2)2 – СН3 СН2 = СН – СН2 – СН3 + Н2; (11.8)
СН3 – (СН2)2 – СН3 СН2 = СН – СН = СН2 + 2Н2; (11.9)
СН3 – СН3 СН2 = СН2 + Н2. (11.10)
Разложение циклогексана (С6Н12):
Первичные реакции
СН2 = СН – СН = СН2 + СН3 – СН3; (11.11)
СН2 = СН – СН = СН2 + СН2 = СН2 + Н2; (11.12)
 +3Н2.
(11.13)
+3Н2.
(11.13)
Вторичные реакции (общие для обоих углеводородов)
СН2 = СН2 СН СН + Н2; (11.14)
2СН2 = СН2 СН2 = СН – СН = СН2 + Н2; (11.15)
СН2 = СН2 + СН2 = СН – СН = СН2 + 2Н2; (11.16)
2СН2 = СН2 + СН2 = СН – СН = СН2 СН – СН3; (11.17)
СН – СН3 + СН2 = СН2 СН3 – СН2 СН – СН3; (11.18)


СН3 – СН2 СН – СН3 + 3Н2 и т. д. (11.19)
Состав и соотношение конечных продуктов пиролиза определяются со-отношением скоростей реакций при конкретных условиях процесса. Теплота реакций пиролиза, если сырьем является этан, равна 3775 кДж/кг (на прореа-гировавшее сырье). Если сырьем является бензин, то величина теплоты реакции составляет 1130 кДж/кг (на пропущенное сырье). Суммарный порядок реакций пиролиза – первый.
11.7.2. Промышленная реализация процесса пиролиза. Необходимая эффективность процесса в трубчатых печах при работе на бензиновых фракциях достигается при температурах от 840 до 860 оС и времени контакта от 0,3 до 0,5 с. В этих условиях требуемая глубина превращения сырья наблю-дается при высокой тепловой напряженности поверхности радиантных труб (335–378 кДж/ м2 · ч).
На рис. 11.4 представлена технологическая схема промышленной уста-новки пиролиза бензиновых фракций (она отличается от схемы пиролиза га-зообразного сырья тем, что водная промывка газов пиролиза заменена масляной и имеется первичная ректификация).
Описание технологической схемы. Сырье под давлением 1–1,2 МПа по-дают в пароподогреватель 1, где его нагревают до 100 оС и далее смешивают с водяным паром и двумя потоками подают в коллекторы, где потоки развет-вляются на четыре в каждом коллекторе. Пройдя часть труб конвекционной секции печи 2, смесь паров бензина и воды поступает в трубы реакционного змеевика. Пирогаз выходит из печи с температурой 840–850 оС и во избежание пиролитического уплотнения непредельных соединений подвергают быстрому охлаждению (закалке) в «закалочном» аппарате 3, который пред-ставляет собой конденсатор смешения, куда подают водный конденсат. За счет теплоты испарения конденсата температура пиролизных газов снижается на 140–150 оС и достигает 700 оС, что является достаточным, чтобы за не-сколько секунд пребывания газа на участке от «закалочного аппарата 3 до котла-утилизатора 4 прекратились реакции пиролиза. В котле-утилизаторе происходит дальнейшее снижение температуры до 400 оС, его тепло используют для получения пара высокого давления.
10
IV


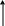
 VI
VII
VI
VII


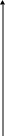 2
3 III
2
3 III

 II
II
 6
6 11 16
6
6 11 16



 IV
IV





 II
4
12
II
4
12



 1
5
1
5
 II
II




 VIII
VIII
IV 9
 I
V
II
I
V
II

 8
8
15

7 IX 13 14
Рис. 11.4. Технологическая схема установки пиролиза бензина
На схеме обозначено: 1, 15 – паровые подогреватели; 2 – трубчатая печь; 3 – «закалочный аппарат; 4 – котел-утилизатор (закалочно-испаритель-ный агрегат); 5 – аппарат масляной промывки пирогаза; 6 – колонны; 7, 13, 14 – насосы; 8 – фильтры; 9, 10 – водяные холодильники; 11 – сепаратор; 12 – отстойник; 16 – отпарная колонна.
I – сырье; II – пар; III – водяной конденсат; IV – вода; V – тяжелое масло; VI – поглотительное масло; VII – газ на очистку; VIII – легкое масло; IX – вода на очистку.
Следующую ступень охлаждения пирогаз проходит в аппарате 5, куда подают тяжелое поглотительное масло. Описанная схема охлаждения входит в печной агрегат, который включает также теплообменник и печь (на схеме не показаны). После аппарата 5 все газовые потоки объединяют в общий поток, и далее схема разделения смолы от пирогаза является общей для всех агрегатов.
После аппарата масляной промывки пирогаза парогазовую смесь направляют в две параллельно работающие колонны 6. В нижней части колонн поток парогазовой смеси отмывают от сажи и кокса тяжелым поглотительным маслом. Этим маслом служит тяжелая пиролизная смола, которая осаждается внизу колонн 6, которую насосом 7 через фильтры 8 и холодильник 9 направляют снова в колонны 6 и аппарат 5. Балансовое количество смолы выводят с установки.
Легкие фракции парогазовой смеси с верха колонн 6 поступают в конденсатор-холодильник 10, где, охладившись до 30–35 оС, разделяются в сепараторе 11 на газ пиролиза, направляемый далее на блок разделения, и обводненный конденсат легкого масла, который отделяют от воды в отстойнике 12. Легкое масло частично возвращают в колонны 6 на орошение, а остальное количество насосом 13 через теплообменник 14 направляют в отпарную колонну 16. Водный слой насосом 14 удаляется с установки на очистку.
Для отпарки из легкого масла газовых компонентов в колонну 16 подают водяной пар. В процессе разделения в колонне 16 выделяют в качестве дистиллята газ, который объединяют с потоком газа, отбираемым из сепаратора 11, и также направляют на блок разделения пирогаза. Очищенное легкое масло выводят из куба колонны 6.
