
Методы диагностики
Клиническая картина НМ очень вариабельна и малоспецифична. Нет ни одного патогномоничного, характерного только для НМ, признака. Диагноз устанавливается на основе сочетания неспецифических клинических критериев.
Диагностические критерии НМ (NYHA, 1964, 1973; Новиков Ю.И., 1981, 1984).
I. Предшествующая инфекция, доказанная клиническими
8
9
и лабораторными данными (включая выделение возбудителя, результаты реакции нейтрализации, связывания комплемента, торможения гемагглютинации, увеличение СОЭ, появление CRP), или другое основное заболевание (лекарственная аллергия и др.).
II. Признаки поражения миокарда.
1. Большие признаки:
патологические изменения на ЭКГ (нарушение реполяри-зации, нарушение проводимости, аритмия);
повышение в крови кардиоспецифических ферментов и изоферментов;
увеличение размеров сердца, подтвержденное данными рентгена и/или эхо-КГ;
застойная СН или кардиогенный шок.
2. Малые признаки:
тахикардия, не соответствующая температуре тела (реже брадикардия);
ослабление I тона сердца;
ритм галопа.
Для постановки диагноза НМ достаточно сочетание предшествующей инфекции с любыми двумя большими или одним большим и двумя малыми признаками поражения миокарда.
Из всех клинических признаков в 100% случаев НМ встречается только один — патологически измененная ЭКГ. Частота остальных зависит от диффузности поражения миокарда, которая определяет тяжесть миокардита.
Электрокардиографические изменения. Изменения ЭКГ при НМ являются неспецифичными. Однако по ценности и объему получаемой информации ведущая роль в диагностике НМ принадлежит именно этому методу (Палеев Н.Р., 1992). НМ сопровождаются ЭКГ-изменениями в 100% случаев, однако полной корреляции между тяжестью изменений миокарда и электрокардиографическими нарушениями нет. Распространенность и глубина изменений миокарда часто бывают значительно большими, чем это можно предполагать на основании ЭКГ.
Характер изменений на ЭКГ при НМ широко варьирует. Наиболее ранними и частыми (не менее 80%) проявлениями миокардиального поражения являются нарушения процессов реполяризации. Раньше всего, с первых дней болезни, появляется депрессия сегмента ST с одновременным уменьшением амплитуды зубца Т. На 2—3-й неделе заболевания формируются отрицательные зубцы Т. Депрессия сегмента ST является кратковременной, чаще всего эту стадию изменений ЭКГ мы не видим из-за поздней госпитализации пациентов.
Длительность указанных нарушений зависит от тяжести НМ. Их локализация может быть самой разнообразной. При вирусном Коксаки В миокардите самые частые и самые выраженные нарушения реполяризации (глубина зубца Т 5г 5 мм) у 75% больных локализуются в области перегородки.
На втором месте по частоте (у 61% больных вирусным НМ) стоит нарушение проводимости: AV-блокады I—III степени, внутрижел уд очковые блокады, вплоть до полной блокады ножек пучка Гиса.
AV-блокады очень характерны и для бактериальных НМ. При дифтерии, например, они по сути являются ключом к диагнозу миокардита.
Существует корреляция между выраженностью нарушений проводимости и степенью тяжести миокардита: AV-бло-када III степени свидетельствует о тяжелом, диффузном НМ.
AV-блокада отличается динамичностью: исчезает у большинства больных по мере лечения, независимо от степени тяжести НМ. Нормализация AV-проводимости происходит в течение 1—4-х недель.
Стойкие нарушения проводимости, особенно если они еще и нарастают, характерны для тяжелых НМ с хроническим рецидивирующим течением. На ранней стадии болезни можно наблюдать неспецифические внутрижелудочковые блокады, в последующем, при рецидивах, иногда в течение 2—3 лет формируется блокада ножек пучка Гиса. Между рецидивами нормализации проводимости не происходит.
Аритмии при вирусном Коксаки В миокардите регистрируются у 30—37% больных. Обычно это желудочковая экстра-
10
11
систолия, реже предсердная. При остром миоперикардите в 8% случаев появляются быстро проходящие эпизоды фибрилляции предсердий. При рецидивирующем течении НМ с развитием атриомегалии, дилатации полостей сердца появляется постоянная фибрилляция предсердий, нарастает желудочковая эктопическая активность вплоть до появления желудочковой тахикардии. У таких больных, как правило, появляются соче-танные тяжелые нарушения ритма и проводимости.
При НМ возможно формирование патологических зубцов Q и QS, что объясняет развитие некоронарогенного некроза миокарда.
С 80-х годов XX века основной упор в диагностике НМ сделан на морфологическое подтверждение диагноза, полученное с помощью эндомиокардиальной биопсии.
Наиболее известны Далласские критерии гистологической диагностики НМ (1986), в рамках которых различают:
Определенный НМ: воспалительная инфильтрация миокарда с некрозом и/или дегенерацией прилегающих миоци-тов, не характерная для ишемических изменений при ИБС.
Вероятный (сомнительный) НМ: воспалительные инфильтраты достаточно редки либо кардиомиоциты инфильтрированы лейкоцитами. Нет участков миоцитонекроза. НМ не может быть диагностирован в отсутствие воспаления.
Отсутствие НМ: нормальный миокард или патологические изменения ткани невоспалительной природы.
Количественные морфологические критерии (Edwards W.D. et al. 1982) заключаются в присутствии более 5 лимфоцитов в поле зрения при увеличении микроскопа в 400 раз.
М. de Z. Higuchi et al. (1990) на основе модификации критериев Далласской классификации и критериев W.D. Edwards предлагают свои гистологические признаки миокардита: присутствие мононуклеарного воспалительного инфильтрата, включающего более 2 близко расположенных к миокардиаль-ному волокну лимфоцитов.
Однако эндомиокардиальная биопсия подтверждает клинический диагноз НМ только в 17—37% случаев, так как высока вероятность забора неизмененного участка миокарда, осо-
бенно в случаях очагового НМ. Поэтому отрицательный результат биопсии не исключает диагноза НМ.
Лабораторная диагностика. При НМ, осложняющих течение инфекционных заболеваний, а также неинфекционных системных процессов, закономерно выявляются признаки активного воспаления: ускоренная СОЭ, С-реактивный протеин, лейкоцитоз, сдвиг лейкоцитарной формулы. Эти же изменения обычно имеют место и при постинфекционных острых НМ с тяжелым течением, при экссудативных миопери-кардитах.
Для хронических и подострых НМ признаки активности воспалительного процесса не характерны.
Лабораторными критериями, подтверждающими миокар-диальное повреждение, является повышение уровней КФК, МВ-КФК, ЛДГ, трансаминаз, тропонинов, выявляемое, однако, не всегда из-за длительности времени от начала заболевания до госпитализации больного. Более длительно (месяцы) может держаться повышенный уровень изоформ ЛДЕ
При проведении иммунологических исследований выявляется повышение уровня иммуноглобулинов IgA и IgG у 50% больных (Гуревич М.А., 1998); ЦИК и ревматоидного фактора — у 44% больных. У 71,4% пациентов отмечено торможение миграции лимфоцитов, средний индекс миграции — 0,58 (при норме 0,8). Снижение миграции лимфоцитов коррелирует со снижением числа Т-лимфоцитов.
Более показателен по сравнению с другими лабораторными тестами, тест дегрануляции базофилов, отражающий процентное содержание дегранулированных форм в периферической крови; в норме оно составляет 10%. Постановка этого теста позволяет подтвердить активный НМ в 82,1% случаев (Мра-вян СР., 1988).
По данным Н.Р. Палеева с соавт. (2001), для больных НМ характерно усиление функциональной активности как Т-, так и В-клеточного звена иммунной системы, которая снижается по мере выздоровления больного или перехода заболевания в ми-окардитический кардиосклероз. С точки зрения диагностики и подбора адекватной терапии, выявленная закономерность име-
12
13
ет большое значение: для людей, заболевших НМ впервые, и на раннем этапе заболевания характерна Т-клеточная активация, переходящая постепенно в В-клеточную активацию, а затем — восстановление нормальных показателей иммунной системы. Для больных с обострением рецидивирующего НМ на раннем этапе характерна одновременно Т- и В-клеточная активация, затем отмечается подавление Т-клеточной активации на фоне сохраняющейся В-клеточной. Далее, по мере выздоровления больного или перехода НМ в миокардиосклероз, происходит постепенное восстановление нормальных показателей экспрессии антигенов лимфоцитами периферической крови.
При НМ повышение экспрессии основных активационных маркеров лимфоцитов периферической крови сопровождается нарушением индукции апоптоза лимфоцитов. Это приводит к нарушению торможения иммунного ответа после элиминации инфекционного антигена из организма, развитию иммунного поражения миокарда (иммунный ответ против антигенов собственных тканей).
Таким образом, иммунологические исследования помогают в диагностике НМ, позволяют отличить от миокардитичес-кого кардиосклероза и подобрать адекватную терапию.
В последние годы для подтверждения диагноза НМ используется радиоизотопная диагностика с радиофармпрепаратами, тройными к воспалению, и проведение магнитно-резонансной томографии сердца с контрастированием для выявления воспалительного отека в миокарде.
Чувствительность и диагностическая точность радиоизотопных методов в диагностике воспалительных заболеваний миокарда колеблется от 85 до 100%. В качестве радиофармпрепаратов используются галлий-67, индий-111, которые обладают аффинностью к нейтрофилам, моноцитам, активированным Т-лимфоцитам и накапливаются в очагах воспаления в миокарде. Наибольшее распространение получила методика мечения лейкоцитов с помощью технеция-99. Однофотонная эмиссионная компьютерная томография с технецием позволяет визуализировать зоны воспаления и некроза, оценить выраженность и протяженность воспалительной инфильтрации,
сделать вывод о наличии кардиосклероза (по результатам изучения перфузии миокарда).
К сожалению, современные методы диагностики НМ, как радиоизотопные, так и иммунологические, мало доступны практическому здравоохранению. Даже эхоКГ еще не стала рутинным методом в клинической практике. Поэтому наиболее важным остается анализ клинической симптоматики, выраженность которой зависит от тяжести НМ.
Клиническая картина и дифференциальная диагностика
I. Легкая форма НМ.
Общепринятых критериев тяжести НМ нет (один из вариантов таких критериев, предложенных в 1999 г., был представлен выше).
К легким формам НМ можно отнести субклинический вариант, который, по данным литературы, встречается почти у 20% больных вирусным НМ. Эти миокардиты не имеют никаких субъективных проявлений и выявляются случайно, например во время вспышки гриппа, когда производится массовое профилактическое ЭКГ-обследование. Либо во время ОРВИ у больного терапевт обнаружит аускультативные симптомы и направит его на ЭКГ-обследование. У таких больных обнаруживаются патологические изменения на ЭКГ.
Но в большинстве случаев причиной обращения к врачу и первой записи ЭКГ у больных являются различные субъективные симптомы, появившиеся на фоне текущей или вскоре после перенесенной инфекции.
Основные жалобы: слабость, очень быстрая утомляемость; кардиалгии, не относящиеся к критериям ИБС; небольшая одышка при физической нагрузке; сердцебиение и перебои в работе сердца.
К объективным признакам легкой формы НМ относятся:
1. Изменения ЭКГ: нарушение реполяризации; AV-блока-да I степени, неспецифические внутрижелудочковые блокады;
14
15
желудочковая экстрасистолия разных градаций по Лауну. Эти изменения динамичны. Нарушения реполяризации и блокады ликвидируются в течение 1—1,5—3 месяцев.
Незначительное повышение кардиоспецифических ферментов (встречается нечасто).
Скрытая сердечная недостаточность, выявляемая инструментальными методами, иногда только во время нагрузки.
Остальные клинические признаки НМ — тахикардия, ослабление I тона сердца — встречаются значительно реже, чем вышеперечисленные. Самым главным признаком легкой формы НМ, отличающим ее от сред нетяжел ой, является отсутствие кардиомегалии и манифестной СН.
Данные эхоКГ могут быть практически нормальными, так же как и лабораторные признаки воспаления: СОЭ, лейкоциты крови, белковые фракции, фибриноген, С-реактивный протеин.
Легкая форма НМ может напоминать нейроциркулятор-ную дистонию, миокардиодистрофию (климактерическую, ти-реотоксическую), с которыми приходится проводить дифференциальную диагностику. Для этого можно сделать ЭКГ-пробы с анаприлином, хлоридом калия. В результате действия этих препаратов у больных нейроциркуляторной дистонией и мио-кардиодистрофией, в отличие от больных НМ, улучшаются процессы реполяризации ЭКГ.
Кроме того, миокардиты вирусной этиологии (Коксаки В, ECHO, грипп) могут сопровождаться экстракардиальными проявлениями (артралгия, артрит, миалгии, сухой плеврит, плевродиния).
Течение легкой формы НМ благоприятное, у абсолютного большинства больных наступает выздоровление. ЭКГ нормализуется в срок от нескольких недель до 3 месяцев. Иногда изменения на ЭКГ держатся до 6 месяцев. Если они наблюдаются более 1 года, диагностируется миокардитический кардиосклероз. Как правило, на ЭКГ сохраняется экстрасистолия.
Однако даже при небольших структурных изменениях миокарда у больных НМ (в том числе и очаговым) возможна внезапная смерть от фибрилляций желудочков или асистолии. На-
блюдающееся в последнее время в ряде европейских стран увеличение частоты внезапной смерти в юношеском и детском возрасте в семьях выходцев из Африки и Азии связывают с ростом заболеваемости НМ. По данным разных авторов, частота легкой формы составляет 46—80%.
II. Среднетяжелая форма НМ диагностируется в тех случаях, когда у больного выявляется кардиомегалия, но отсутствует застойная сердечная недостаточность. Она встречается у 33% больных вирусным миокардитом.
На ЭКГ, кроме изменения сегмента ST, волны Т, нарушения ритма и проводимости, возможно появление быстро проходящего патологического зубца Q. Часто отмечается тахикардия, сохраняющаяся после нормализации температуры тела, ослабленный I тон на верхушке сердца, появление III и IV тонов. Может выслушиваться систолический шум за счет снижения тонуса подклапанных структур. На эхоКГ могут выявляться зоны гипокинезии.
Вирусный миокардит часто сопровождается вовлечением в воспалительный процесс перикарда (миоперикардит). Эти случаи также целесообразно относить к среднетяжелой форме НМ.
У больных с миоперикардитом выражен болевой синдром, который может напоминать ангинозную боль: давящий характер, локализация слева у грудины, иррадиация в левое плечо, необходимость медикаментов для купирования. При выслушивании иногда удается определить шум трения перикарда в III—IV межреберье слева у грудины. На ЭКГ появляются изменения, характерные для перикардита — подъем сегмента ST. В этих случаях приходится проводить дифференциальную диагностику с инфарктом миокарда. Отличают миоперикардит от инфаркта миокарда следующие признаки:
Боль усиливается на вдохе (так как в воспалительный процесс вовлекается находящаяся рядом плевра), часто связана с позой больного (усиливается или ослабевает в определенной позе), отсутствует реакция на нитроглицерин.
Изменения ЭКГ: подъем сегмента ST не имеет очагового характера, скорее диффузный и не сопровождается появле-
16
17
нием патологического зубца Q; форма сегмента ST горизонтальная или вогнутая с переходом в положительный зубец Т; отсутствуют реципрокные изменения, отражающие очаговость поражения, свойственную коронарной патологии. Нет стадийности изменения ЭКГ, характерной для инфаркта миокарда. Имеется ранний признак острого перикардита: депрессия интервала PQ(R) ниже изолинии во II, III отведениях от конечностей.
При вирусных миоперикардитах сегмент ST возвращается к изолинии более быстро, чем у больных перикардитом другой этиологии (туберкулезным, при системных заболеваниях соединительной ткани). Почти у половины больных (у 48% больных миокардитом Коксаки В) динамика сегмента ST завершается в течение первых 3 недель болезни и лишь у отдельных пациентов — в течение нескольких месяцев. У 33% больных миоперикардитом наблюдаются ранние рецидивы перикардита по данным ЭКГ: через 2—4 недели от начала заболевания появляется повторный подъем сегмента ST в тех же отведениях, что и первый, но менее высокий и диффузный, охватывая лишь 2—3 отведения. Снижение сегмента ST происходит медленнее, чем в первый раз.
Индикаторная гиперферментемия при миоперикарди-те в сравнении с коронарной патологией характеризуется меньшей степенью повышения и длительным персистированием в сыворотке, обычно соответствует максимальной активности процесса.
При среднетяжелом НМ могут быть изменения в крови воспалительного характера. С наибольшей постоянностью встречается умеренный лейкоцитоз. Основные показатели острой фазы воспаления изменяются незначительно и менее чем у 50% больных вирусным миокардитом.
Выздоровление при среднетяжелой форме НМ наступает в большинстве случаев, но задерживается до 3 месяцев и более. Считают, что больные с недостаточно выраженным иммунным ответом (с относительно небольшим повышением уровня IgG) характеризуются увеличенным риском развития аутоиммунного хронического НМ.
18
III. Тяжелая форма НМ развивается у больных с диффузным поражением миокарда. Для этих больных кроме кардио-мегалии характерны симптомы застойной сердечной недостаточности с самого начала заболевания.
Кардиомегалия обусловлена не только дилатацией полостей сердца, но и наличием у части больных экссудативного перикардита. Перикардит (сухой и экссудативный) встречается у 80% больных тяжелой формой вирусного миокардита. Частота тяжелой формы НМ, по данным разных авторов, составляет от 12 до 20%.
Изменения сегмента ST и зубца Т на ЭКГ у больных тяжелой формой НМ более диффузные и выраженные, чем у двух предыдущих форм. Часто отмечается глубокий инвертированный зубец Т с амплитудой 5 мм и более. Возможны изменения желудочкового комплекса в виде появления зубца QS. Часто (более чем у половины больных) отмечается низковольтная ЭКГ. Наиболее патогномоничны для тяжелой формы НМ нарушения предсердно-желудочковой проводимости с возникновением синдрома Морганьи—Адамса—Стокса и внутриже-лудочковой — с развитием полной блокады ножек пучка Гиса. Прогрессирование нарушений проводимости совпадает с хроническим рецидивирующим течением НМ. Кроме того, для тяжелой формы НМ характерны упорная тахикардия, глухие тоны сердца, ритм галопа.
На эхоКГ выявляется резко выраженное снижение сократимости левого желудочка сердца, причем часто оно носит не глобальный, а сегментарный характер, что может создать трудности при дифференциальной диагностике с ишемической болезнью сердца. Примерно у 15% больных с тяжелой формой НМ обнаруживают тромбы в левом желудочке, формирование которых связано с сегментарной гипокинезией миокарда и сопутствующим эндокардитом. Возможна дисфункция и дилатация правого желудочка. Тяжелый диффузный НМ может осложняться кардиогенным шоком, формированием хронической аневризмы сердца, тромбоэмболиями.
Воспалительные изменения в крови встречаются у 60% больных тяжелой формой НМ, но их выраженность незначи-
19
тельна. Тяжелая форма НМ может заканчиваться полным выздоровлением, хотя это бывает редко. Более чем у половины больных развивается хроническое течение с летальным исходом в среднем через 5—6,5 лет.
Тяжелый НМ необходимо отличать от дилатационной кар-диомиопатии. При этом надо помнить о частом вовлечении в воспалительный процесс при тяжелом НМ перикарда. В отличие от ДКМП для острого тяжелого НМ характерно несоответствие между резко выраженным снижением контрактиль-ности миокарда и небольшой степенью его дилатации. В настоящее время признается, что большая часть ДКМП является результатом вирусного миокардита.
Определенную роль в возникновении тяжелых НМ с хроническим рецидивирующим течением играют генетические факторы. Так, носительство антигена гистосовместимости HLA-A3 ассоциируется с тяжелой формой вирусного Кокса-ки В миокардита, имеющего хроническое рецидивирующее течение, с прогрессирующим формированием клинически выраженного кардиосклероза. В качестве примера приводим клиническое наблюдение.
Больной К., инженер, в 1995 г. в возрасте 35 лет стал отмечать приступы сердцебиения после алкогольного эксцесса (в анамнезе имелось злоупотребление алкоголем). В ноябре 1996 г. перенес энтеровирус-ную инфекцию с лихорадкой 38—39°С, явлениями гастроэнтероколи-та, по поводу чего обследовался в инфекционной больнице. Из нее переведен в кардиологическое отделение (история болезни № 6279) в связи с развившейся застойной сердечной недостаточностью и изменениями ЭКГ. При поступлении в клинику состояние больного тяжелое. Выявлялась кардиомегалия, сердечная недостаточность стадии На. На ЭКГ: постоянная фибрилляция предсердий, тахисистолическая форма. Элевация сегмента ST в отведениях V,—V6, инвертированная волна TV5 ус(рис. 1).
Холтеровское мониторирование: постоянная фибрилляция предсердий, частая желудочковая экстрасистолия, эпизоды неустойчивой желудочковой тахикардии с частотой желудочкового ритма 160/мин.
ЭхоКГ: дилатация желудочков и предсердий, тромб в левом желудочке. Диффузный гипокинез миокарда, особенно выраженный в
20
межжелудочковой перегородке, фракция выброса — 32%. Митральная регургитация I ст. Выпот в полости перикарда.
Рентгенография грудной клетки: легочные поля воздушны, корни структурны. Сердце увеличено за счет левого желудочка.
Анализ крови: лейкоцитоз — 10,2 • 109/л; АсАТ — 1,15 ммоль/л; АлАТ — 1,08 ммоль/л; альфа-2-глобулины — 17,3%; фибриноген — 5 г/л; С-реактивный белок (+++); повышен уровень IgA.
Диагностирован неревматический (вирусный) миоперикардит, тяжелая форма, декомпенсационный клинический вариант, СН Па, сочетанное нарушение ритма.
Больному проводилось противовоспалительное лечение делаги-лом, ортофеном, преднизолоном, симптоматическое лечение сердечной недостаточности каптоприлом, альдактоном, диуретиками, ди-гоксином, корвитолом, кордароном.
Через 2,5 месяца сердечная недостаточность уменьшилась до I стадии. Исчезли воспалительные изменения в крови.
ЭхоКГ: нормализовались размеры левого предсердия и правых отделов сердца, ликвидировался выпот в полости перикарда. Сохранялся диффузный гипокинез миокарда, фракция выброса — 40%. На ЭКГ: фибрилляция предсердий, эусистолия. Сохраняются реполяри-зационные изменения на передней стенке, верхушке.
Холтеровское мониторирование: исчезла желудочковая тахикардия, экстрасистолия уменьшилась на 50%.
В последующем явления недостаточности кровообращения постепенно прогрессировали, что служило причиной повторных госпитализаций. В 1998 г. после ОРВИ развился рецидив выпотного миоперикардита. На ЭКГ вновь появилась элевация сегмента ST в отведениях V2—V4 и стойко инвертированная волна TV2.V6 С этого года появилась преходящая неполная блокада левой ножки пучка Гиса.
По данным эхоКГ постепенно нарастали размеры полостей правых и левых отделов сердца, фракция выброса снизилась до 20%, сохранялся диффузный гипокинез миокарда.
Рентгенологически с 1998 г. в легких выражены признаки венозного застоя. Корни малоструктурные, широкие, застойные. Сердечная тень большая, расширена за счет всех полостей (КТК = 66%). Тонус миокарда снижен, амплитуда пульсации малая.
Воспалительные изменения в крови (повышение альфа-2-глобулинов, фибриногена, появление С-реактивного белка) и гиперфер-ментемия были выражены незначительно и появлялись только в 1996 и 1998 гг., когда имелись признаки экссудативного перикардита. По-
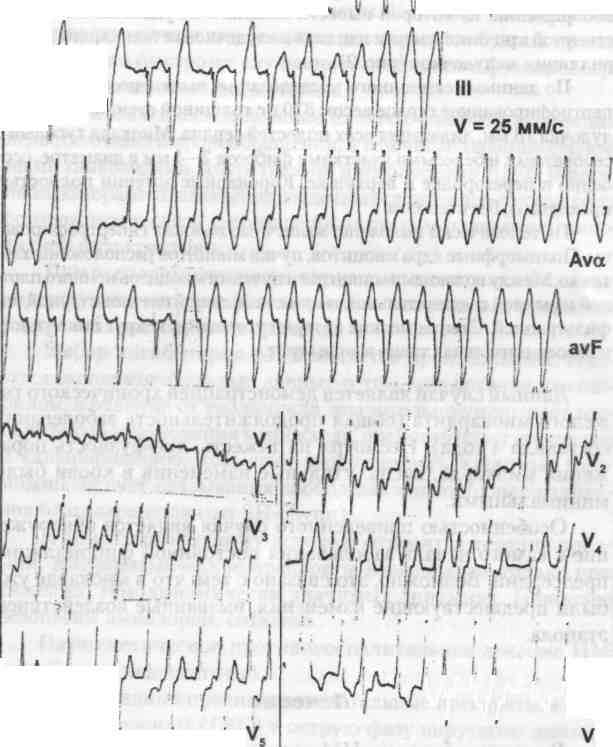
Рис. 2. ЭКГ больного К. от 28.09.2000 г.: V = 25 мм/с, ЧСС - 167/мин, желудочковая тахикардия
22
том, во время всех многочисленных госпитализаций, обнаруживались только лейкоцитоз от 10,2 • 109 до 18,3* 109 с сегментоядерным сдвигом и лимфопения. С 1999 г. у больного появилась гипотония, затруднявшая лечение сердечной недостаточности. С этого года у больного диагностируется дилатационная кардиомиопатия как исход перенесенного миокардита. Последняя госпитализация была в сентябре 2000 г. с терминальной рефрактерной недостаточностью кровообращения, из которой вывести больного не удалось. Непосредственной причиной смерти явились желудочковая тахикардия и фибрилляция желудочков (рис. 2).
По данным секционного исследования, выявлено огромное гипертрофированное сердце весом 870 г с толщиной стенки левого желудочка 18 мм, дилатация всех полостей сердца. Миокард тусклый с сероватыми и белесыми участками фиброза 2—4 мм в диаметре, особенно в перегородке и верхушке. Коронарные артерии полностью проходимы, без стенозов.
Гистологически выявлено: мышечные волокна гипертрофированы. Полиморфные ядра миоцитов, пучки миоцитов расположены хаотично. Между волокнами миоцитов и пучками миоцитов немного плотной и рыхлой соединительной ткани с небольшой гистиоцитарной инфильтрацией. Стенки мелких артерий утолщены, вокруг них — плотная соединительная ткань в виде муфт.
Данный случай является демонстрацией хронического тяжелого миокардита (общая продолжительность заболевания составила 4 года). Несмотря на тяжесть, диффузность поражения миокарда, воспалительные изменения в крови были минимальными.
Особенностью приведенного случая является обнаружение с самого начала заболевания постоянной фибрилляции предсердий. Возможно, это связано с тем, что в миокарде уже были предшествующие изменения, вызванные воздействием этанола.
