
- •Глава 11 Ортопедическое лечение адентии с использованием имплантатов.
- •Глава 12 Челюстно-лицевая ортопедия. 5. К. Kocryp ...... 444
- •Глава 2
- •Глава 3
- •Глава 4
- •Глава 5
- •Глава 6
- •Глава 7
- •Глава 8
- •Глава 9
- •Глава 10
- •Глава 1 1
- •Глава 12
- •Глава 1 3
- •Вадим Николаевич копейкин руководство по ортопедической стоматологии
Глава 1 1
ОРТОПЕДИЧЕСКОЕ ЛЕЧЕНИЕ\^ДЕНТИИ С ИСПОЛЬЗОВАНИЕМ ИМПЛАНТАТОВ
В современной отечественной стоматологической литературе вопросы ортопедического лечения с использованием имплан-татов освещены крайне недостаточно и ограничены в основном представлениями о поднадкостничных имплантатах.
Примерно такой же объем информации содержится в учебниках. Этих сведений, безусловно, недостаточно, для того чтобы выработать правильное отношение к проблеме имплантологии, имеющей свою историю. В нашей стране первое сообщение об имплантации зубов было сделано в 1891 г. Н. Н. Знаменским на IV Пироговском съезде врачей в Москве, где он доложил о приживлении искусственных зубов из фарфора и металла. Некоторый интерес к этим вопросам отмечался в начале нынешнего века [Поляк Я., 1913; Кофман А. И., 1926] и в 50-х годах [Елисеев В. Г., Варес Э. Я., 1956; Мудрый С. П., 1956]. Однако отношение специалистов к имплантологии не изменилось, и только через четверть века возродился интерес к проблеме стоматологической имплантации [Криштаб С. И., Лось В. В., 1985; Чепу-лис С. П. и др., 1984; Амрахов Э. Г., 1985; Паникаровский В. В., Безруков В. М., 1985; Миргазизов М. 3., Олесова В. Н.,1986;
Суров О. Н., 1987; Марков Б. П., 1987; Воробьев В. А. и др., 1987; Матвеева А. И„ 1988; Шевченко В. И., Городецкий А. Н., 1989, и др.].
Большинство работ, опубликованных в 50—60-х годах, посвящено поднадкостничным имплантатам. Негативные результаты операций с поднадкостничными имплантатами привели к идее об использовании внутрикостных конструкций. В США этой проблеме были посвящены работы Strock (1939), Linkou (1966), в Италии Formiggini (1947), во Франции Chercheve (1962), Scialom (1962), в Германии Heinrich (1971), Prucin (1971), Sandhaus (1971), в Швеции Branemark и Breine (1964), Branemark и соавт. (1977).
Новый подход позволил в 70—80-х годах значительно обогатить теорию и практику зубной имплантологии и определить ее роль и место в клинике ортопедической стоматологии. Этому способствовали работы по созданию новых материалов, изучению их биологической совместимости, исследования реакций костной ткани и слизистой оболочки на введение имплантата;
усовершенствование оперативной техники и инструментария;
разработка новых конструкций имплантатов и зубных протезов;
исследования биомеханических закономерностей распределения напряжений в костях; уточнение показаний и противопоказаний к протезированию с использованием имплантатов; создание объективных критериев оценки результатов лечения.
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ИМПЛАНТАЦИИ
Фундаментом имплантологии являются современные представления о реакции организма на введение имплантатов и знание вопросов регенерации. Как известно, замещение тканей и инкапсуляция инородных материалов, получившие название процессов организации, являются частными случаями регенеративных процессов. Конечным исходом процессов организации является рассасывание и замещение инородного субстрата соединительной тканью либо отделение его посредством фиброзной капсулы от окружающих тканей, а также образование спаек, вплоть до зарастания серозных полостей. В отношении инородного тела процесс организации выражается в развитии вокруг него грануляционной ткани, инкапсуляции (образование капсулы вокруг инородного тела). В непосредственной близости от инородных тел из элементов грануляционной ткани иногда образуются гигантские клетки в виде крупных протоплазматических тел с многочисленными ядрами. Они облегают инородные тела, а в отдельных случаях захватывают и фагоцитируют их. Эти клетки принято называть гигантскими клетками инородных тел.
Приведенные закономерности характерны для случаев, когда инородный материал полностью находится внутри тканей и не сообщается с внешней средой. Приемлемы ли они для зубного имплантата, часть которого находится внутри тканей, а часть выступает в полость рта? Как происходит инкапсуляция такого инородного тела? Каковы специфические особенности взаимоотношения зубного имплантата в пограничных зонах имплантат — кость, имплантат — десна, имплантат — полость рта?
Как же происходит защита надкостницы и костной ткани от проникновения бактерий и токсинов из полости рта через поврежденную слизистую оболочку? Такое возможно лишь при условии существования барьерного защитного механизма в пограничной зоне имплантат — мягкие ткани. Познание природы этого механизма является ключевой проблемой имплантологии в стоматологии. По мнению некоторых авторов, существует определенное сходство между строением маргинального пародонта естественных зубов и морфологией тканей, окружающих имплантат в пришеечной области. Оно состоит в наличии эпителиального прикрепления и связи. Впервые мнение о наличии органической связи между эпителием десны и твердыми тканями зубов выдвинул Cottlieb (1921).
Г. Ю. Пакалнс (1970), проводивший гистологическое изучение маргинального пародонта, полностью подтвердил эту концепцию. Более того, автор доказал, что эта связь сохраняется и в старческом возрасте, хотя соотношения тканей маргинального пародонта с тканями зубов изменяются: маргинальный паро-донт располагается на уровне цемента зубов, эпителий органически связан с поверхностью корня зуба, с цементом. Определенная связь существует и между эпителием и имплантатом. Именно она обеспечивает разделение внутриальвео-лярной части имплантата от внеальвеолярной и защиту от проникновения микробов и токсинов. В отсутствие приведенного выше механизма так называемая зубная, или зубопротезная, имплантология была бы нереальной. По-видимому, благодаря этому механизму и происходит своеобразная инкапсуляция внутриа-львеолярной части имплантата.
Mckinney и другие исследователи называют этот процесс биологическим запечатыванием зубного имплантата, мы именуем его пришеечной биологической герметизацией имплантата (ПБГИ). Последняя возможна лишь при опре-
407
деленных условиях, которые в настоящее время еще недостаточно изучены. В те же время отмечена роль ряда факторов, способствующих успешному пройде-нию имплантации: гладкая поверхность пришеечной части имплантата, идадя-щее оперативное вмешательство на слизистой оболочке, безукоризненная гигиена полости рта, правильное положение протезных конструкций по отношению к десневому краю и др. Это позволяет считать, что они имеют значение в биологическом «запечатывании» имплантата.
Немаловажное значение в общем механизме инкапсуляции имплантата имеет характер взаимоотношений в пограничной зоне имплантат — кость, где в зависимости от свойств и структуры материала гистологически могут выявляться три вида основных реакций: дистантный остеогенез, контактный остео-генез и остеогенез с врастанием новообразованной кости в толщу имплантата.
Первый вид реакций связан с процессами образования вокруг имплантата соединительнотканной капсулы, отграничивающей костную ткань от поверхности имплантата. Второй вид характеризуется образованием костной ткани вокруг имплантата, но без проникновения внутрь последнего. Третий вид — так называемый контактный остеогенез — получил название «оссеоинтеграция». Этот вид реакций, по мнению Бранемарка, наблюдается при применении пористых имплантатов. Механизм оссеоинтеграции связан с химическими и биохимическими процессами, происходящими в пограничной зоне имплантат — кость при взаимодействии окисного слоя титана с остеоидной тканью, в котором важную роль играют протеогликаны. При третьем виде реакции наблюдается проникновение костной ткани внутрь имплантата.
Первый вид реакций характерен для имплантатов из сплавов благородных металлов, сплавов кобальта, хрома и молибдена; второй — для непористого титана и его сплавов, углерода, сапфира и др., третий — для биокерамики и гидро-ксилапатита, пористых сплавов. Следует отметить, что на разных поверхностях одного и того же имплантата могут возникать реакции различного характера. Это в первую очередь наблюдается в пористых материалах.
Рассматривая роль протеогликанов в процессах оссеоинтеграции, следует исходить из того, что они вместе с коллагеном образуют основное вещество внеклеточного матрикса соединительной ткани. Протеогликаны представляют собой полианионные молекулы большой массы, содержащие гликозамины, состоящие из гексозаминов и гексуроновых кислот, ковалентно связанные с полипеп-тидным остовом. Наиболее характерное свойство различных протеогликанов состоит в том, что они как полианионы притягивают и прочно связывают катионы во внеклеточном матриксе. Поливалентные катионы (Са2^) обеспечивают агрегацию протеогликанов. Поскольку протеогликаны существуют в тканях в виде агрегатов, то очень важна координация синтеза и компонентов. В настоящее время существует предположение об информационно-регуляторной роли гликозаминогликанов в обмене протеогликанов и клеточной дифференцировке.
Установлена также зависимость качественного и количественного состава компонентов матрикса от нагрузки органа. Например, выявлены значительные различия в качественном составе гликозаминогликанов и интенсивности их обмена в нагруженных и ненагруженных отделах сустава |Slowman, Brand, 1986]. Эти данные позволяют глубже понять различия оссеоинтеграционных процессов, происходящих в нагруженных и ненагруженных имплантатах в период их приживления.
При всей сложности структурных связей имплантата с окружающими тканями эта система является лишь биотехнической моделью натурального паро-донта. Однако их сравнение (табл. 4) позволяет более глубоко проанализировать возможность использования имплантатов, а также их роль и значение при ортопедическом лечении.
408
Таблица 4. Сравнительные данные о морфологии и функции пародонта и его модели имплантат—кость—десна
Сравниваемые
признаки
Пародонт
Общая характеристика
Строение лунки
Характер связи
корня с костью альвеолы
Структура
зубодеснево-го
соединения
Лунка образуется в процессе формирования корня зуба. Внутренняя поверхность стенок альвеол состоит из компактной кости. Здесь находятся многочисленные отверстия,особенно вблизи дна, через которые проходят кровеносные сосуды и нервы
Волокна периодонта с одной стороны переходят в цемент корня, с другой — в альвеолярную кость, образуя связочный аппарат, который состоит из большого числа коллагеновых волокон, собранных в пучки, между которыми располагаются сосуды, нервы, клетки, межклеточное вещество. Основной функцией волокон периодонта является поглощение механической энергии, возникающей при жевании, равномерное распределение ее на костную ткань альвеолы, нервно-рецеп-торный аппарат и микроциркулятор-ное русло периодонта
В норме имеется зубодесневое соединение, структуру которого объясняют по-разному.
Первый вариант объяснения: поверхностные клетки соединительного эпителия имеют гемидесмосомы и связаны с кристаллами апатита поверхности зуба через тонкий зернистый слой органического материала. Второй вариант: между эпителием и поверхностью зуба существует физико-химическая связь. Адгезия эпителиальных клеток к поверхности зуба осуществляется за счет макромолекул десне-вой жидкости
Искусственно созданная биотехническая система, состоящая из биоинертного или биоактивного материала, структурно и функционально вступающая в связь с костной тканью, надкостницей и слизистой оболочкой (биотехническая система имплантат—кость—десна)
В большинстве случаев создается хирургическим путем. Внутренние стенки костного ложа состоят из губчатого вещества, резко отличающегося по механическим свойствам от компактной кости
В зависимости от материала и его структуры, условий приживления возможны следующие виды связей имплантата с окружающей тканью:
корневая часть имплантата окружена соединительнотканной капсулой;
соединительная ткань проникает в поверхностный слой имплантата;
костная ткань и имплантат образуют соединение по типу анкилоза на небольшом расстоянии от поверхности имплантата; костная ткань и имплантат образуют анкилоз за счет прорастания тканей всей толщины имплантата
Существует мнение о возможности образования эпителиального прикрепления в пришеечной области имплантата. Гемидесмосомы обнаружены в пограничной зоне имплантат—десна при применении зубных имплантатов из виталиума, титана, карбона, эпоксидной смолы, сапфира. Есть данные о том, что эта тонкая структура формируется в течение 48 ч после имплантации (Swope и James). Закономерности формирования эпителиального прикрепления и его надежность как биологического барьера нуждаются в дальнейшем изучении
Функции пародонта:
барьерная
Барьерная функция тканей, окружающих имплантат и вступающих с ним во взаимодействие, существует, поскольку способность эпителия десны к ороговению сохраняется, тургор десны имеется, мукополиса-хариды соединительнотканных образований в зоне около имплантата выявляются, эпителиальное прикрепление существует, антибактериальная функция слюны не нарушается, лаброциты и плазматические клетки встречаются
409
Продолжение гоблу 4
Сравниваемые
признаки
Пародонт
трофическая
рефлекторная
регуляция жевательного давления
пластическая
амортизирующая
Трофическая функция пародонта состоит в обеспечении нормального питания и обмена веществ в тканях за счет ней-рогуморальных механизмов, где капилляр с участком контактирующей с ним ткани рассматривается как структурная и функциональная единица трофики тканей
Осуществляется за счет многочисленных нервных окончаний, имеющихся в пародонте. Раздражение рецепторов передается по разнообразным рефлекторным магистралям
Пластическая функция пародонта заключается в постоянном воссоздании его тканей, утраченных в ходе физиологических или патологических процессов.
Выполняют эту функцию цементо- и остеобласты. Определенную роль играют и другие клеточные элементы: фиб-робласты, лаброциты, а также состояние транскапиллярного обмена
Амортизирующая функция пародонта состоит в ослаблении и смягчении жевательного давления и защите от травмы тканей зубной альвеолы сосудов и нервов периодонта.
Она обеспечивается за счет физико-механических свойств волокон периодонта, жидкого содержимого и коллагенов межтканевых щелей и клеток, а также изменения объема сосудов
Трофическая функция тканей, связанных с имплантатом, резко отличается от трофической функции пародонта. Она обеспечивается системой кровоснабжения и иннервации костной ткани и десны
Следует полагать, что рефлекторная регуляция жевательного давления тканями, окружающими имплантат, существует, но снижена, поскольку отсутствует периодонт с его рецеп-торным аппаратом. Однако нервные сплетения, находящиеся в костной ткани, могут участвовать в выполнении этой функции. Это положение нуждается в проверке
Пластическая функция тканей, окружающих имплантат, сохранена. Остеобласты обнаруживаются в костной ткани, прилегающей к им-плантату
Амортизирующая функция тканей, окружающих имплантат, практически отсутствует, ее можно создать лишь искусственно путем введения в конструкцию имплантата амортизаторов. Некоторую амортизирующую функцию приписывают соеди-нительнотканной капсуле, окружающей имплантат, но роль ее в этом процессе ничтожна
Примечание. Данные по морфологии и функции пародонта приведены по В. С. Иванову (1981),
ОСОБЕННОСТИ ОБСЛЕДОВАНИЯ БОЛЬНЫХ
Проводя обследование больных по традиционной схеме (жалобы, анамнез, осмотр, пальпация, перкуссия и лабораторно-инструментальные исследования), необходимо обратить внимание на следующие особенности. Опрос больных следует сочетать с анкетированием, которое позволит получить ответы на вопросы, имеющие первостепенное значение для определения общих показаний и противопоказаний к имплантации. Так, может быть предложена следующая схема опроса пациентов.
410
Ф. И. О.
Возраст
Домашний адрес, телефон
Имеется ли у Вас наследственная отягощенность? да, нет
Перенесенные заболевания
Имеются ли заболевания опорно-двигательного аппарата,
кроветворной или эндокринной систем?
Болели ли вирусным гепатитом когда
Измеряли ли уровень сахара почему
Бывают ли боли в области сердца
Бывают ли гнойные воспалительные процессы на лице
Кровоточат ли у Вас десны
Зубы подвижны или нет
Как давно Вы это заметили
Как заживают раны, порезы
Отмечается ли сухость во рту
Когда Вам удалили последний зуб
Какова причина удаления (кариес, заболевание пародонта, травма, другие причины)
Как перенесли удаление зубов
Как протекает менструальный цикл
Имеется ли у Вас повышенная чувствительность к лекарствам
Связана ли работа с действием профессиональных вредностей да, нет
Нет ли у Вас привычки скрежетать зубами, особенно ночью да, нет
Пользовались ли ранее зубными протезами (съемными, несъемными) да, нет
С особенностями ортопедического лечения с применением зубных протезов на имплантате ознакомлен. Обязуюсь выполнять все предписания врача. Даю согласие на ортопедическое лечение с применением имплантации (Подпись)
Заключительную часть анкеты заполняют после окончания обследования и установления возможности осуществления.
На основании данных анкеты и последующего обследования можно определить общее состояние организма больного и возможную реакцию на имплантат. Если этих данных окажется недостаточно, то следует направить больного на консультацию к соответствующим специалистам. Несомненно, большую помощь окажет заключение участкового терапевта или семейного врача о состоянии здоровья больного.
При осмотре зубов и рта следует обратить особое внимание на признаки заболеваний, признанных имплантологами абсолютными или относительными противопоказаниями к имплантации. К ним относят генерализованный пародон-тит или пародонтоз, выраженную деформацию окклюзионной поверхности зубного ряда, макроглоссию, заболевания слизистой оболочки полости рта, новообразования, дефекты челюстных костей после перенесенного остеомиелита, дисфункцию височно-нижнечелюстного сустава и др.
Из инструментально-лабораторных исследований зубочелюстной системы обязательными являются обзорная рентгенография, ортопантомография или телерентгенография лицевого черепа. Снимки должны быть получены в стандартных условиях и пригодны для проведения измерений с целью определения вертикальных размеров от альвеолярного гребня до носовой полости и верхнечелюстных пазух на верхней челюсти и до нижнечелюстного канала—на нижней.
Ряд методов исследования используют для оценки функционирования имплантатов: пробу Шиллера — Писарева для оценки состояния десны у оставшихся зубов и вокруг имплантата — измерение глубины десневой бороздки у имплантата; измерение количества десневой жидкости с подсчетом количества лейкоцитов.
411
С целью оценки функционирования имплантатов применяют также рентгенологические методы. Снимки получают сразу после имплантации, через 3, 6 и 12 мес, а затем через год при динамическом наблюдении за больными. Оценка имплантатов может быть осуществлена с помощью показателей функционирования имплантата (ПФИ) [Миргазизов М. 3., 1984]:
1 — имплантат неподвижен или подвижен в пределах физиологической податливости тканей, воспаление десны и костный карман отсутствуют;
0,75 — наблюдается периодически возникающая подвижность имплантата I—II степени, появление и исчезновение воспаления десны, костный карман отсутствует (стадия компенсации);
0,5 — постоянная подвижность имплантата I—II степени, образование костного кармана (стадия субкомпенсации);
0,25 — подвижность имплантата 111 степени, выраженный костный карман (стадия декомпенсации);
О — полное исчезновение окружающей имплантат костной ткани и выталкивание его из челюсти траву ляц^ями. 4
Пользуясь этими показателями, можно оценить эффективность имплантаций, а также сроки функционирования тех или иных имплантатов при ортопедическом лечении. Так, поданным В. Н. Олесовой (1986), при применении двухмоментной методики имплантации цилиндрических имплантатов из титана в качестве дистальной опоры мостовидного протеза через 2 года показатели функционирования имплантатов 1—0,75 установлены у 83,4%, 0,5—у 16,6% больных. Отторжение имплантатов (показатель равен 0) произошло у 5,8% больных.
Кроме перечисленных методов исследования зубочелюстной системы, при протезировании больных с использованием имплантатов широко используют изучение диагностических моделей челюстей, которое позволяет оценить характер окклюзионных взаимоотношений зубных рядов, а также уточнить конструкцию имплантата и протеза.
ПРОТИВОПОКАЗАНИЯ И ПОКАЗАНИЯ
Современный уровень стоматологической имплантологии ограничен, к сожалению, очень узким кругом показаний к проведению ортопедического лечения больных с использованием имплантатов. В связи с этим желание многих больных иметь несъемные зубные протезы вместо съемных или улучшить фиксацию съемных протезов за счет имплантатов очень часто не совпадает с возможностями метода. Когда говорят об успешном лечении 80—90% больных, создается впечатление о широком применении имплантатов. Однако следует помнить, что этот показатель вычислен по отношению к больным, не имевшим противопоказаний к применению данного метода. Как только круг противопоказаний сужается, а круг показаний расширяется, процент успеха сразу резко снижается.
В имплантологии противопоказания принято делить на общие и местные. К общим относят болезни сердечно-сосудистой системы, крови, печени (цирроз), почек (хроническая почечная недостаточность) заболевания нервно-психической сферы, инфекционные, аллергию, новообразования, иммунопатологические состояния и др. В группу местных противопоказаний включают болезни слизистой оболочки полости рта, остеомиелит челюстных костей, заболевания височно-нижнечелюстного сустава, невралгические заболевания, выраженные аномалии прикуса, макроглоссию, парафункции, неблагоприятные анатомо-топографические условия, состояние после радиотерапии челюстно-лицевой
412
и шейной областей. Некоторые из этих местных противопоказаний носят относительный характер и по мере их устранения теряют свою ограничительную силу, например, аномалия прикуса.
В отсутствие общих и местных противопоказаний ортопедическое лечение с использованием имплантатов показано следующим больным:
1) с концевыми (односторонними, двусторонними) дефектами зубного ряда;
2) с полным отсутствием зубов, когда традиционными способами протезирования невозможно обеспечить удовлетворительное функционирование полных съемных протезов из-за несостоятельности протезного ложа или отсутствия адаптации к полным съемным протезам;
3) с одиночным зубом, когда протезирование зубов не может быть эффективным при применении традиционных способов;
4) с обширными включенными дефектами зубного ряда.
В тех случаях, когда речь идет об эффективности ортопедического лечения, следует иметь в виду ее функциональные, эстетические, профилактические, социальные и психологические аспекты.
Отказ больного от частичного съемного протеза, желание его иметь несъемную конструкцию с использованием имплантатов не следует рассматривать как некий каприз или прихоть. В каждом случае врачу необходимо глубоко проанализировать мотивации пациентов, выяснить причины отказа от съемных конструкций и тщательно оценить возможность использования имплантации.
Следует подчеркнуть, что некоторые больные, у которых по разным причинам не удалось добиться удовлетворительных результатов от традиционного протезирования, испытывают чувство разочарования и безысходности. В этих случаях использование имплантации (в отсутствие противопоказаний) может явиться единственным способом, позволяющим выйти из сложившейся ситуации. С этим обстоятельством связаны огромный интерес к имплантации определенной части больных и глубокое разочарование, когда из-за общих или местных противопоказаний использование имплантатов невозможно.
Разъяснение противопоказаний к имплантации таким больным необходимо проводить очень продуманно, со строгим соблюдением деонтологических принципов. Обязательно следует подчеркнуть, что с развитием имплантологии противопоказания будут сужаться и что съемные конструкции следует рассматривать как этап, имеющий важное лечебно-профилактическое значение.
Определенный интерес для уточнения показаний и противопоказаний к использованию имплантатов представляют данные, полученные при обследовании больных с концевыми дефектами зубного ряда. Так, В. В. Лось (1985) установил, что 13,3% обратившихся в поликлинику имели односторонние концевые дефекты на одной из челюстей. При этом из 380 больных, находившихся под динамическим наблюдением, 152 не пользовались протезами, в результате у части из них развивалась деформация окклюзионной поверхности противоположного зубного ряда. При обследовании у 30 больных из этой группы были установлены условия для проведения имплантации: наличие устойчивых зубов, ограничивающих концевой дефект, хорошо сохранившийся альвеолярный отросток в области удаленных моляров, отсутствие деформации окклюзионной поверхности противоположного зубного ряда.
В. Н. Олесова (1986), обследовавшая 105 человек в возрасте от 20 до 60 лет с односторонними концевыми дефектами зубного ряда нижней челюсти, установила, что у 56% обследованных были изготовлены съемные пластиночные или несъемные консольные протезы. Большинство больных (60%) не пользовались съемными протезами. Лиц молодого возраста угнетало присутствие во рту съемной конструкции. У больных, пользовавшихся консольными протезами,
413
наблюдались подвижность опорных зубов, резкое укорочение зуб^1ого ряда, Часто встречались деформации зубных рядов и воспалительные заболевания пародонта. У 27% больных выявлены сопутствующие заболевания внутренних органов, некоторые из которых (у 3,8% больных) относились к значительно . снижающим регенеративные способности организма (эндокринные расстройства, болезни крови, диффузные поражения соединительной ткани, аллергия),
Определение параметров беззубого участка челюсти у больных, у которых не было противопоказаний к имплантации, дало следующие результаты: расстояние от вершины альвеолярного гребня до нижнечелюстного канала варьировало от 9 до 24 мм, у 52% обследованных составляло 10—15 мм; ширина альвеолярной части на уровне средней трети челюсти у 93,4% человек составляла 6—10 мм.
Эти данные свидетельствуют о возможности применения у большинства больных с концевыми дефектами нижней челюсти внутрикостных имплантатов, поскольку конструкции диаметром 4—5 мм и длиной 10—15 мм могут нести определенную функциональную нагрузку и служить дополнительной опорой несъемных протезов.
Абсолютные противопоказания к внутрикостной имплантации — заболевания соединительной ткани, болезни крови, аллергические заболевания, пародон-тоз, близкое расположение нижнечелюстного канала к вершине альвеолярного гребня. Противопоказано применение имплантатов при близком расположении верхнечелюстной пазухи к гребню альвеолярного отростка.
Решение ряда клинических задач (обследование, составление плана лечения, ведение документации, анализ и обработка результатов наблюдения за больными и др.) может облегчить применение электронно-вычислительных машин (ЭВМ).
Нами (М. 3. Миргазизов, С. М. Бурметьев, Г. А. Кошкин) на базе ПЭКВМ «Искра-226» был разработан программно-технический комплекс (ПТК) «Имплантат» позволяющий проводить анализ информации, используемой при ортопедическом лечении с использованием имплантатов. ПТК «Имплантат». обеспечивает выполнение следующих функций: загрузку и актуализацию базы данных с клавиатуры по формам ввода; поиск информации в базе данных и вывод ее по запросу (по форме вывода или без нее) на экран дисплея либо на АЦПУ; редактирование информации в базе данных; выполнение сервисных процедур по обслуживанию наборов данных; поиск и вывод информации на экран дисплея или АЦПУ в графическом режиме; статистические обработки наборов данных.
На основании исходных данных ЭВМ анализирует состояние здоровья больного, выявляет абсолютные и относительные противопоказания к применению имплантации, выдает заключение о невозможности ее применения, в частности при наличии выявленных противопоказаний; обеспечивает планирование конструкции протеза в целом (с имплантатом), выводит рисунок конструкции в графическом режиме на экран дисплея или АЦПУ; проводит топографическую обработку ортопантомограммы (определяет с помощью автоматического устройства кодирования графической информации расстояний от вершины, альвеолярного гребня на верхней челюсти до нижнего края верхнечелюстной пазухи, от вершины альвеолярной части на нижней челюсти до нижнечелюстного канала для определения типа, размера, конструкции и места установки имплантата); проводит статистическую обработку данных — исходных и полученных при диспансерном наблюдении за больными, пользующимися протезами с применением имплантатов.
Следующая операция обеспечивает поиск и вывод информации из фонда и состоит в составлении запроса на поиск информации при заданных ограничениях и печати ее в произвольной форме на экране дисплея или АЦПУ.
414
ЭВМ обладает большими возможностями в создании региональных банков данных по имплантологии, с помощью которых может быть решена проблема накопления и анализа коллективного опыта ортопедического лечения с использованием имплантатов. Создание такого банка данных предусматривает поступление информации от соответствующих подразделений, занимающихся имплантацией. Для этих целей разработана специальная карта, в которой записывают результаты опроса или анкетирования больных; данные о состоянии зубов и полости рта в момент обращения к врачу по поводу имплантации;
данные о состоянии зубочелюстной системы после подготовки к имплантации и после лечения с использованием имплантатов; данные контрольных осмотров. При этом сведения об имплантатах и протезах предоставляются в соответствии с едиными рабочими классификационными схемами. Все это позволяет объективно оценить успехи и неудачи лечения больных с использованием имплантатов.
МАТЕРИАЛЫ, ПРИМЕНЯЕМЫЕ В ИМПЛАНТОЛОГИИ
В стоматологической имплантологии применяют большое количество материалов. Различают биотолерантные, биоинертные и биоактивные материалы. К биотолерантным относят сплавы благородных металлов, сплавы кобальта, хрома и молибдена, к биоинертным — титан и его сплавы, АЬОз, углерод, к биоактивным — стеклокерамика с биоактивной поверхностью, СаР04-керамика, гидроксилапатит.
Имплантационные материалы должны отвечать определенным требованиям. В частности, они должны быть коррозионноустойчивыми, неканцерогенными, нетоксичными, не вызывать аллергические реакции, обладать высокими механическими и технологическими свойствами, легко стерилизоваться, быть удобными в работе, эстетичными, общедоступными.
В имплантологии наиболее широко применяют металлы и сплавы. В стоматологических учреждениях страны, в которых производят имплантацию, используют нержавеющую сталь, КХС, титан, никелид-титан, серебряно-палладиевый сплав. Перспективными материалами являются титан и его сплавы, сапфир, гидроксилапатит.
В настоящее время изучена реакция костной ткани на большинство из перечисленных материалов. В. В. Паникаровский и соавт. (1985) показали, что вокруг имплантатов из КХС формируется соединительнотканная капсула. Большинство новообразованных костных структур имеют остеонное строение.
В работах М. 3. Миргазизова и В. Н. Олесовой (1985, 1986) прослежены закономерности образования связей с костью пористого имплантата из сплава NiTi с памятью формы. Реакция костной ткани на имплантацию этого материала заключается в активных процессах костеобразова;
ния. Через 3 мес после имплантации пористого никелида титана вновь образованная костная ткань на некоторых участках границы с имплантатом повторяет рельеф сплава, прослеживается в поверхностных порах имплантата. В то же время на других участках границы имплантат — кость образуетстя плотная соединительная капсула. В дальнейшем поровые пространства имплантата все глубже заполняются вновь образованной костной тканью. Через 6 мес после имплантации происходит формирование костных балок и постепенное замещение их остеонными структурами, характерными для зрелой пластинчатой кости. Через 9 мес наблюдается картина полного прорастания имплантата.
В. А. Воробьев (1987) установил определенную динамику реактивных изменений костной ткани на серебряно-палладиевый имплантат: в ранние сроки после его введения в окружающих тканях возникает острый воспалительный процесс, проявляющийся в очаговой нейтрофильной инфильтрации вблизи имплантата, но очень быстро развивается соединительная ткань. В последующие сроки вблизи имплантата формируется остеоидная ткань, которая с течением времени созревает с последующим многоразовым напластовыванием новообразованной кости.
Успех имплантации при применении металлических материалов зависит от многих факторов: состава и свойств металлов, формы имплантата, свойств
415
костной ткани, но наиболее важным свойством металлов и сплавов является устойчивость их к коррозии, которая определяет электрохимическое «поведение» металлического имплантата. Этому вопросу в литературе уделяется большое внимание. Доказано, что такие материалы, как нержавеющая сталь, сплавы на основе Со—Сг—Мо, СО—Сг—W—Ni, титан и его сплавы: Ti—6А1— 4V, TiNi, благородные металлы и сплавы на их основе являются коррозионно-устойчивыми.
Способность этих материалов противостоять химическому и электрохимическому воздействию среды (полость рта и ткани, окружающие имплантат) связана с пассивацией металлов, обусловленной образованием на поверхности металла пленок труднорастворимых соединений, например оксидов. Металлургические, технологические, конструкционные погрешности и другие причины могут привести к повреждению защитной пленки, вызывая процессы коррозии и ответную реакцию тканей. Возможны следующие типы коррозии: общая, гальваническая, ямочная, щелевая, коррозия напряжения, включая усталостную коррозию.
Из всех перечисленных металлических материалов самой высокой коррозионной стойкостью обладают титан и его сплавы, что позволяет осуществлять пожизненную имплантацию титановых конструкций в организм больного. Однако модель поверхностных реакций органических молекул с металлическими имплантатами, которая учитывает как свойства ткани и состав биологической жидкости, так и вид и свойства окислов, покрывающих поверхность имплантата, показывает, что для титановых имплантатов транспорт электронов через границу раздела ингибируется достаточно толстым пассивирующим окисным слоем. При этом адсорбция белков не сопровождается изменением их нативной конформации. На поверхности металлов или сплавов, образующих в биологической среде слой окислов с электронной проводимостью, адсорбированные белковые макромолекулы изменяют конформацию из-за электрохимических реакций. Таким образом, высокая биосовместимость обусловлена значительно сниженным ионным обменом на поверхности раздела имплантат — живая ткань, что обеспечивает стабильную регенерацию клеток.
Предварительное суждение о биосовместимости имплантата может быть основано на результатах анализа данных об его электрохимическом «поведении» в средах, моделирующих жидкие среды организма. Полученные результаты обычно сравнивают с электрохимическим «поведением» титана или некоторых его сплавов, применяемых в медицине.
Высокая коррозионная стойкость титана и его сплавов хорошо известна и позволяет осуществлять пожизненную имплантацию фиксаторов в организме больного. Однако среди всех известных титановых сплавов особое положение занимает никелид титана, обладающий наряду с указанными выше свойствами также термомеханической памятью — эффектом памяти формы.
Никелид титана обладает высокой стойкостью в 20% растворе соляной кислоты и растворах солей, но нестоек в царской водке, плавиковой и азотной кислотах.
С целью оценки коррозионной стойкости никелида титана и сплавов на его основе при комнатной температуре (23 °С) были сняты анодные потенциодина-мические кривые в разных средах — 5 об % Н1ХОз, 3,7 об % НС1, 40 об % КОН, 50 об % НССОН (рис. 142, 143). Исследовали сплавы на основе никелида титана, в том числе с добавками меди, алюминия, железа или марганца, полученные по разным технологическим схемам [Гафаров А. Р. и др., 1985].
Одна схема получения сплавов предусматривала многократную (4—6 раз) электродуговую плавку в медном водоохлажденном поддоне шихты, состоящей из никеля и йодидного титана. В качестве легирующего элемента использовали электролитическую медь.
416

Рис. 142. Поляризационные кривые сплавов на основе TiNi в 3,7% растворе НС1. 1 — TiNi (приготовлен по схеме 1); 2 — TiNi (приготовлен по схеме 2); 3 — сплав ВТ-6.
-У,
В
-0,5
0,5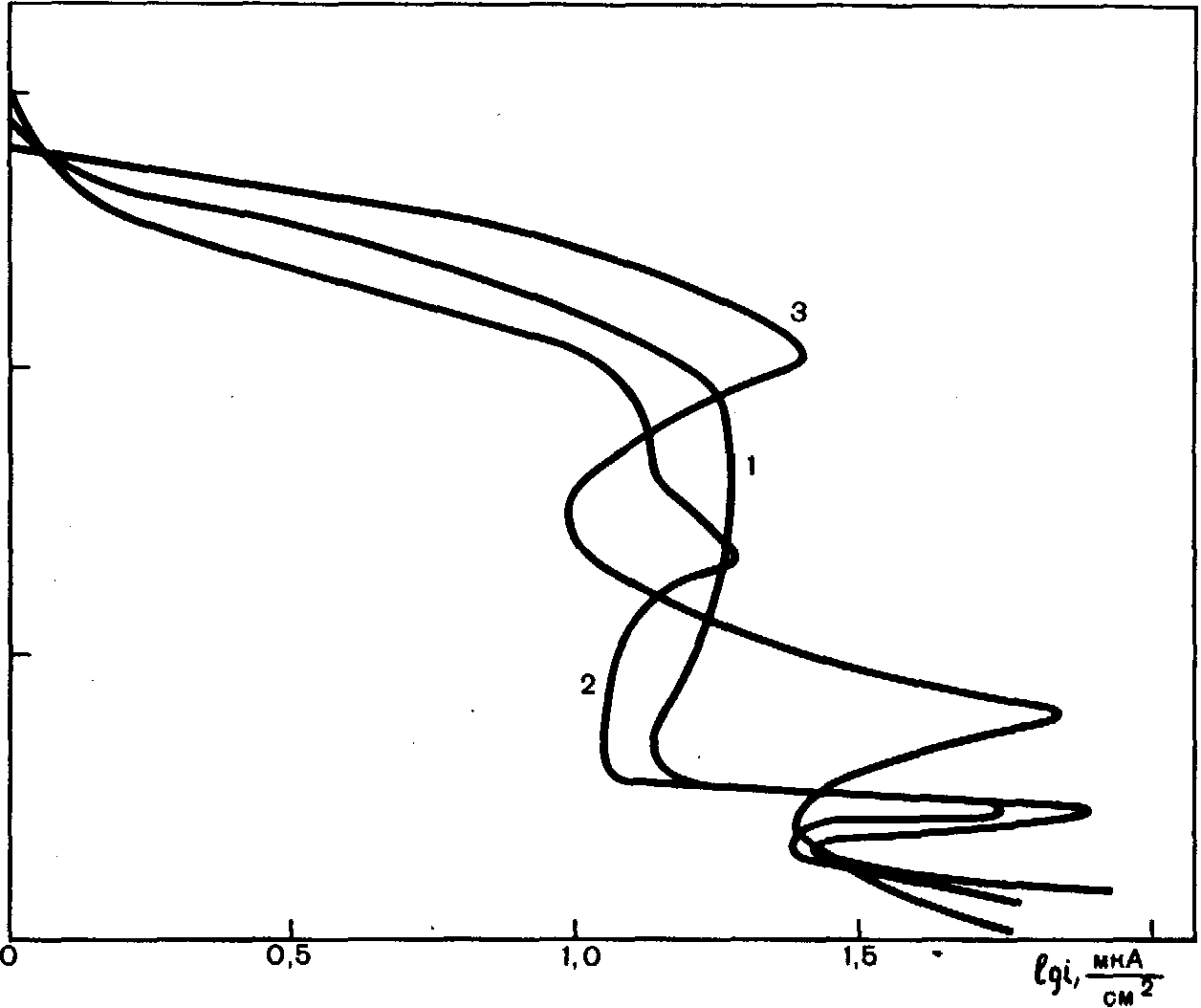
Рис. 143. Поляризационные кривые сплавов на основе TiNi в 40% растворе КОН.
1 — TiNi (приготовлен по схеме 1); 2 — TiNi (приготовлен по схеме 2); 3 — нержавеющая сталь.
15 Руков. по ортоп. стом.
Другая схема предусматривала на первой стадии получение электрода методом самораспространяющегося высокотемпературного синтеза, а затем проведение двукратного электродугового переплава. В качестве шихтовых материалов использовали порошки титана марки ПТЭМ-1 (ТУ—48—10—22— 73), никеля марки ПНК-1 ВЛ7 (ГОСТ 14—12—03—65), железа карбонильного особо чистого марки А (ТУ— 6— 09— 3000— 73), меди майги ПМС-1 (ГОСТ 4960—68) и алюминия марки АСД-1 (ТУ—48—5—100—75). Слитки, полученные этими способами, прокатывали при температуре 800—850° С с полосы толщиной 1 мм, из которых вырезали образцы для испытаний.
Сравнение анодных потенциодинамических кривых для сплавов на основе никелида титана показало, что независимо от состава наблюдается область активного растворения, пассивного состояния и перепассивации.
Максимальной коррозионной стойкостью обладает стехиометрический никелид титана, отклонение от стехиометрии или его легирование приводит к небольшому снижению коррозионной стойкости.
При испытании в 3,7 об % НС1 коррозионная стойкость сплавов на основе никелида титана заметно выше, чем у нержавеющей стали марки 12Х18Н10.
Сплавы на основе никелида титана, полученные из чистых шихтовых материалов путем многократной электродуговой плавки, обладают более высокой коррозионной стойкостью, чем сплавы, полученные из порошков с помощью самораспространяющегося высокотемпературного синтеза и двукратного электродугового переплава. Последние отличаются повышенной структурной и химической неоднородностью и более высоким содержанием газовых примесей. Известно, что гомогенность структуры и состава обеспечивает более высокую коррозионную стойкость сплавов.
Дальнейшее сравнительное исследование электрохимического «поведения» сплавов на основе никелида титана, сплавов титана ВТ 1-010 и ВТЗ-1 и нержавеющей стали 12Х18Н10Т в водных растворах с концентрацией 3 масс % NaCI и 3,7 масс % НС1 показало, что сплавы на основе никелида титана хорошо пассивируются, а их коррозионная стойкость, особенно сплава, легированного молибденом, примерно соответствует стойкости сплава ВТ 1-00 и заметно выше, чем у нержавеющей стали [Итин В. И. и др., 1989].
Результаты лабораторных исследований корризионной стойкости сплавов на основе никелида титана полностью совпадают с полученными при исследовании биологической совместимости этого сплава.
Среди работ, посвященных изучению этой проблемы, особо следует выделить работу Costleman и соавт. (1976), в которой на основе тщательно спланированного эксперимента на собаках, гистологических исследований и нейтронно-активационного анализа кости, мышц, печени, почек, селезенки, легкого и мозга доказана' биосовместимость нитинола и его преимущества перед сплавами на основе кобальта и хрома. Авторы указывают, что кость, прилегающая к имплантату из сплава кобальта и хрома, контаминировалась хромом после выдержки до 17 мес. В сплавах NiTi этого явления не наблюдалось. К аналогичным выводам пришли Набэсима и соавт. (1982), Ониси и соавт. (1983), которые вживляли титаново-никелевую пластину свиньям и баранам.
По единодушному мнению исследователей, сплавы на основе никелида титана отвечают трем основным требованиям, без соответствия которым ни один материал не может считаться пригодным для введения в организм человека.
Это, во-первых, высокая антикоррозионная устойчивость; во-вторых, отсутствие токсичности, канцерогенности; в-третьих, наличие механических свойств, близких к свойствам живых тканей, что позволяет с высокой надежностью осуществлять лечение больных.
418 -
КОНСТРУКЦИИ ИМПЛАНТАТОВ
Существует множество систем имплантатов. Многообразие имплантатов обусловило необходимость их систематизации. Взяв за основу тот или иной признак, можно создать довольно стройную классификацию имплантатов. Например, по биосовместимости материала, применяемого для имплантации, различают биотолерантные (нержавеющая сталь, КХС), биоинертные (алюми-нийоксидная керамика, титан, углерод, никелид титана), биоактивные (гидро-ксилапатит, трикальций-фосфат, стеклокерамика с активной поверхностью), имплантаты по форме—цилиндрические (сплошные, полые), винтообразные, листовидные (пластинчатые), конусовидные, формы корня естественного зуба, по структуре материала — беспористые, поверхностно-пористые, со сквозной пористостью, комбинированные, по свойству материала — без эффекта «памяти» формы, с эффектом «памяти» формы, по локализации — чрескорне-вые, подслизистые, поднадкостничные, внутрикостные, чрескостные, комбинированные, по функции — замещающие, опорные, опорно-замещающие, по восприятию жевательного давления — с амортизатором (внекостным, внутри-костным, комбинированным), без амортизатора, по конструкции внутрикостной части — разборные, неразборные, по конструкции соединения имплантата с супраструктурой — неразъемное соединение с помощью магнитных систем, по способу изготовления — стандартные, индивидуальные, по месту производства — заводского производства, лабораторного изготовления (в зуботехни-ческой лаборатории).
Конструктивно в имплантате выделяют три основные части: корневую часть, шейку и головку (опорная головка). Применяют и другие термины:
корневую часть называют внутриальвеолярной или внутриопорной конструкцией, шейку — пришеечной областью имплантата, шейку и головку вместе — внеальвеолярной коронковой частью имплантата. В отдельных конструкциях выделяют плечи, ножки имплантата, каркас и т. д.
О. Н. Суров (1987) применил, фактически повторив конструкцию по Линкову, вариант конструкции имплантата из КХС, состоящую из головки, шейки, поднадкостничной пластинки и внутрикостных ножек. Автор назвал эту конструкцию ЭСИ (эндосубпериостальный имплантат). По его мнению, наиболее простым и эффективным является вариант, когда на ЭСИ во фронтальном отделе делают мостовидные протезы и съемный протез. Конструкция может быть также использована как средняя опора для мостовидного протеза. Имплантаты используют в качестве опор при применении традиционных систем фиксации протезов по Румпелю или Дольдеру.
В зарубежной литературе конструкции имплантатов объединяют в системы, давая им определенные названия: CBS (рис. 144, а), диск-имплантат по Скортеччи (рис. 144, б), имплантат по Линкову (рис. 144, в), фриолит-имплантат по Шульту (рис. 144, г), AMS (рис. 144, д), IMZ по Киршу (см. рис. 149), система «Biolox» и др. Каждая система имеет свое инструментальное обеспечение.
Следует более подробно остановиться на некоторых системах. Система CBS представляет собой набор внутрикостных имплантатов из алюминийоксид-ной керамики и инструментов для их имплантации. Корневая часть имплантата имеет винтообразную форму, коронковая — круглую форму со шлицами. Размеры: общая длина 15—20 мм, диаметр 4—5 мм.
Система AMS — набор пластиночных имплантатов из сплава T16A14V и инструментов для имплантации. Конструктивно имплантат состоит из пластиночной решетчатой внутрикостной части и головки. Разновидности внутрикостной части отличаются по величине пластинки, ее формы (выпуклая и вогнутая), локализации (тело, ветвь нижней челюсти).
15* 419
Рис.
144. Виды
имплантатов. а
—
CBS; б
— Uisk-имплантат;
в —
Beatt-имплантат;
г —
Frialit-
имплан-. тат; д
—
AMS.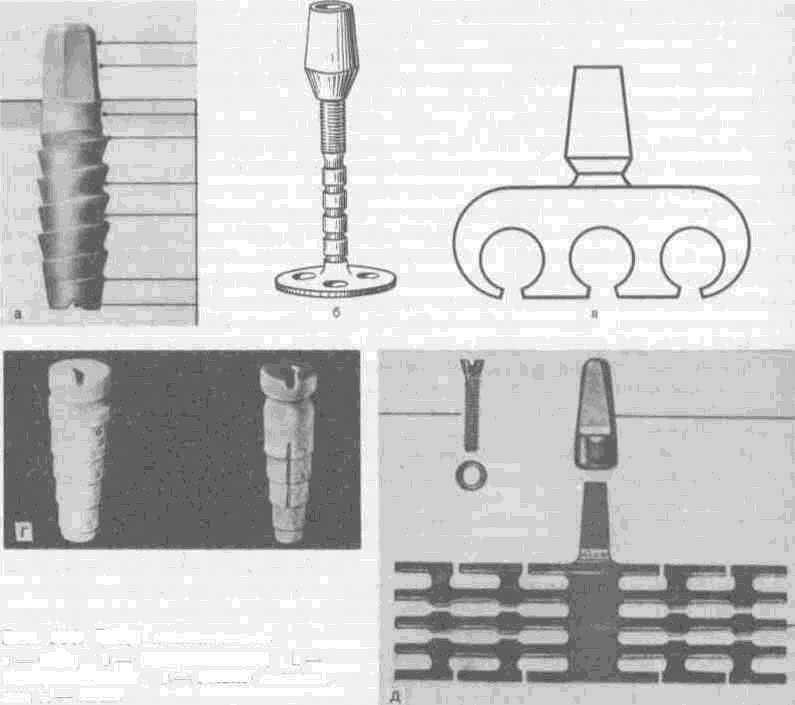
Диск-имплантат по Скортеччи представляет собой цилиндрический стержень с основанием в форме диска и головкой частью с винтовой нарезкой, на которую наворачивают коронковую часть имплантата. Имплантат изготавливают из чистого титана; выпускается в виде набора, состоящего из трех типоразмеров имплантатов и трех типоразмеров режущих инструментов, соответствующих по форме диск-имплантату.
Операционная техника состоит из следующих основных этапов: делают вертикальный разрез на вестибулярной поверхности альвеолярного отростка и горизонтальный — по гребню альвеолярного отростка с отслойкой слизисто-надкостничного лоскута, создают костное ложе (бормашиной с помощью диск-инструмента); подготавливают костное ложе к установке имнлантата;
устанавливают диск-имплантат в костном ложе; ушивают рану; подсоединяют коронковую часть имплантата и осуществляют протезирование.
Система «Biolox» содержит внутрикостные и эндодонтические имплантаты из алюминийоксидной керамики как для однофазной, так и для двухфазной имплантации, а также инструменты для их установки в челюстных костях. При однофазной имплантации в качестве боковой опоры на нижней челюсти используют имплантаты с анкерными крыльями, на верхней челюсти (в переднем отделе) — имплантаты цилиндрической формы с ретенционной прорезью в корневой части. Коронковая часть имплантата повторяет форму препарирован-
420
ного зуба с уступом под керамическую коронку. Для беззубой нижней челюсти выпускают винтовой цилиндрический имплантат с граненой коронковой частью. В комплект для двухфазной имплантации входит разборный имплантат с винтовой нарезкой и внутренним отверстием для соединения с коронковой частью имплантата.
Эндодонтические штифты системы «Biolox» предназначены для трансдентальной фиксации, ортоградного, ретроградного пломбирования корня и ауто- и аллопластических реплантаций зубов. Для работы с ними имеется набор инструментов.
Jacobs (1985) делит известные в настоящее время системы имплантатов на две группы: «старая» система (листовидные имплантаты Линкова и др.) и «молодая» система (IMZ, Frialit и др.). По его статистическим данным, удельный вес «молодой» системы составляет 82% от всех видов имплантатов, используемых во врачебной практике, причем их применяют в возрасте до 50 лет. Лучшие результаты получены при применении «молодой» системы.
Многообразие конструкций имплантатов затрудняет их выбор. С целью облегчения этой задачи можно пользоваться следующими рекомендациями. Конструкцию имплантата следует выбирать в соответствии с клиническими условиями с учетом переносимости больным материала; степени атрофии альвеолярных отростков на тех участках, где отсутствуют зубы; анатомо-топографических соотношений альвеолярных гребней и верхнечелюстных пазух, носовой полости на верхней челюсти и нижнечелюстного канала на нижней;
толщины слизистой оболочки, покрывающей альвеолярные отростки; толщины нижней челюсти в переднем и боковых отделах. Например, при выраженной атрофии альвеолярных отростков и близком расположении к гребню пазух и канала показано применение поднадкостничного имплантата, при небольшой толщине нижней челюсти в боковых отделах целесообразно использовать листовидные имплантаты. В остальных случаях следует отдавать предпочтение цилиндрическим имплантатам.
В том случае, когда на имплантат ожидается значительная жевательная нагрузка, необходимо сделать выбор в пользу имплантатов с амортизаторами. Кроме того, выбор конструкции имплантата может быть обусловлен методом имплантации, который планируется использовать в том или ином случае. Например, для двухфазной имплантации может быть применена только разборная конструкция, для непосредственной имплантации предпочтительнее керамические имплантаты, имеющие форму естественного зуба. Выбор конструкции имплантата зависит также от возможностей их приобретения или изготовления в конкретном учреждении и инструментального обеспечения. В связи с этим большую ценность для врача представляют готовые комплекты имплантатов и инструментов, которые облегчают выбор имплантата и его применение, поскольку эти комплекты создают для решения конкретных задач ортопедического лечения с использованием имплантатов.
Отечественная медицинская промышленность выпускает комплект листовидных титановых имплантатов и инструментов, который позволяет реализовать метод однофазной имплантации при частичном и полном отсутствии зубов.
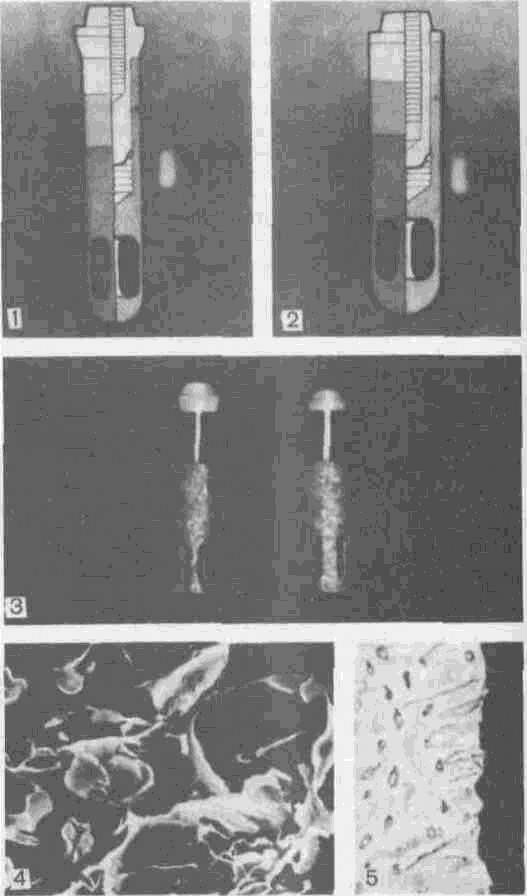
Комплект имплантатов и инструментов на основе использования пористых и беспористых сплавов титана для двухфазной имплантации разработан коллективом сотрудников Кемеровского медицинского института, Сибирского физико-механического института (рис. 145; рис. 146, см. вклейку; рис. 147). Он содержит три типа имплантатов: тип ПЦ-А — пористый цилиндрический с амортизатором, тип ПЦ-Б/А — пористый цилиндрический без амортизатора, может иметь неразборный вариант для однофазной имплантации, тип ПЦ-ЭПФ — пористый цилиндрический с эффектом памяти формы системы МГИ (М. 3. Мир-газизов, В. Э. Гюнтер, В. И. Итин). Первый тип имплантата имеет следующие
421
характеристики: диаметр 3,9 мм, длина 9, 11 и 13 мм, второй тип—диамет) 3,9 и 3,5 мм, причем 3,5-миллиметровые имеют длину 11, 13, 15 мм, третий тип -диаметр 3,9 мм, длину 9, 11 и 13 мм. Конструкции имплантатов реализуют n;i практике концепцию сквозной оссеоинтеграции в корневой части имплантата. а также имитацию периодонтальных волокон за счет тонких проволочных нитеи из сплава с памятью формы (тип ПЦ-ЭПФ).
Все три типа имплантатов разборные. К имплантатам прилагаются конструкционные элементы (титановый винт-заглушка, культя-амортизатор, культевой конус и соединительные винты), лабораторные приспособления (направляющие втулки — базисные, оттискные, коронковые, культовые штифты) и инструменты (сверла, компостер, фигурный нож, шаблон-измеритель, ударное устройство, ударная головка, отвертки, приспособления для охлаждения и деформации элементов с эффектом памяти формы, устройство для извлечения имплантата, контейнер).
Комплект применяют следующим образом. Определив показания к протезированию зубов с использованием имплантатов. приступают к выбору тип;', имплантата. Имплантат типа ПЦ-А преимущественно показан в тех случаях, когда имплантат как опора конструктивно связан с естественными зубами. Моделирование посредством амортизатора параметров физиологической подвижности зубов, включенных в опорную систему мостовидного протеза, позволяет рационально распределить жевательную нагрузку на ткани, окружающщ

Рис. 145. Комплект имплантатов и инструментов. Объяснение в тексте.
Рис. 147. Инструменты для имплантации.
а—направляющие кольца и втулки; б—компостеры для иссечения слизистой оболочки у места введения имплантата; в — фигурный нож для отсечения слизистой оболочки, г — низкооборотш"'' наконечник и ручной привод; д — сверла; е — измеритель глубины костного ложа; ж приспио ление для вколачивания имплаитата; з — отвертки.
422
![]()

00 ^
ф 0 О




![]()
![]()
зубы и имплантаты. Имплантат типа ПЦ-Б/А показан в тех случаях, когда имплантаты не связаны с естественными зубами, например при полном отсутствии зубов. Третий тип имплантата — ПЦ-ЭПФ — наиболее приемлем при значительном уменьшении высоты альвеолярного отростка. В этих случаях целесообразно устанавливать подряд несколько имплантатов в расчете на то, что внутрикостные проволочные элементы с памятью формы создадут взаимосвязанный блок, способный противостоять жевательной нагрузке при относительно неблагоприятном соотношении корневой и коронковой частей имплантат-ной системы.
После выбора типа имплантата осуществляют подбор конструкционных элементов, лабораторных приспособлений и инструментов. Последовательность клинико-лабораторных этапов непосредственного и отсроченного изготовления зубных протезов после имплантации представлена в табл. 5 и 6.
МЕТОДЫ ИМПЛАНТАЦИИ
Существующие методы имплантации могут быть сгруппированы по следующим классификационным признакам: по сроку имплантации — непосредственно после удаления зуба (имплантация в свежую лунку удаленного зуба), отсроченные (после полного заживления лунки зуба); по признаку сообщения с полостью рта в период приживления имплантата — сообщающиеся (однофазная имплантация), несообщающиеся (двухфазная методика с «закрытым» приживлением корневой части имплантата в первой фазе). В зависимости от выбора этих методик возникает ситуация приживления имплантата в условиях функциональной нагрузки и без функциональной нагрузки.
Сущность методики непосредственной имплантации заключается в том, что операцию имплантации проводят одновременно с удалением зуба. Этот метод целесообразно применять для замещения передних зубов, но он противопоказан после удаления зубов при заболеваниях пародонта.
По мнению сторонников методики непосредственной имплантации, она обеспечивает плотный охват шейки имплантата волокнами маргинальной связки, если их аккуратно отсепарировать и сильно не травмировать при удалении зуба.
Классическим примером непосредственной имплантации являются тюбин-генские непосредственные имплантаты (Frialit) из алюминийоксидной керамики ступенчато-цилиндрической формы с лакунами по всей корневой поверхности. В пришеечной области этих имплантатов имеется гладко отполированная бороздка для десны. Головка имплантата разборная, она фиксируется в корневой части после введения ее в костное ложе. Тюбингенские имплантаты показаны для замещения резцов, клыков и премоляров, подлежащих удалению вследствие травмы, резорбции корней, периодонтита и других причин, кроме системных заболеваний пародонта.
Операция заключается в удалении зубов или их корней, последовательной обработке лунки конусовидным, цилиндрическим и ступенчатым сверлом, введении имплантата в костное ложе, фиксации имплантата с помощью лигатурного связывания, защитой раны эластичной повязкой на 6 дней. После этого проводят временное протезирование, а через 3 мес — постоянное;
обычно изготавливают металлокерамические протезы.
Методика отсроченной имплантации заключается в формировании искусственной лунки (костного ложа) для имплантата после окончательного заживления костной раны после удаления зубов. Сроки здесь могут быть разными—от 1,5 мес до года в зависимости от интенсивности репаративных процессов. Имплантологи справедливо считают, что только при полном заживлении костной ткани возможно создание искусственной лунки, обеспечи-
424 .
вающей плотный контакт имплантата с костью и его устойчивость. Этот способ применяют наиболее часто, поскольку у большинства больных, обращающихся по поводу имплантации, как правило, зубы давно отсутствуют.
Описывая операцию имплантации зуба, целесообразно выделить в ней четыре последовательных этапа: 1) иссечение и отслаивание слизисто-над-костничного лоскута; 2) создание костного ложа для имплантата; 3) введение имплантата в костное ложе; 4) закрытие послеоперационной раны.
Первый этап операции может быть выполнен двумя способами: путем иссечения слизисто-надкостничного лоскута с помощью пробочника (компостера) и иссечения лоскута скальпелем с последующей отслойкой и откидыва-нием его.
Создание костного ложа для имплантата может быть осуществлено разными способами: сверлением, с помощью долота и комбинированным методом (сверление и формирование ложа с помощью долота). В свою очередь сверление можно производить бормашиной на низких оборотах или ручным способом, что полностью исключает перегревание костной ткани. Оптимальные условия для сверления кости возникают при применении локальной гипотермии с помощью аппарата «Ятрань» [Миргазизов А. М., 1988].
Третий этап — введение имплантата в костное ложе — также может быть выполнен разными способами: вкручиванием (при использовании винтообразных имплантатов), вколачиванием и свободным размещением имплантата в костное ложе (при чрескостной имплантации на нижней челюсти).
Последний этап—закрытие послеоперационной раны—заключается в укладывании слизисто-надкостничного лоскута и фиксации его швами. При иссечении слизисто-надкостничного лоскута с помощью компостера швы не накладывают — достаточно закрыть рану тампоном или защитной базисной пластинкой.
Далее рассмотрим методы однофазной и двухфазной имплантации.
Методика однофазной имплантации состоит в том, что корневую часть имплантата плотно устанавливают в костном ложе, а головка при этом выступает в полость рта. Пришеечная часть имплантата вступает в контакт со слизистой оболочкой. Этот способ прост и доступен для широкого применения, не требует сложных разборных конструкций имплантатов. Однако при его применении высока вероятность неудач, поскольку регенеративные процессы происходят при наличии сообщения с полостью рта.
Методика двухфазной имплантации предусматривает приживление сначала только корневой части имплантата в условиях изоляции от полости рта, лишь после успешного решения этой задачи происходит соединение корневой части имплантата с головкой. Классическим примером двухфазной методики имплантации является система Бронемарка, применяемая при полном отсутствии зубов (рис. 148, см. вклейку). Эта система показана в следующих случаях: 1) недостаточная фиксация полных съемных протезов из-за выраженной атрофии альвеолярных отростков; 2) неспособность больного адаптироваться к съемным протезам независимо от степени их фиксации; 3) функциональные расстройства (тошнота, рвота), связанные с применением съемных протезов, при этом возраст больных колеблется в больших пределах — от 20 до 77 лет. Для большинства больных необходим примерно год пользования полными съемными протезами, для того чтобы произошла окончательная функциональная перестройка кости после удаления зубов.
Вначале проводят тщательное клиническое и рентгенологическое обследование больных. Осуществляют строгий отбор больных в соответствии с принятыми показаниями бригадой специалистов (стоматолог-хирург, ортопед, рентгенолог и др.).
Оперативные вмешательства производят в два этапа (фазы): введение
425
Первая фаза операции состоит из ряда последовательных манипуляции, проводимых под местной анестезией с премедикацией: 1) проведение широкого горизонтального разреза слизистой оболочки с вестибулярной стороны пример но на уровне половины высоты альвеолярного отростка, отслаивание и откиды вание в язычную или небную сторону слизисто-надкостничного лоскута до обнажения альвеолярного отростка от одного ментального отверстия до другого на нижней челюсти и до стенок верхнечелюстных пазух на верхней; 2) выравнивание альвеолярного гребня в зоне расположения имплантатов путем сошлифо-вывания; 3) определение местоположения шести имплантатов на каждой челюсти и разметка их путем сверления с помощью обычного шаровидного бора;
4) создание первого костного ложа для имплантата, место для которого выбирают ближе к средней линии челюсти, тщательно ориентируя по отношению к гребню и телу челюсти;
5) создание костного ложа для остальных имплантатов с обеспечением параллельности гнезд с помощью специального приспособления (параллело-метра), которое устанавливают в костном ложе первого имплантата; 6) расширение и подготовка костного ложа для введения корневой части имплантата; 7) введение корневой части имплантата в костные ложа; 8) ушивание раны; 9) послеоперационное ведение больного.
Вторую фазу операции проводят после заживления — через 3—4 мес на нижней челюсти и 5— 6 мес на верхней. Она состоит в установлении опорных головок, т. е. внеаль-веолярной части конструкции. С этой целью обнажают винты-заглушки, осторожно их вывинчивают, заменяя на опорные головки. Операционное поле закрывают на 1 нед защитной каппой.
Рис. 149. Система «IMZ» по Киршу.
426
Протезирование начинают через 2 нед после операции по установке опорных головок. Послеоперационные результаты весьма успешные, на протяжении 15--20 лет стабильность протезов отмечена в 99% случаев на нижней челюсти, в 95% — на верхней челюсти.
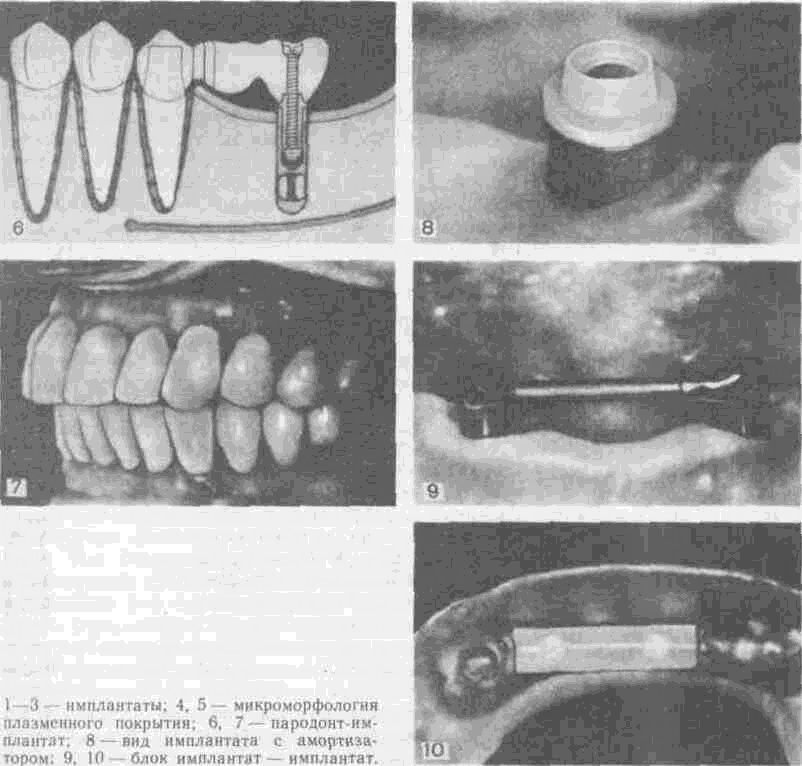
Близка к системе Бронемарка двухмоментная внутрикостная система имплантатов IMZ (интрамобильные цилиндрические имплантаты), разработанная в ФРГ в 1970 г. Эта система снабжена амортизатором, который доступен наблюдению и замене, поскольку протезные конструкции, опирающиеся на амортизирующий элемент, соединены с имплантатом с помощью винтов (рис. 149). По данным Kirsch и Mentag (1986), 95% IMZ-имплантатов продолжали успешно функционировать через 7,5 лет после их установления. Такой успех объясняется надежной оссеоинтеграцией, а также тем, что к имплантату прикреплена слизистая оболочка десны. Кроме того, большую роль играют тщательный отбор пациентов, высокий уровень диагностики, дооперационное планирование лечения, точность хирургической техники и высокий уровень гигиены полости рта, поддерживаемый пациентом.
ОСОБЕННОСТИ КОНСТРУИРОВАНИЯ ЗУБНЫХ ПРОТЕЗОВ С ИСПОЛЬЗОВАНИЕМ ИМПЛАНТАТОВ
Конструирование зубных протезов с использованием имплантатов завися' от клинической картины, определяемой состоянием оставшихся зубов и ткане! протезного ложа, метода имплантации и конструкции имплантата. Так, конст руирование зубных протезов на базе поднадкостничных имплантатов npi полном отсутствии зубов сводится к изготовлению зубного протеза, фиксирую щегося на выступающих в полость рта штифтах с помощью телескопических замковых или магнитных систем крепления.
Оригинальный метод фиксации полного съемного протеза на нижне» челюсти с помощью имплантатов из стали, обладающей ферромагнитным» свойствами, и магнитов из самарий-кобальта разработал Б. П. Марков (1987) Сущность его заключается в том, что на альвеолярную часть беззубой нижне-челюсти хирургическим путем поднадкостично подшивают имплантаты из стал» марки 30Х13 либо 40Х13 (сплавы обладают ферромагнитными свойствами и биосовместимостью). Соответственно расположению имплантатов в протезе устанавливают магниты из самарий-кобальта. Сила притяжения магнитов способствует улучшению фиксации протезов. Схема воздействия постоянного магнитного поля на дополнительную фиксацию протеза показана на рис. 150, Метод показан при выраженной атрофии альвеолярного отростка нижней челюсти, когда традиционными способами невозможно обеспечить фиксацию протеза.
При внутрикостной имплантации разработано большое количество конструкций зубных протезов, что порождает трудности и неуверенность в выборе оптимального варианта. Определенную помощь врачу могут оказать разработанные нами правила конструирования зубных протезов с использованием внутрикостных цилиндрических имплантатов. Они составлены на основе результатов клинических наблюдений, экспериментальных исследований распределения напряжений в околоимплантатной зоне и теоретических положений, опирающихся на современные достижения имплантологии и ортопедической стоматологии.
Предлагаемые правила являются ориентировочными, поэтому по мере получения новых данных о допустимой нагрузке на имплантаты и о способах ее расчета они могут быть уточнены. В связи с этим изложенные правила рекомендуются для решения практических задач конструирования зубных протезов с использованием цилиндрических имплантатов на том уровне знаний, который имеется в настоящее время. Предложенные ниже правила следует рассматривать как временные.
1. При наличии зубов имплантат следует конструктивно связывать с естественным зубом и рассматривать их как единый блок пародонт — имплантат (ПИ), способный выполнять не только замещающую, но и опорную функцию (рис. 151, 1). Однако при создании блоков следует обеспечить одно важное условие: физиологическая подвижность зуба, включенного в блок, и амортизирующие свойства имплантата должны быть близки друг другу.
2. Два конструктивно связанных имплантата образуют блок имплантат — имплантат (ИИ), способный выполнять как замещающую, так и опорную функции (рис. 151, 2).
3. Блоки ПИ и ИИ, конструктивно соединяясь непосредственно друг с другом или через искусственные зубы, образуют единую» конструкцию зубного протеза (рис. 151, 3). При этом в мостовидном протезе оптимальное соотношение количества опорных блоков и искусственных зубов должно составлять 1:1 с предельным допуском 1:1,5 с учетом клинических особенностей. В том случае, если выдержать это соотношение невозможно, создают съемную конструкцию.
,»:?8
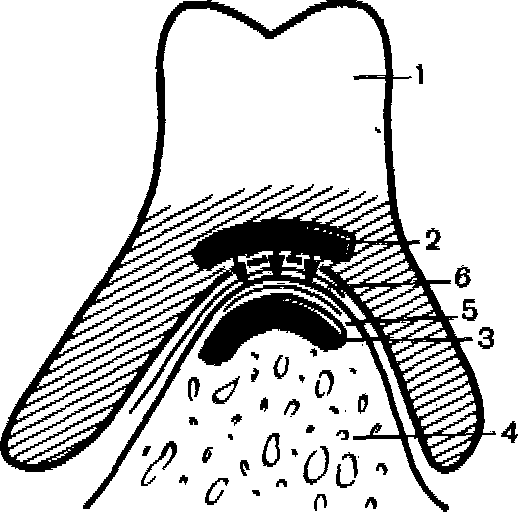
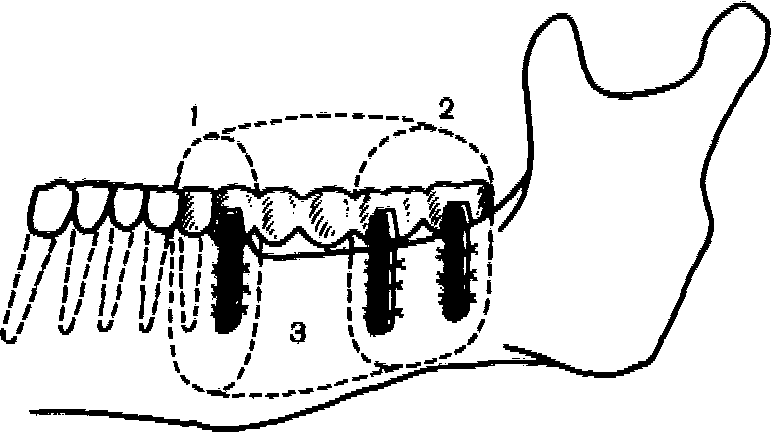
Рис. 150. Схема действия постоянного магнитного поля на дополнительную фиксацию протеза по Маркову. 1 — протез; 2 — магнитная пластинка; 3 — металлический имплантат; 4 — альвеолярная часть нижней челюсти; 5— надкостница; 6— слизистая оболочка.
Рис. 151. Мостовидный протез, фиксированный на зубах и имплантатах. 1 — блок пародонт — имплантат; 2 — блок имплантат — имплантат; 3 — единая конструкция протеза.
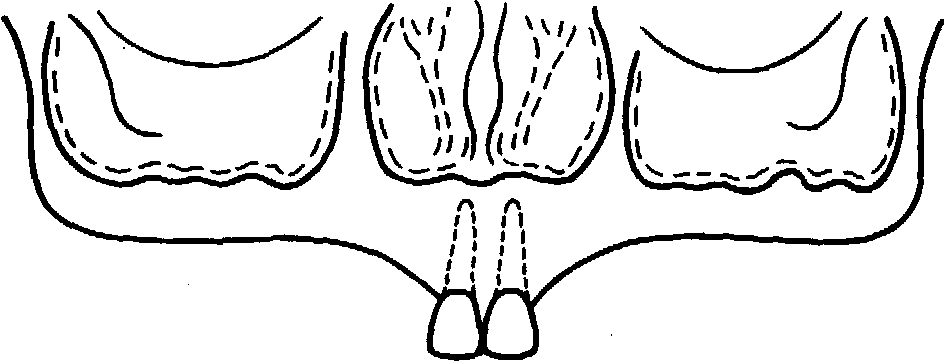
Рис.
152. Зона
введения импланта-та при близкорасположенной
к альвеолярному отростку верхнечелюстной
пазухе.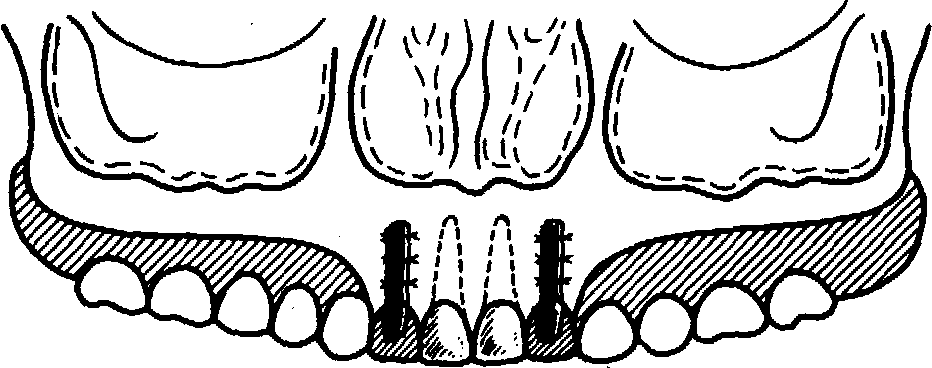
4. Искусственные зубы на базисе съемного протеза или в виде тела мостовидного протеза располагают на участках альвеолярного отростка, где нет условий для имплантации ' (рис. 152). Это правило распространяется на случаи неравномерной атрофии альвеолярных отростков, создающей неблагоприятные анатомо-топографические соотношения для имплантации (близость верхнечелюстных пазух, носовой полости и нижнечелюстного канала к альвеолярным гребням).
' Благоприятные условия для имплантации могут быть созданы по показаниям методом костной пластики.
429
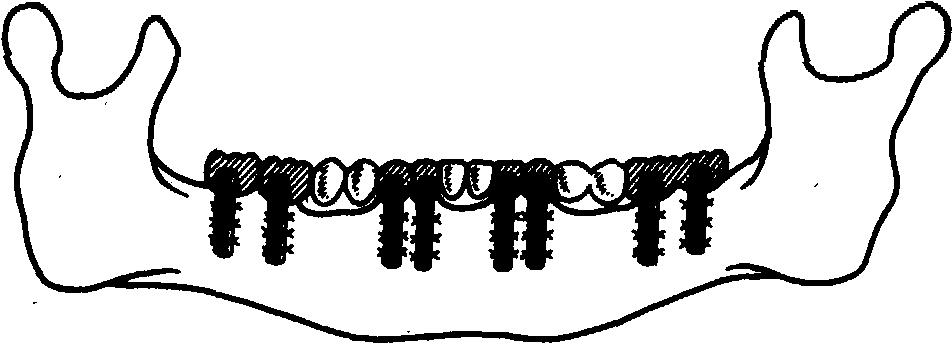
Рис.
153.
Стабилизация опор по дуге.
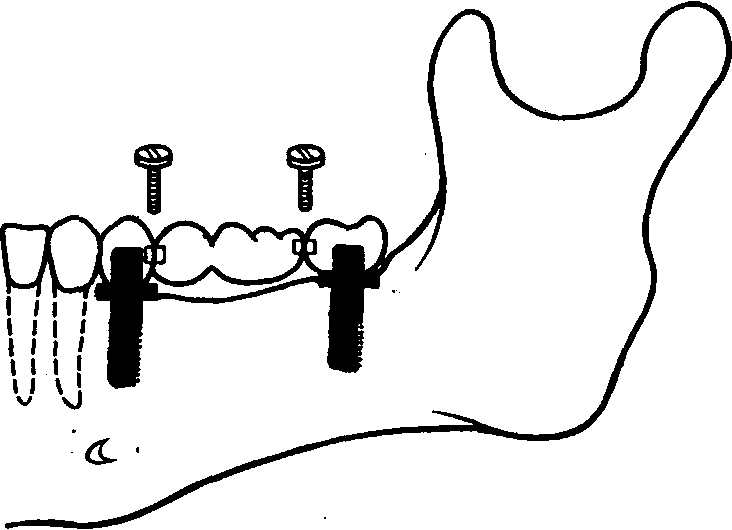
Пользуясь 'этими правилами, можно конструировать зубные протезы при любом виде дефектов зубного ряда по классификации Кеннеди, одиночном зубе и полном отсутствии зубов. Варианты конструкций представлены на рис. 155.
Рис.
154.
Разъемное соединение амортизатор с
помощью винта.
протезов через
ткани вокруг имплантата и происходит рефлекторная регуляция жевательного давления.с участием периодонта естественного зуба.
•Второе правило основано на том, что блокирование приводит к снижению концентрации напряжений в костной ткани вокруг имплантатов и создает резерв выносливости к нагрузке.
Третье правило — способность блоков пародонт — имплантат и имплан-тат — имплантат служить опорой мостовидных протезов с соотношением количества опор и искусственных зубов 1:1 —основано на результатах клинических наблюдений и известном положении: пародонт в норме может нести удвоенную нагрузку. Это положение распространено на блок имплантат — имплантат, который приравнен к одному естественному зубу.
Кроме указанных правил, при конструировании зубных протезов с использованием имплантатов необходимо учитывать характер межальвеолярных взаимоотношений. При большом пространственном расхождении центров альвеолярных гребней возникают биомеханические условия, неблагоприятные для функционирования имплантата. Например, при сагиттальном расхождении альвеолярных гребней стремление поставить передние зубы в несъемном мостовидном протезе по ортогнатическому прикусу приводит к резкому смещению осей имплантата и искусственного зуба, создавая неблагоприятную ситуацию для корневой части имплантата. В таких случаях целесообразно сделать выбор в пользу съемного протеза.
Воссоздание требуемой межальвеолярной высоты приводит к резкому увеличению внеальвеолярной части протеза. В таких случаях следует также отдавать предпочтение съемной конструкции, используя имплантаты лишь в качестве дополнительных опор, усиливающих фиксацию съемных протезов.
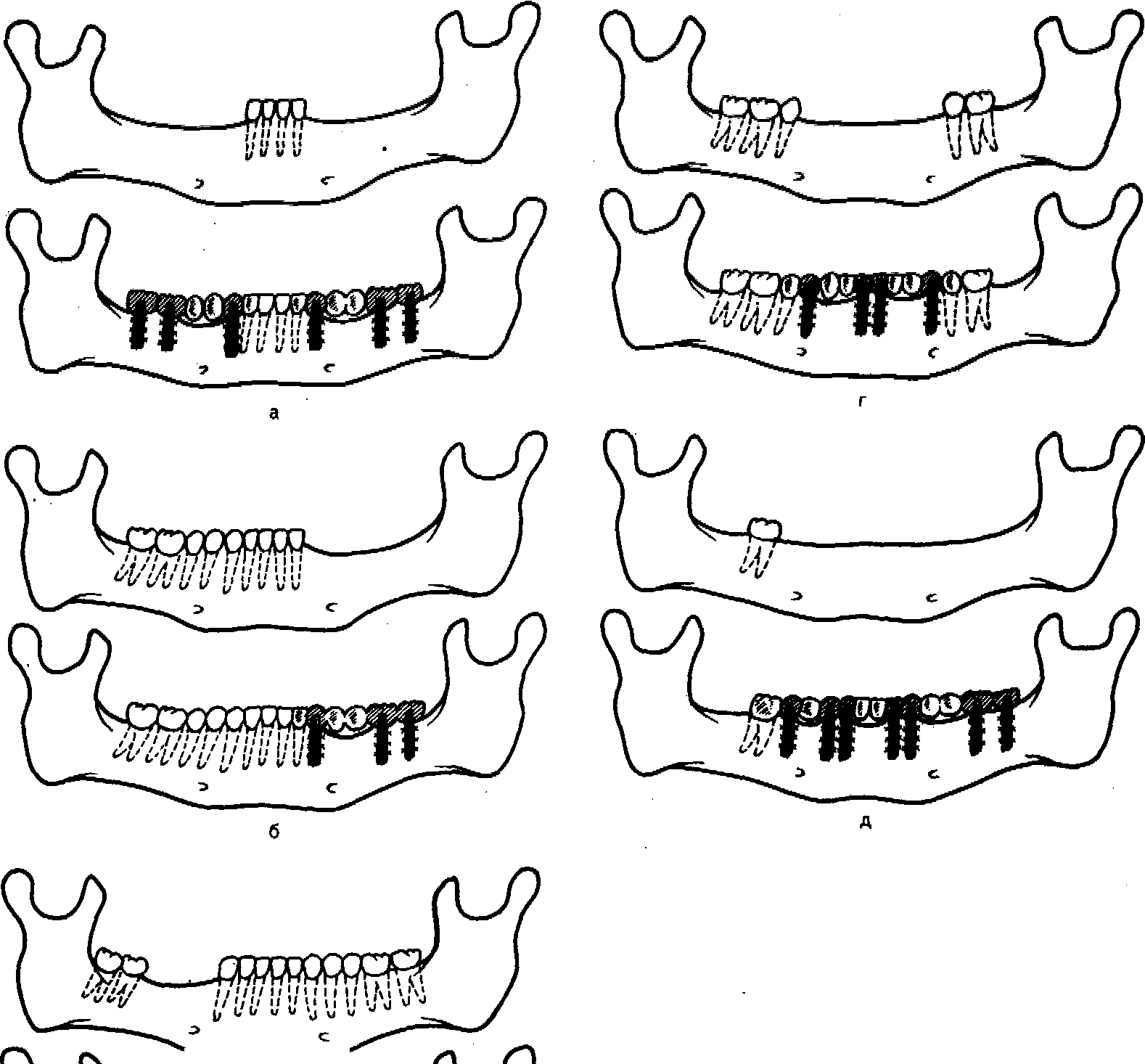
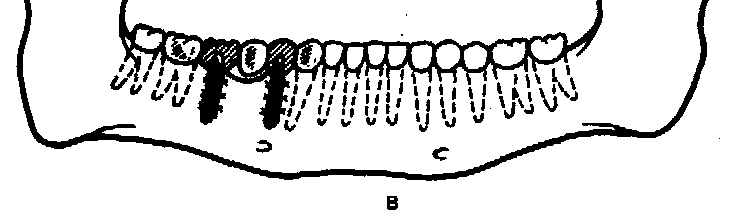
Рмс. 755. Варианты конструкций зубных протезов при различных видах дефекта зубного ряда.
а — при I классе дефекта; б — при II; в — при III; г — при IV классе; д — при одиночно сохранившемся зубе.
СПОСОБЫ ОРТОПЕДИЧЕСКОГО ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ ИМПЛАНТАТОВ
Способы протезирования зубов тесно связаны с методикой имплантации и конструкциями имплантатов, которые используют в качестве опор для зубных протезов. Однако, взяв в качестве классификационного признака послеоперационный срок нагружения имплантата зубным протезом, можно выделить два способа протезирования зубов — непосредственное и отсроченное.
Под непосредственным протезированием зубов с использованием имплантатов следует понимать способ, предусматривающий непосредственную, на операционном столе, фиксацию заранее изготовленного зубного протеза на естественных зубах и имплантатах. Этот способ можно применять при одномоментной методике имплантации и чрезвычайно точном совпадении параметров
431
опор, сконструированных на гипсовых моделях челюстей, с параметрами опор, полученными после имплантации. При непосредственном протезировании зубов с использованием имплантатов они немедленно подключаются к функциональной нагрузке. Процессы перестройки костной ткани и слизистой оболочки протекают в условиях механических нагрузок.
Под термином «отсроченное протезирование» мы понимаем такой способ, при применении которого протезирование начинают через определенный период времени после имплантации. Отсроченное протезирование зубов может быть ближайшим и отдаленным, причем ближайшим следует считать протезирование, проводимое через 1—2 нед после имплантации, отдаленным — через несколько месяцев. В этот период имплантаты зубным протезом не нагружают, они могут быть защищены каппами или другими приспособлениями. Отсроченное протезирование зубов может быть проведено при использовании любой методики имплантации, но более благоприятные условия возникают при двухфазной методике.
Разработанный нами комплект имплантатов и инструментов позволяет реализовать на практике оба способа протезирования зубов. Приводим описание этих способов.
Первый способ — непосредственное протезирование. Зубной протез изготавливают до имплантации и фиксируют на операционном столе после введения имплантатов в костное ложе.
Поскольку метод непосредственного постимплантационного протезирования зубов предусматривает изготовление протеза до операции, то особо важное значение приобретает точное совпадение расположения и параметров имплантатных опор, установленных на гипсовой модели, и имплантатов, которые будут установлены в челюстных костях во время операции. Такое совпадение может быть обеспечено за счет идентичного расположения имплантатов на моделях и в челюстных костях. Для этой цели служит базисная пластинка с направляющими втулками.
Создание костного ложа путем сверления по направляющим втулкам, установленным в пластинке строго по местоположению имплантатов, позволяет безошибочно решить задачу переноса конструкции с модели на челюсть, причем сверление кости следует проводить, начиная с малого диаметра сверла, и завершать его сверлом, соответствующим диаметру имплантата, соблюдая правила охлаждения.
Последовательность клинических и лабораторных этапов непосредственного протезирования зубов после однофазной имплантации с использованием комплекта имплантатов и инструментов системы «ПЦ-имплантаты» представлена в табл. 5. В ней четко выделены основные этапы: диагностика, планирование, изготовление непосредственного протеза, операция имплантации зуба и фиксация протеза на опорах. При этом для каждого этапа указаны необходимые инструменты, лабораторные приспособления и имплантаты, что облегчает освоение данного метода при работе с системой пористых цилиндрических имплантатов.
Модификацией непосредственного протезирования зубов с использованием имплантатов является способ, разработанный В. А. Воробьевым (1988). Им создана конструкция мостовидного протеза, состоящего из опорной коронки и цельнолитой части, включающей в себя искусственные зубы и имплантат, имеющий вид стержня диаметром около 3 мм с булавовидным утолщением на конце (рис. 156). Конструкцию изготавливают из серебряно-палладиевого сплава. Клинико-лабораторные этапы ее изготовления состоят в следующем:
препарируют зубы, служащие медиальной опорой мостовидного протеза, и изготавливают обычным способом искусственные коронки из серебряно-палладиевого сплава. После припасовки коронок больного переводят в хирургический
Таблица 5. Последовательность клинико-лабораторных этапов непосредственного протезирования зубов после однофазной имплантации |
|
Клинические и лабораторные этапы |
Перечень инструментов и имплантатов из системы *ПЦ-имплантаты» |
Диагностика |
|
Обследование больного с целью установления показаний и про |
|
тивопоказаний к имплантации; |
|
клиническое обследование |
|
дополнительные исследования (получение оттисков для изго |
|
товления диагностических моделей, рентгенография зубов и че |
|
люстей), функциональные исследования |
|
консультация других специалистов |
|
санация полости рта |
|
Анализ полученных данных, принятие решения |
|
Планирование |
|
Выбор типа имплантата, определение размеров и местоположе |
Измерительная планка, им- |
ния имплантатов по результатам измерений ортопантограм- |
плантаты: типы ПЦ-А, |
мы и моделей челюстей; пространственная ориентация имплан |
ПЦ-Б/А, ПЦ-ЭПФ |
тата по отношению к альвеолярному отростку, телу челюсти |
|
и оставшимся зубам, в первую очередь к опорным, с помощью |
|
параллелометра |
|
Изготовление базисной пластинки с направляющими втулками, |
Направляющие втулки (базис |
воспроизводящими пространственное положение имплантатов |
ные) стержни |
Изготовление непосредственного протеза |
|
Препарирование зубов, получение оттисков |
|
Изготовление моделей челюстей, шаблонов с прикусными вали |
|
ками |
|
Определение центрального соотношения зубных рядов, фиксация |
|
моделей челюстей в окклюдаторе |
|
Лабораторное изготовление опорных частей протеза |
|
Припасовка опорных частей на естественных зубах и получение |
|
оттисков |
|
Изготовление моделей челюстей с припасованными опорными |
Базисная пластинка с направ |
частями протеза и установка культовых штифтов с помощью |
ляющими втулками |
базисной пластинки с направляющими втулками |
|
Изготовление металлического каркаса протеза, моделирование |
|
зубов из воска и замена на пластмассу (при традиционной ме- |
|
таллопластмассовой технологии) либо изготовление металло- |
|
керамического или металлопластмассового протеза по совре |
|
менной технологии |
|
Имплантация |
|
Иссечение, отслаивание слиэисто-надкостничного лоскута |
Компостер, направляющие |
|
втулки (базисные), фигур |
|
ный нож |
Создание костного ложа |
Сверла, направляющие втул |
|
ки (базисные), шаблон-из |
|
меритель |
Введение имплантата в костное ложе |
Пинцет титановый, ударная |
|
головка, ударное устройство, |
|
устройство для охлаждения |
|
и деформации элементов с па |
|
мятью формы, держатель эле |
|
ментов имплантата, винт-за |
|
глушка, отвертки |
Фиксация зубного протеза на имплантатах и естественных зубах |
Соединительные винты (при ис |
|
пользовании типа ПЦ-А) |
16 Руков. по ортоп. стом. |
433 |
Рис.
156.
Мостовидный протез с дисталь-ной опорой
на имплантат из серебряно-палладиевого
сплава.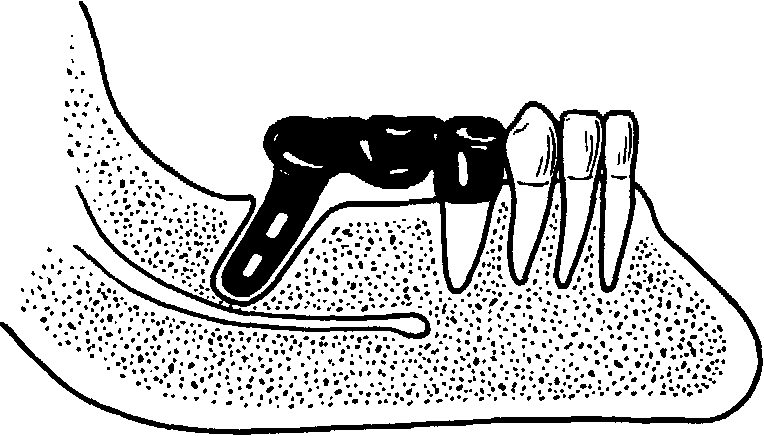
кабинет и осуществляют операцию создания искусственной лунки. Под проводниковой анестезией 2% раствором новокаина (тримекаина, лидокаина) производят разрез по альвеолярному гребню и отслаивают слизисто-надкостничный лоскут. Затем кортикальную пластинку у места введения имплантата перфорируют специальным инструментом (пробойником). В спонгиозной костной ткани формируется лунка для имплантата с помощью углового формирователя ложа и желобоватого долота. Костные опилки смывают раствором фурацилина и в образовавшуюся лунку устанавливают стерильный штифт, по форме и размеру соответствующий будущему имплантату. После этого снимают оттиск (штифт извлекают из лунки вместе с оттиском), рану промывают раствором фурацилина и тампонируют турундой с йодоформом.
В зубопротезной лаборатории по полученным оттискам изготавливают модели и загипсовывают их в окклюдатор. С боковой поверхности гипсовой модели вырезают углубление до штифта, который затем удаляют. На гипсовой модели моделируют недостающие зубы из воска, а в углублении — имплантат. Затем восковую композицию путем литья заменяют на серебряно-палладиевый сплав. Отливку обрабатывают, устанавливают на модель и припаивают к опорным коронкам. Готовый мостовидный протез стерилизуют и устанавливают на опорные зубы и в искусственную лунку, освобожденную от турунды и промытую раствором фурацилина. Фиксацию протеза на опорных зубах осуществляют с помощью фосфат-цемента.
Рассмотрим особенности отсроченного постимплантационного способа протезирования зубов. Его используют при ортопедическом лечении больных как с частичным, так и с полным отсутствием зубов. При этом могут быть применены и однофазная, и двухфазная методики имплантации. Однако использование двухфазной методики автоматически приводит к отсроченному протезированию через 4—6 мес после первой фазы.
Преимущество этого способа состоит в том, что репаративные процессы в первой фазе происходят в условиях изоляции от среды полости рта и без функциональных нагрузок на имплантат. Продолжительность первой фазы связана с процессами минерализации костной ткани. Длительность второй фазы небольшая, поскольку слизистая оболочка заживает значительно быстрее.
Последовательность клинико-лабораторных этапов отсроченного протезирования зубов после двухфазной имплантации с использованием системы «ПЦ-имплантаты» описана в табл. 6. В ней даны основные этапы: диагностика, планирование, операция имплантации зуба (I и II этапы), изготовление зубных протезов и их укрепление на естественных и искусственных зубах (рис. 157, 158).
В каждом этапе выделены основные клинико-лабораторные операции и специальные инструменты, необходимые для их выполнения. Однако следует обратить внимание на ряд важных моментов, существенно влияющих на исход лечения, в частности это относится к использованию базисной пластинки с
434
Таблица 6. Последовательность клинико-лабораторных этапов отсроченного протезирования зубов после двухфазной имплантации
Клинические и лабораторные этапы
Перечень инструментов и имплантатов из системы ЧЩ-имплантат»
Диагностика
Обследование больного с целью установления показаний и противопоказаний к имплантации:
клиническое обследование
дополнительные исследования (получение оттисков для изготовления диагностических моделей, рентгенография зубов и челюстей), функциональные исследования
направление на консультацию к другим специалистам
направление на санацию полости рта Анализ полученных данных, принятие решения
Планирование
Выбор типа имплантата, определение размеров имплантата и их местоположение в рамках планируемой конструкции протеза, окончательный выбор конструкции протеза
Изготовление базисной пластинки с направляющими втулками
Припасовка базисной пластинки в полости рта
Имплантация
Первая фаза
Иссечение, отслаивание слизисто-надкостничного
лоскута
Создание костного ложа
Введение имплантата в костное ложе
Закрытие послеоперационной раны Наблюдение в течение 4—6 мес
Вторая фаза Иссечение слизистой оболочки
над имплантатом
Удаление винта-заглушки. Соединение головки имплантата с корневой частью
Уход за раной мягких тканей и наблюдение (в течение 7 дней)
Изготовление зубных протезов
Препарирование зубов
Получение оттисков
Изготовление моделей челюстей
Определение центрального соотношения зубных рядов (челюстей)
Лабораторное изготовление опорных частей протеза
Припасовка опорных частей протеза в полости рта на имплантатах и естественных зубах
Окончательное изготовление зубного протеза в лаборатории
Укрепление зубного протеза на опорах
Наблюдение
Устранение осложнений
Типы ПЦ-А, ПЦ-Б/А, ПЦ-ЭГ1Ф, измерительная планка
Направляющие втулки (базисные) стержни
Компостер, направляющие втулки (базисные), фигурный нож
Сверла, направляющие втулки (базисные), шаблон-измеритель
Пинцет титановый, ударная головка, ударное устройство, устройство для охлаждения и деформации элементов с памятью формы, держатель элементов имплантата, винт-заглушка, отвертки
Базисная пластинка, съемный протез
Компостер, базисная пластинка с направляющими втулками, которая была использована в первой фазе имплантации
Отвертки, культя-амортизатор (головка имплантата)
Направляющие втулки (оттискные) Стержни-хвостовики, культовые стержни Направляющие втулки (базисные)
Модели челюстей с элементами из комплекта
Модели челюстей с элементами из комплекта Соединительные винты, отвертки
Приспособление для извлечения имплантата, нож для разрезания амортизатора
1б* 435

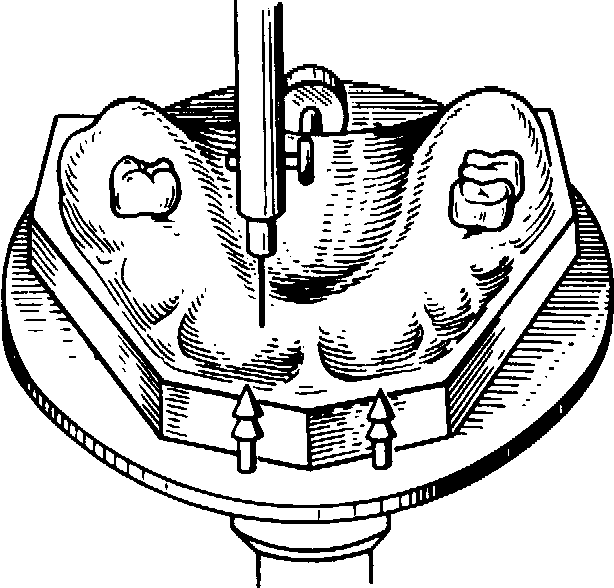


Рис. 157. Последовательность лабораторных этапов изготовления базисной пластинки с направляющими втулками для проведения имплантации. Объяснение в тексте.
направляющими втулками, введению имплантата с эффектом памяти формы. Так, мы считаем необходимым создавать костное ложе для внутрикостных опор с помощью базисных пластинок с направляющими втулками. Такие пластинки изготавливают по гипсовым моделям беззубых челюстей, где предварительно устанавливают штифты в местах локализации имплантатов. Использование пластинок с направляющими втулками позволяет создать костное ложе для имплантатов строго в заданных местах и правильно их ориентировать в челюстных костях.
Что касается введения имплантата с памятью формы, то перед введением его в костное ложе проволочные элементы с памятью формы подвергают пластической деформации. С этой целью имплантат охлаждают каким-нибудь хладагентом (стерильный замороженный фурацилин, изотонический раствор хлорида натрия, жидкий азот, хлорэтил и др.) и проволочные элементы, расположенные вертикально к оси имплантата, подгибают в имеющиеся углубления так, чтобы диаметр имплантата на данном участке не превышал диаметр других участков, свободных от проволочных элементов. В таком состоянии имплантат устанавливают в костное ложе, вколачивая его с помощью специального ударного устройства.
На следующем этапе, когда проводят раскрытие имплантатов (вторая фаза операции), используют ту же базисную пластинку с направляющими
436-
Рис.
158. Моменты
имплантации (а, б) и вид несъемного
мостовидного протеза (в).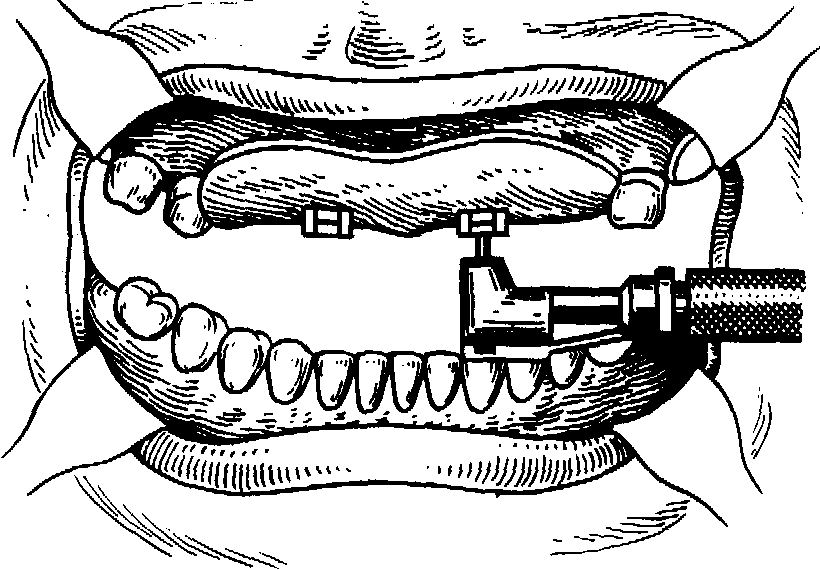

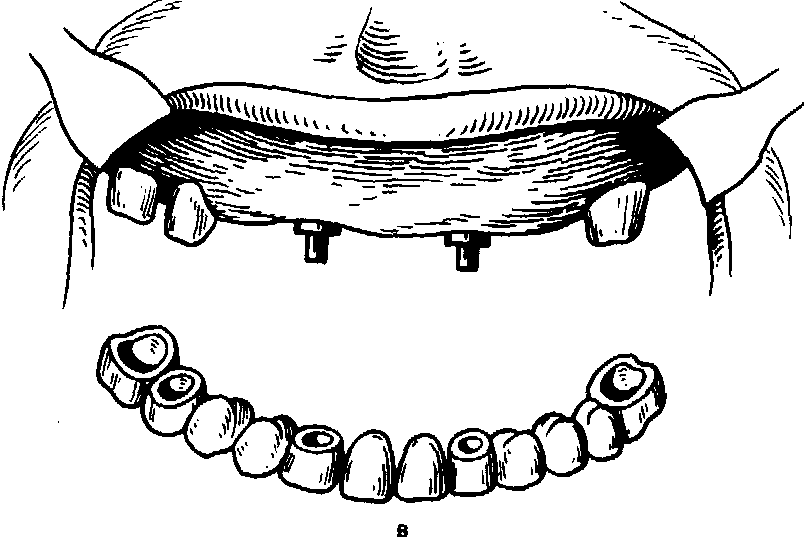
Способ отсроченного протезирования зубов с использованием двухфазной имплантации может быть применен и при концевых дефектах зубного ряда. Такой способ протезирования зубов при концевых дефектах зубного ряда нижней челюсти мостовидным протезом с дистальной опорой на цилиндрический (разборный) имплантат из титана с квазипористой поверхностью применила В. Н. Олесова (1986). В первой фазе под проводниковой анестезией 2—0,5% раствором тримекаина производят разрез слизистой оболочки и отслаивание слизисто-надкостничного лоскута у места установления имплантата. После этого в альвеолярном отростке,
используя ручные сверла из титана с известным диаметром (от 2,8 до 5 мм) и длиной (8, 10 и 12 мм), создают искусственную лунку, в которую с определенным усилием устанавливают корневую часть имплантата с ввинченной в центральный канал заглушкой. Рану ушивают кетгутовыми швами. Продолжительность фазы заживления 2—3 мес. По истечении этого срока в месте внедренного
437
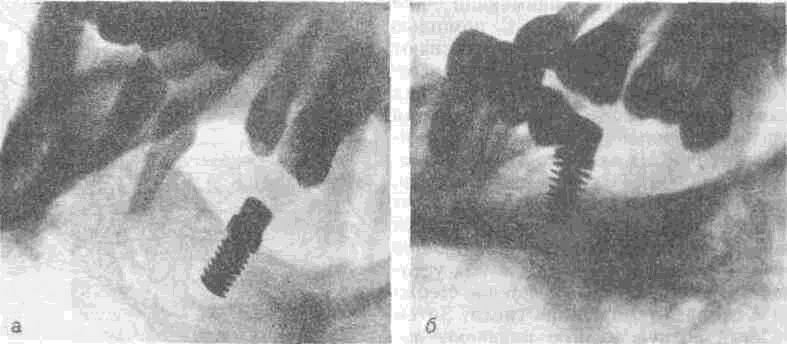
Рис. 159. Рентгенограммы дистального участка нижней челюсти.
а — внутрикорневая часть имплантата с головкой; б — мостовидный протез с дистальной опорой на имплантат.
имплантата слизистую оболочку перфорируют, заглушку удаляют и ввинчивают головку имплантата (рис. 159).
Препарирование естественного зуба, примерку коронок и изготовление колпачка на стандартную головку имплантата проводят в период приживления, что позволяет припасовывать их сразу же после фиксации головки имплантата и получать оттиски для изготовления мостовидного протеза, фиксацию которого осуществляют в ближайшие 2—3 дня.
В качестве примера ближайшего постимплантационного протезирования зубов можно привести методику, разработанную В. В. Трофимовым (1989). В качестве дополнительной опоры мостовидного протеза используют внутрикост-ный якорный имплантат (ВЯИ) из титана или серебряно-палладиевого сплава. Конструктивная форма ВЯИ в значительной мере отвечает анатомо-топографи-ческим условиям не только нижней, но и верхней челюсти, особенно она приемлема при выраженной атрофии альвеолярных отростков и резком уменьшении расстояния между альвеолярным гребнем и верхнечелюстной пазухой или нижнечелюстным каналом. По своей конструкции ВЯИ разборный, состоит из саблевидных стержней, поперечной опорной планки, колпачка.
Обработку операционного поля проводят 1 % раствором диоксида, проводниковую анестезию — 2% раствором тримекаина с добавлением вазопрессоров.
Доступ к поверхности альвеолярного отростка челюсти обеспечивают двумя сходящимися разрезами слизистой оболочки и надкостницы вдоль гребня альвеолярного отростка и перпендикулярно к переходной складке.
Отслаивают треугольный слизисто-надкостничный лоскут и обнажают альвеолярный отросток в месте предполагаемой имплантации. С помощью сверла на малых оборотах (не более 30 об/мин) проводят перфорацию кортикальной пластинки на вершине альвеолярного гребня. Этим же сверлом в зоне предполагаемого введения имплантата формируют направляющий канал глубиной до 2 мм.
На перфорированное отверстие кортикальной пластинки накладывают опорную планку. На дистальное отверстие опорной планки, совмещенное с направляющим каналом, устанавливают сегмент имплантата в виде саблевидно-изогнутого стержня и легкими толчками через ударное приспособление вводят в кость челюсти. Через медиальное отверстие опорной планки, выполняющей
438
роль матрицы, формируют направляющий канал в противоположном направлении от дистального стержня, в который вводят второй сегмент (стержень) имплантата. Оба сегмента (стержня) погружают в кость до тех пор, пока стопорные кольца не упираются в наружную поверхность опорной планки, Выступающие наддесневые части сегментов имплантата сводят и укрепляют колпачком.
Слизисто-надкостничный лоскут возвращают на место и фиксируют узловатыми швами из полиамидной нити. На верхней челюсти костная ткань менее компактна, чем на нижней, поэтому часто отсутствует необходимость в формировании направляющих каналов. Сегменты (стержни) вводят через отверстия опорной планки, наложенной на кость альвеолярного гребня с помощью ударного приспособления.
В послеоперационном периоде осуществляют мероприятия, направленные на ликвидацию местных воспалительных проявлений. Назначают гипосенсиби-лизирующие, седативные и противовоспалительные препараты (димедрол, фенобарбитал, метиндол и антисептические жидкости), проводят физиотерапевтические процедуры. Антибактериальные препараты назначать нецелесообразно.
После заживления операционной раны (7—12-е сутки после операции) проводят ортопедический этап лечения. Препарируют опорные зубы (не менее двух) под коронки и получают оттиски с обеих челюстей. В лаборатории изготавливают коронки на опорные зубы и имплантат. В клинике коронки припасовывают и, если имеется необходимость, определяют высоту прикуса. В лаборатории изготавливают мостовидный протез, который проверяют и припасовывают в полости рта пациента. После этого его дорабатывают в лаборатории и фиксируют на опорные зубы и имплантата с помощью висфат-цемента.
Отсроченное протезирование зубов может быть проведено и после одномоментной имплантации. В таких случаях перед окончательным протезированием используют временные протезы или защитные фиксирующие приспособления.
На том или ином этапе лечения больных с использованием имплантатов могут возникать осложнения. Во время операции могут возникнуть кровотечение, повреждение нервов, перфорация стенки верхнечелюстной пазухи или носовой полости, повреждение соседних зубов, перелом альвеолярного отростка, поломка имплантата или инструмента в кости, невозможность достижения первичной стабильности имплантата.
К послеоперационным осложнениям относятся отек, гематома, инфекция, подвижность имплантата, резорбция костной ткани вокруг имплантата, повреждение нервов, поломка имплантата, прободение десны.
В процессе пользования зубными протезами могут возникнуть поломки протеза, часто в местах соединения с имплантатом, патологические изменения в пародонте или твердых тканях естественных зубов, включенных в конструкцию протеза, воспаление слизистой оболочки, пролежни.
Имплантологи должны предупредить больных о возможности таких осложнений, одновременно принимая все меры к их предупреждению и устранению, если они возникнут вопреки всем профилактическим мероприятиям.
Основой профилактики осложнений являются правильное определение показаний к имплантации, точная диагностика и планирование всех этапов комплексного лечения, безупречная оперативная и зубопротезная техника, неукоснительное соблюдение больным правил пользования зубным протезом, тщательный уход за полостью рта.
Более удобными с точки зрения устранения осложнений являются разборные протезы, которые позволяют, не разрушая всю конструкцию, заменить элементы, вызвавшие те или иные осложнения.
439
ТЕХНОЛОГИЧЕСКИЕ ОСОБЕННОСТИ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТОВ
По способу изготовления имплантаты могут быть разделены
группы: заводского производства (стандартные) и лабораторного изготовлени (стандартные и индивидуальные).
Первая группа имплантатов может быть приобретена через систему медр пинского снабжения, а вторая — изготовлена в условиях зуботехническо лаборатории, дополнительно оснащенной соответствующим оборудование» инструментами и материалами.
В зависимости от материала, из которого изготавливают имплантать могут быть использованы различные технологии: литье (КХС, серебрянс палладиевые сплавы, титан и его сплавы и др.), спекание (керамика, керметы) механическая или электроискровая обработка (титан, никелид титана, сапфиры углерод и др.), методы порошковой металлургии и самораспространяющегося высокотемпературного синтеза (СВС) (титан, никелид титана).
Нами разработаны четыре способа изготовления внутрикостных импланта тов из титана и сплавов на основе никелида титана [Миргазизов М. 3. др., 1988].^
Первый способ: по стандартным или индивидуальным размерам методом литья или механической обработки изготавливают беспористую основу имплан тата, на которую затем наносят пористое покрытие методом порошковой металлургии или СВС (рис. 160).
Второй способ: методом порошковой металлургии или СВС получают из титана или никелида титана пористую заготовку цилиндрической, пластинчатой трубчатой формы. Из этой заготовки изготавливают имплантат любой конструк ции методом механической или электроискровой обработки (рис. 161).
Третий способ: методом порошковой металлургии или СВС сразу, исключая этап механической обработки, получают имплантат по стандартным или индиви дуальным пресс-формам (рис. 162).
Четвертый способ заключается в поэлементном изготовлении имплантата беспористого стержня, пористых корневых колец, пришеечных колец, колец с имитаторами периодонтальных связок из проволоки с памятью формы
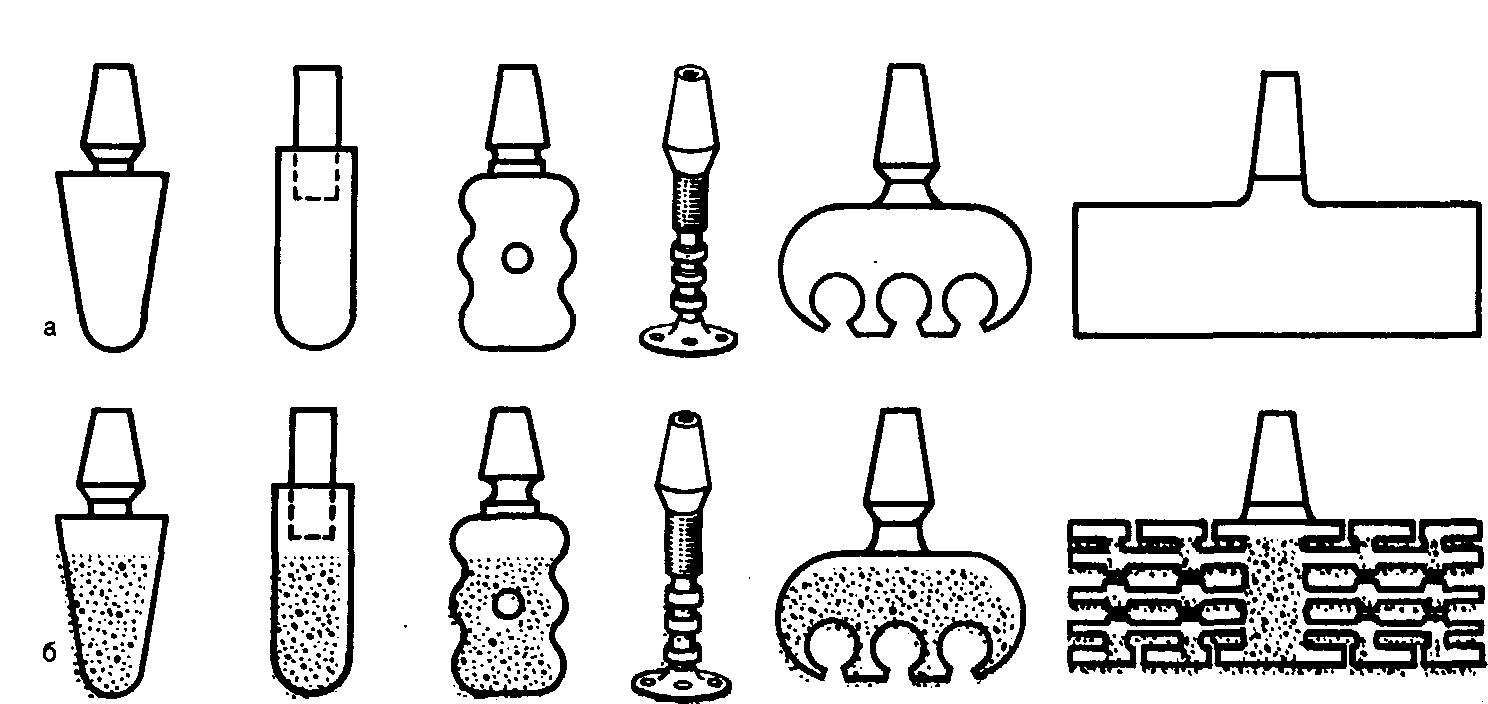
Рис. 160. Общий вид имплантатов, изготовленных первым способом. а — до нанесения пористого покрытия; б — после его нанесения.
14П
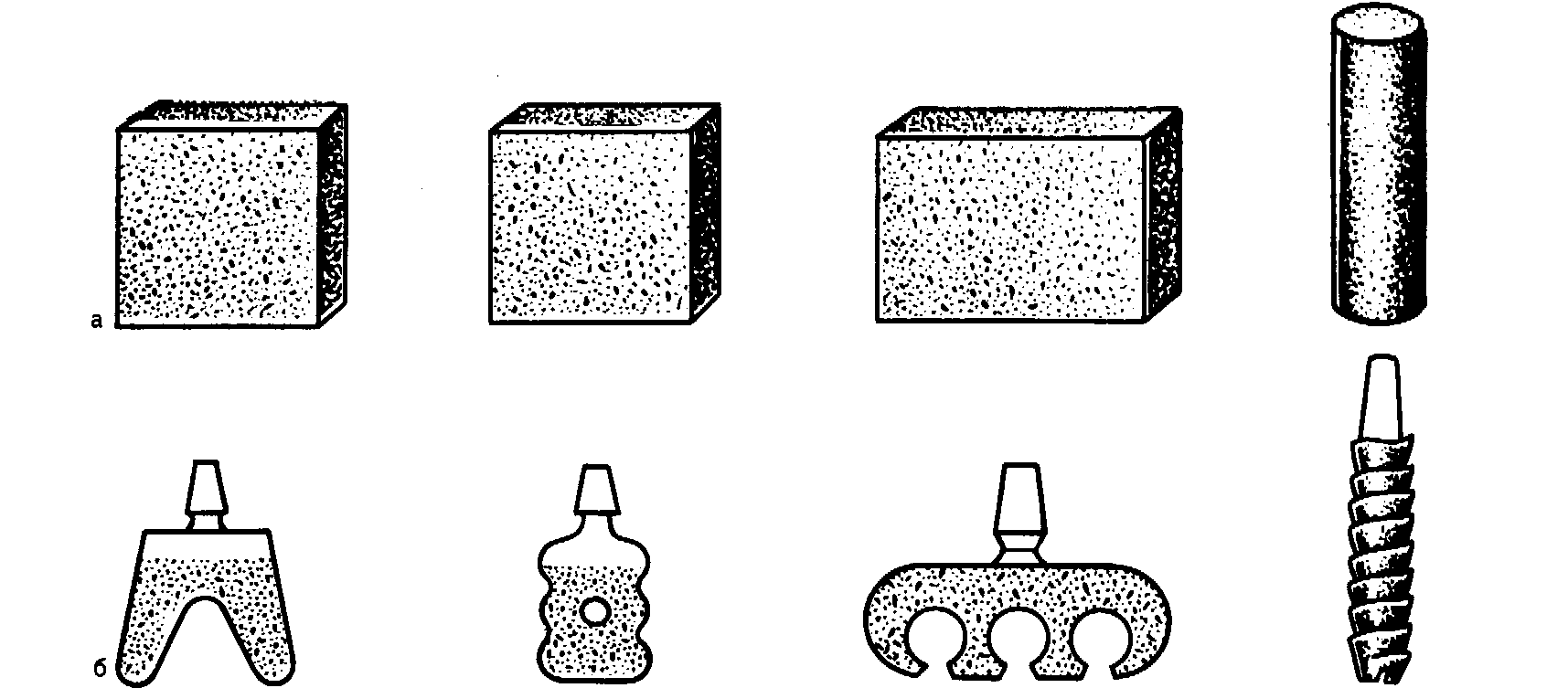
Рис. 161. Общий вид имплантатов, изготовленных вторым способом. а — заготовки; б — имплантаты, изготовленные из этих заготовок.
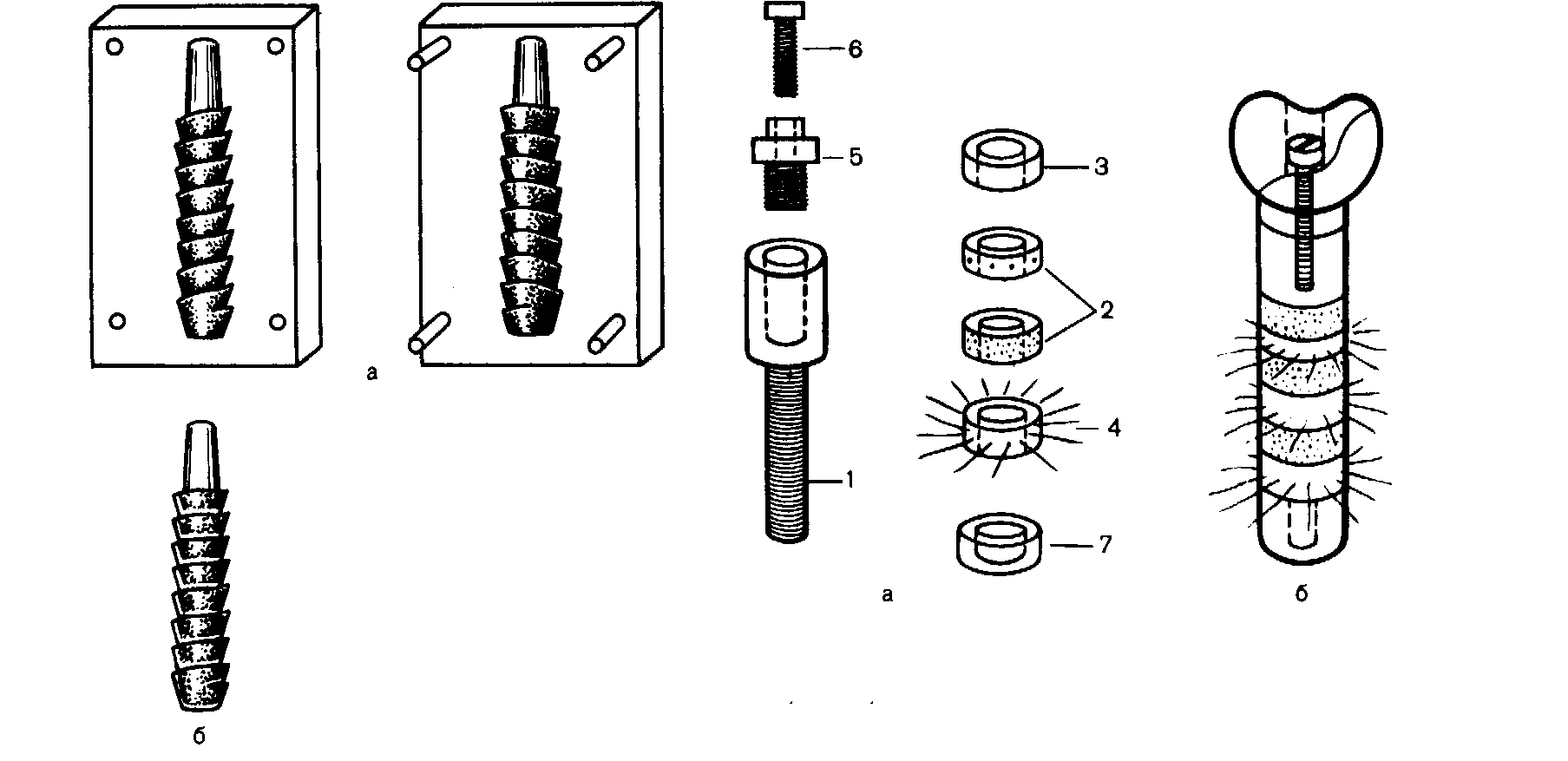
а — пресс-форма; б — имплантат.
Рис. 163. Общий вид имплантатов, изготовленных четвертым способом.
а — элементы имплантата; 1 — беспористый стержень; 2 — пористые корневые кольца; 3 — пришеечные кольца; 4 — кольца с имитаторами периодонтальных связок из проволоки с памятью формы; 5 — амортизатор; б — соединительный винт; 7 — шаровидная гайка; б — имплантат в собранном виде.
амортизатора, соединительных винта и гайки. Пористые корневые кольца могут быть изготовлены из пористого титана, никелида титана, гидроксилапатита, керамики, кермета и др. Пришеечные кольца изготавливают из беспористого титана, гидроксилапатита, никелида титана, стеклокерамики, сапфира и др. Путем сборки из перечисленных элементов можно создать имплантат требуемой конструкции и величины (рис. 163).
441
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ОРТОПЕДИЧЕСКОГО ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ ИМПЛАНТАТОВ '
Протезирование зубов с использованием имплантатов является комплексным методом лечения стоматологических больных с различными видами дефектов зубных рядов. Его осуществляет бригада специалистов, состоящая из двух врачей-стоматологов (хирурга и ортопеда) и одного зубного техника.
В соответствии с приказом Минздрава СССР от 4 марта 1986 г. № 310 «О мерах по внедрению в практику метода ортопедического лечения с использованием имплантатов» в стоматологических учреждениях организуются отделения стоматологической имплантации. В системе указанных учреждений в пределах общей численности должностей, предусмотренных для стоматологических учреждений области (края, республики), вводятся должности медицинского персонала (стоматолог-ортопед, два зубных техника, операционная медицинская сестра).
Для проведения хирургического этапа имплантации в стоматологических отделениях многопрофильных больниц выделяется от 3 до 5 коек.
Координацию научных исследований по имплантологии осуществляет проблемная комиссия 30.04 «Ортопедическое лечение и протезирование дефектов и деформаций зубочелюстной системы» Научного совета по стоматологии АМН СССР и ЦНИИС.
Опыт работы показывает, что эффективность ортопедического лечения с применением имплантатов сдерживается в настоящее время следующими факт-торами.
1. Отсутствием фундаментальных исследований проблем оссеоинтеграции применительно к имплантатам из металлических и неметаллических материалов.
2. Несовершенством методов, отсутствием специальных инструментов и устройств для обработки костного ложа имплантата при хирургической процедуре; необходимостью комплексной разработки проблем малотравматичного i препарирования костной ткани при установке имплантата и разработки основ для проектирования и освоения промышленностью специальных комплектов ;
хирургического инструмента.
3. Отсутствием региональных статистических данных о потребностях в лечении этого типа, что исключает объективное прогнозирование потребности и оценки показаний к этому виду лечения в каждом конкретном случае.
4. Недостаточным уровнем информации, необходимой стоматологу для определения тактики оперативного вмешательства, выбора конструкции и разме- ' ров имплантата и вида протеза.
С целью координации научных исследований и практического внедрения методов имплантологии в отечественную практику ЦНИИС разработал комплексную научно-техническую программу работ на период 1987—1990 гг. Программа предусматривает решение следующего комплекса основных проблем.
1. Объективизация клинических показаний, разработка принципов отборам предоперационной диагностики пациентов для ортопедического лечения с применением имплантатов и критериев оценки их функционирования.
2. Разработка и совершенствование хирургической техники имплантации;
конструирование имплантатов и зубных протезов с учетом биомеханики зубочелюстной системы; углубленное изучение вопросов оссеоинтеграции имплантатов из металлических и неметаллических материалов и биосовместимости имплантатов и протезных конструкций с тканями полости рта.
3. Создание, экспериментально-клинические испытания и внедрение имплантатов, протезных конструкций, специального инструментария и методов, обес-
Раздел написан руководителем отделения имплантологии ЦНИИС А. И. Матвеевой.
442
печивающих проведение всего цикла протезирования с использованием имплан-татов, в том числе сравнительные испытания отечественных и зарубежных образцов.
4. Проблемы лечения в послеоперационном и отдаленном периоде и профилактики осложнений при имплантации; исследование и разработка биомедицинских, технических и технологических путей повышения эффективности протезирования с использованием имплантатов.
5. Организационно-методическое, опытно-производственное и промышленное обеспечение внедрения имплантатов в клиническую стоматологию.
Комплексная программа предполагает применение современных биологических, биофизических, биомеханических, морфометрических методов исследования экспериментального материала и морфофункциональной оценки результатов клинических наблюдений, а также проведение комплекса проектно-кон-структорских и технологических разработок по обеспечению хирургического и ортопедического этапов лечения с учетом отечественного и зарубежного опыта.
На основании результатов проведенных исследований, проектных и опытно-конструкторских работ планируют разработку показаний и критериев оценки состояния зубочелюстной системы пациента и принципов протезирования с использованием имплантатов; разработку щадящих хирургических вмешательств при различных анатомо-топографических особенностях зубочелюстной системы пациента; решение основных проблем оссеоинтеграции имплантатов из различных материалов с учетом биосовместимости и биомеханики имплантатов; экспериментальное и клиническое изучение рациональных методов, систем имплантатов, инструментария и протезных конструкций; разработку, создание и внедрение отечественных систем имплантатов, протезных конструкций и инструментария в ортопедическую практику; изучение послеоперационных и отдаленных этапов протезирования с использованием имплантатов; разработку биомедицинских, технических и технологических мероприятий повышения эффективности ортопедического лечения; разработку комплекса мер по профилактике осложнений на всех этапах лечения с применением имплантатов; внедрение методических рекомендаций по протезированию с применением имплантатов; выпуск нормативных документов на клиническое внедрение этого вида лечения, в том числе стандартов; организацию серийного производства имплантатов, комплектов инструментов и приборов.
