
- •Предисловие
- •Основные меры безопасности при работе в лаборатории
- •Запись эксперитентальных данных
- •Введение
- •Тема 1. Аминокислоты. Белки
- •Лабораторная работа №1 цветные реакции на белки и аминокислоты. Осаждение белков
- •Контрольные вопросы и задания
- •Тема 2. Ферменты
- •Лабораторная работа №2 свойства ферментов
- •Контрольные вопросы
- •Тема 3. Витамины
- •Лабораторная работа №3 качественные реакции на витамины
- •Контрольные вопросы
- •Тема 4. Углеводы
- •Лабораторная работа №4 свойства углеводов
- •Контрольные вопросы
- •Тема 5. Липиды
- •Лабораторная работа №5 свойства жиров
- •Контрольные вопросы
- •Тема 6. Минеральные вещества организма и их обмен
- •Лабораторная работа №6 качественное определение неорганических соединений костной ткани
- •Контрольные вопросы
- •Литература
- •Рекомендуемая литература
- •398020, Г. Липецк, ул. Ленина, 42
Лабораторная работа №3 качественные реакции на витамины
Опыт №1. Реакция витамина А с сульфатом железа (II)
К 1-2 каплям рыбьего жира или 0,05%-ного раствора витамина А в хлороформе добавляют 5-10 капель ледяной уксусной кислоты, насыщенной сульфатом железа (II) и 1-2 капли концентрированной серной кислоты. Появляется голубое окрашивание, постепенно переходящее в розово-красное. Каротины дают при этой реакции зеленое окрашивание.
Опыт №2. Реакция витамина А с серной кислотой
1 каплю рыбьего жира растворяют в 4-5 каплях хлороформа и прибавляют 1 каплю концентрированной серной кислоты. Появляется голубое окрашивание, быстро переходящее в буро-красное.
В основе приведенной реакции лежит способность серной кислоты отнимать от витамина А воду с образованием цветных продуктов реакции.
Опыт №3. Реакция витамина В1 с диазореактивом
К 5 каплям основного раствора сульфаниловой кислоты прибавляют 5 капель 5%-ного раствора нитрита натрия. К полученному раствору диазореактива добавляют небольшое количество (на кончике шпателя) тиаминхлорида и 5-7 капель 10%-ного раствора карбоната натрия. Жидкость окрашивается в оранжево-красный цвет.
Опыт №4. Реакция витамина С с гексацианоферратом (III) калия
Аскорбиновая кислота, окисляясь, восстанавливает гексацианоферрат (III) калия до гексацианоферрата (II) калия, который с ионом железа в степени окисления +3 образует в кислой среде осадок синего цвета – «берлинскую лазурь».

![]()
К 1 мл раствора витамина С прибавляют 2 капли раствора гидроксида калия, 2 капли раствора гексацианоферрата (III) калия и энергично встряхивают содержимое пробирки. Затем в пробирку добавляют 6-8 капель 10%-ного раствора соляной кислоты и 1-2 капли раствора хлорида железа (III). Выпадает синий или зеленовато-синий осадок.
Контрольные вопросы
1. Роль витаминов в жизнедеятельности организма.
2. Жирорастворимые витамины, их строение и физиологическая роль.
3. Водорастворимые витамины В1, В2, В6 и С, их строение, химическая природа и физиологическая роль.
4. Коферменты, их функции.
Тема 4. Углеводы
Углеводы можно считать основой существования большинства организмов. В таких углеводах как сахара и крахмал заключено основное количество калорий, получаемых с пищей человеком и почти всеми животными. Углеводы используются как временные депо глюкозы; выполняют функции структурных и опорных элементов в клеточных стенках бактерий и растений, в соединительной ткани и оболочках клеток животных; служат в качестве смазки в суставах; обеспечивают слипание клеток.
Различают 3 основных класса углеводов: моносахариды, олигосахариды и полисахариды.
Моносахариды или простые сахара содержат только одну структурную единицу альдегидо- или кето-многоатомного спирта. По числу атомов углерода моносахариды подразделяются на триозы, тетрозы, пентозы, гексозы и т.д. Среди природных моносахаридов наиболее распространены D-глюкоза (гексоза, альдоза), D-фруктоза (гексоза, кетоза).

D-глюкоза α- D-глюкопираноза

D-фруктоза β-D-фруктофураноза
Олигосахариды – вещества, образованные несколькими моносахаридными единицами, соединенными ковалентными связями. Наиболее часто встречаются дисахариды, состоящие из 2-х моносахаридных единиц. Типичный представитель дисахаридов – сахароза, молекулы которой содержат остатки D-глюкозы и D-фруктозы.

Сахароза
При образовании дисахарида одна молекула моносахарида образует связь с другой молекулой за счет своего гликозидного гидроксила. Вторая молекула моносахарида участвует в образовании связи двумя путями: 1) спиртовым гидроксилом:
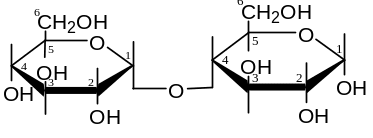
Мальтоза
α-D-глюкопиранозил-(1→4)- α-D-глюкопираноза
2) гликозидным гидроксилом:
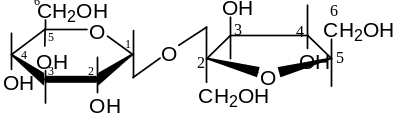
Сахароза
α-D-глюкопиранозил-(1→2)- β-D-фруктофураноза
В первом случае в молекуле дисахарида остается свободным гликозидный гидроксил, благодаря чему эти дисахариды обладают восстанавливающими свойствами (мальтоза). Во втором случае в молекуле дисахарида нет свободного гликозидного гидроксила, вследствие чего он лишен восстанавливающих свойств (сахароза). Гликозидные связи легко гидролизуются кислотами.
Полисахариды представляют собой длинные цепи, образованные сотнями или тысячами моносахаридных единиц. Наиболее распространенные в растительном мире углеводы – крахмал и целлюлоза - образованы остатками D-глюкозы. Различие между ними состоит лишь в способах связи остатков D-глюкозы между собой.


В полисахаридах гликозидный гидроксил одной молекулы моносахарида соединен со спиртовым гидроксилом второй молекулы через гликозидную связь. Полисахариды имеют свободный гликозидный гидроксил на большое число связанных молекул моносахарида, поэтому практически, они не проявляют восстанавливающих свойств. При полном гидролизе под действием кислоты или специфических ферментов полисахариды расщепляются с образованием моносахаридов или их производных.
Крахмал представляет собой смесь двух полимеров глюкозы – амилозы и амилопектина. α-Амилоза состоит из длинных неразветвленных цепей, содержащих остатки D-глюкозы, соединенные друг с другом 1,4-связями.
Цепи амилопектина сильно разветвлены.
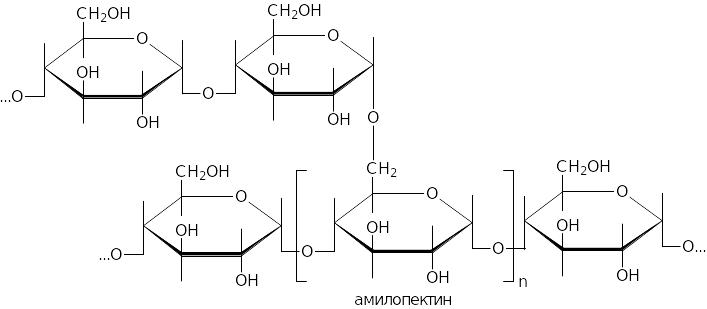
Гликоген – основной резервный полисахарид в клетках животных. Это разветвленный полисахарид, состоящий из остатков D-глюкозы. В желудочно-кишечном тракте гликоген и крахмал гидролизуются, высвобождая D-глюкозу и небольшое количество мальтозы. В клетках животных гликоген подвергается ферментативному фосфоролизу с образованием не глюкозы, а глюкозо-1-фосфата.
