
- •Раздел III. Равновесные электродные процессы
- •Величины, характеризующие энергетическое состояние заряженных частиц
- •Эдс как сумма гальвани-потенциалов
- •Эдс как сумма вольта-потенциалов
- •Теория возникновения электродного потенциала и эдс
- •Гальвани-потенциал на границе двух металлов
- •Гальвани-потенциал на границе металл – раствор Осмотическая теория Нернста
- •Сольватационная теория электродного потенциала
- •Классификация электродов
- •Электроды первого рода
- •Электроды второго рода
- •Электроды третьего рода
- •Газовые электроды
- •Амальгамные электроды
- •Окислительно-восстановительные, или редокси-электроды
- •Физические цепи
- •Концентрационные цепи
- •Химические цепи
- •Аккумуляторы
- •Электрокинетические явления
- •Электрокапиллярные явления
- •Потенциалы нулевого заряда и нулевые точки металлов
- •Теория конденсированного двойного слоя Гельмгольца
- •Теория диффузного двойного слоя Гуи – Чапмана
- •Адсорбционная теория Штерна
- •Дальнейшее развитие теории строения дэс
Химические цепи
Химические цепи принято разделять на простые и сложные. В простых химических цепях один из электродов обратим по отношению к катионам электролита, а другой к его анионам. В сложных химических цепях это условие не соблюдается.
Простые химические цепи. В водородно-кислородном элементе
М1 Н2 Н2О О2 М2
источником электрической энергии служит химическая энергия реакции между кислородом и водородом с образованием воды
Н2 + 1/2 О2 = Н2О .
Выражение для ЭДС водородно-кислородного элемента имеет вид
Е
= Ео
+
ln
![]() .
.
К этому же уравнению можно прийти, рассмотрев частные электродные реакции. На водородном электроде протекает реакция ионизации водорода
Н2 = 2Н+ + 2е ,
а на кислородном реакция ионизации кислорода с образованием гидроксильных ионов
1/2 О2 + Н2О + 2е = 2ОН– .
Сумма электродных реакций дает общую реакцию в химической цепи
Н2 + 1/2 О2 + Н2О = 2Н+ + 2ОН– ;
Е
= Ео
+
ln
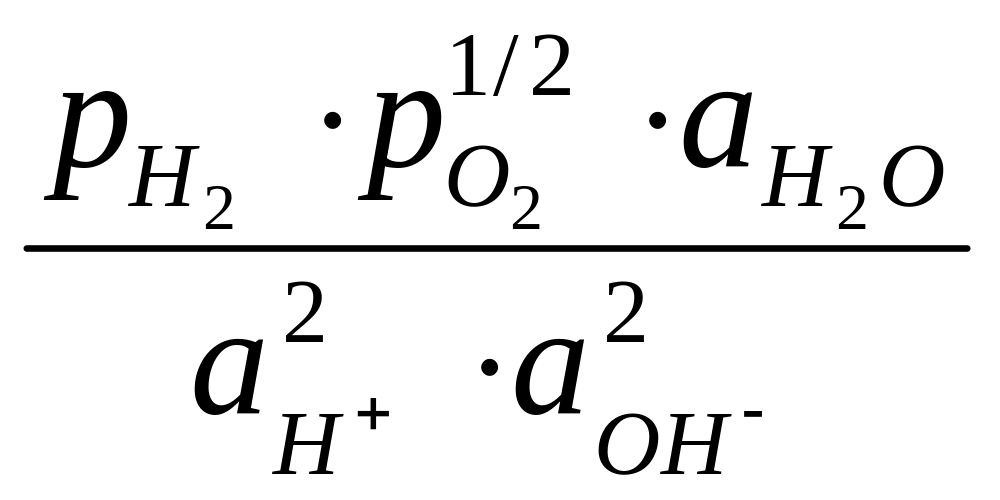 .
.
Преобразуем
выражение, положив
![]() = 1 и учтя, что
= 1 и учтя, что
![]() = Kw
:
= Kw
:
Е = Ео ln Kw + ln .
Полученное выражение совпадает с вышеприведенным выражением для ЭДС при
Ео = Ео ln Kw .
При
25оС
Ео
=
![]() +
+
![]()
ln
Kw
=
ln
Kw
=
= 0 + 0,401 0,059 lg 10-14 = 0,401 + 0,829 = 1,230 В ;
Е = 1,230 + 0,03 lg .
Видно, что ЭДС водородно-кислородного элемента зависит от парциальных давлений водорода и кислорода, увеличиваясь с их ростом по логарифмическому закону. Она не зависит от рН среды и должна быть одной и той же в чистой воде и в растворах щелочи или кислоты. Так как электропроводность чистой воды очень низка, то на практике применяют растворы щелочи, чаще всего раствор КОН:
М1 Н2 КОН О2 М2 .
Другим примером простых химических цепей может служить стандартный элемент Вестона
Pt Hg, Cd CdSO4 Hg2SO4 Hg Pt ,
ЭДС которого отличается очень большим постоянством во времени и малым температурным коэффициентом. В элементе Вестона левый электрод обратим по отношению к ионам кадмия
Cd = Cd2+ + 2e ,
а правый по отношению к сульфат-ионам
Hg2SO4 + 2e = 2Hg + SO42– .
Общая реакция, протекающая в элементе:
Cd + Hg2SO4 = Cd2+ + SO42– + 2Hg .
При учете постоянства активностей твердых веществ ЭДС элемента Вестона описывается уравнением
Е
= Ео
ln
![]() = Ео
ln
= Ео
ln
![]() .
.
Следовательно, его ЭДС определяется активностью раствора сульфата кадмия. В электрохимической практике для измерения ЭДС компенсационным методом чаще всего применяют элементы Вестона с насыщенным раствором CdSO4. Амальгамный электрод в таком элементе содержит 12,5% кадмия. ЭДС насыщенного элемента Вестона при Т, близкой к комнатной, находят по уравнению
Et = 1,0183 4,010–5 (t 20) .
Третьим примером простых химических цепей может служить свинцовый, или кислотный, аккумулятор (см. ниже, «Аккумуляторы»).
Простые химические цепи – цепи без переноса. Однако подавляющее большинство химических цепей – это цепи с переносом, в которых растворы соединены или непосредственно, или через солевой мостик. Комбинируя различные окислительно-восстановительные полуреакции, можно построить очень большое число химических цепей. Разность соответствующих стандартных потенциалов позволяет в первом приближении оценить ЭДС этих цепей. Точное значение ЭДС химических цепей с переносом рассчитать не удается, во-первых, из-за невозможности точного определения диффузионного потенциала, и во-вторых, из-за неизбежной замены активностей отдельных ионов в формуле Нернста средними активностями или просто концентрациями этих ионов.
Сложные химические цепи. Примером сложных химических цепей является элемент Даниэля – Якоби
Zn ZnSO4¦CuSO4 Cu ,
в котором протекает реакция
Zn + Cu2+ = Zn2+ + Cu .
Левый электрод отрицательный полюс элемента обратим по отношению к ионам цинка, а правый положительный полюс элемента по отношению к ионам меди. ЭДС элемента Даниэля – Якоби зависит поэтому от отношения активностей ионов меди и цинка:
Е
= Ео
+
ln
![]() .
.
В этом элементе имеется граница между двумя растворами, на которой возникает диффузионный потенциал, поэтому ЭДС элемента в действительности сложнее. Однако, поскольку подвижности ионов меди и цинка не слишком отличаются друг от друга и концентрации сульфата меди и цинка близки между собой, диффузионный потенциал не играет существенной роли в создании ЭДС этого элемента.
Сдвоенные химические цепи. В сдвоенных химических цепях две простые химические цепи, отличающиеся лишь активностью электролита, имеют один общий электрод и, таким образом, электрически соединены через проводник первого рода в единую цепь. Например, простые цепи с хлоридсеребряным и водородным электродами можно превратить в сдвоенную цепь с общим водородным электродом:
I II
Ag AgCl HCl H2 Pt H2 HCl AgCl Ag .
(aI) (aII)
В каждой из двух ячеек цепи протекает одна и та же реакция
Ag + H+ + Cl– = AgCl + 1/2 H2 ,
но в противоположных направлениях, причем если aI aII , то в первой ячейке реакция идет слева направо, а во второй справа налево:
Ag + H+I + Cl–I = AgCl + 1/2 H2 ;
AgCl + 1/2 H2 = Ag + H+II + Cl–II .
Суммарный процесс эквивалентен переносу 1 моль ионов водорода и 1 моль ионов хлора из первой ячейки во вторую
H+I + Cl–I = H+II + Cl–II ,
хотя фактический перенос в этой системе из-за отсутствия непосредственной границы раздела между растворами исключен и изменение содержания HCl обусловлено не переносом ионов, а химическими реакциями, протекающими в цепи. Сдвоенные химические цепи являются поэтому цепями без переноса или цепями без жидкостной границы. На основании уравнения реакции ЭДС системы будет равна
Е
= Ео
+
ln
= 2
ln
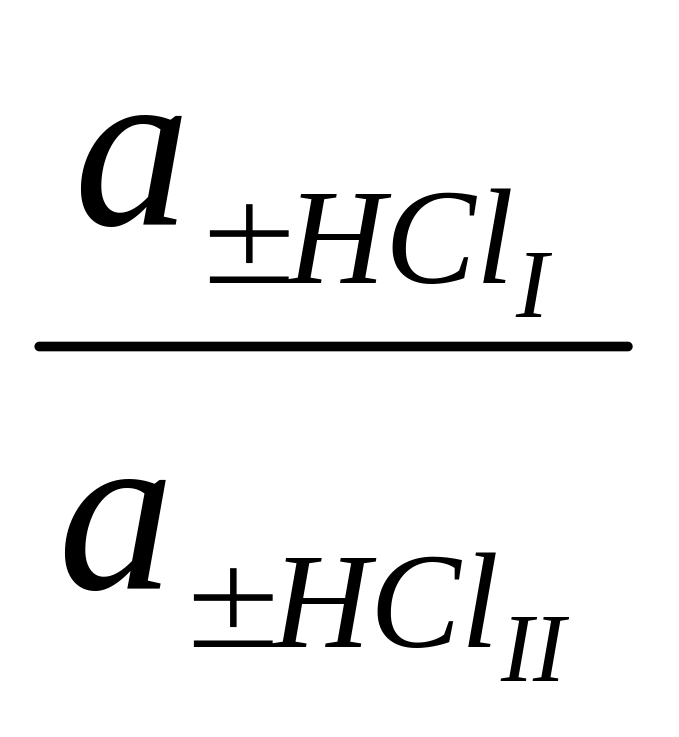 ,
,
причем стандартная ЭДС Ео равна 0, так как в обеих ячейках протекает одна и та же реакция, но в противоположных направлениях. При этом на одной стороне водородного электрода (общего для обеих ячеек) совершается катодный процесс Н+ + е = 1/2 Н2 , а на другой анодный 1/2 Н2 = Н+ + е. Подобные электроды называются биполярными и широко используются электрохимической промышленностью.
И по характеру процесса, и по форме уравнения для ЭДС двойная химическая цепь напоминает концентрационные цепи второго рода. Однако в сдвоенных химических цепях нет диффузионного потенциала и связанных с ним осложнений. Сопоставление ЭДС сдвоенной химической цепи и ЭДС концентрационной цепи с переносом с тем же электролитом позволяет определить его числа переноса. Сопоставление ЭДС двойной химической цепи с ЭДС соответствующей его простой цепи дает возможность с большой точностью находить стандартные потенциалы их электродов и коэффициенты активности электролитов.
