
- •Модуль2 Физика атомного ядра
- •Модуль 3 Физика частиц
- •11) Молекулярные спектры
- •12) Электрон в периодическом поле кристаллической решетки. Уравнение Шредингера, волновая функция, спектр энергий.
- •15) Капельная модель ядра предложена Бором и Вейцзейкером (1935г) относится к 1 группе. Ядро представляется в виде капли заряженной жидкости громадной плотности.
- •17) Радиоактивность –свойство атомных ядер самопроизвольно (спонтанно) изменять свой состав путем испускания элементарных частиц или ядерных фрагментов.
- •43) Нуклеосинтез
«ЯДЕРНАЯ ФИЗИКА»
Геологический факультет
Экзаменационные вопросы по дисциплине «Ядерная физика»
Модуль1. Элементы физики атома
1.Структура атома. Опыт Резерфорда и формула Резерфорда для рассеяния альфа- частиц.
2.Уровни энергии атома водорода. Полуклассическая теория атома водорода. Постулаты Бора. Формула Бора для энергии электрона в атоме водорода.
3.Сериальная формула Бальмера–Ридберга для частот поглощения и излучения атома водорода.
4.Элементы квантовой (волновой) механики. Принцип корпускулярно-волнового дуализма. Соотношения неопределенности Гейзенберга для координат и импульсов и энергии и времени. Волновая функция, вероятность наблюдения частицы, условие нормировки.
5. Уравнения Шредингера со временем и стационарное уравнение Шредингера.
6. Движение свободной частицы. Уравнение Шредингера. Волновая функция и энергия.
7.Прохождение частицы через потенциальный барьер. Формула для коэффициента прозрачности барьера.
8.Частица в центральносимметричном поле. Атом водорода, волновая функция, уровни энергии.
9.Квантовое состояние. Четыре квантовых числа. Принцип Паули. Электронные оболочки атомов химических элементов.
10. Молекула. Образование молекулы водорода. График потенциальной энергии в зависимости от расстояния между электронами.
11.Спектры молекул: электронные, колебательные, вращательные.
12.Кристаллы. Электрон в периодическом поле кристаллической решетки. Уравнение Шредингера, волновая функция, спектр энергий.
13.Металлы. Полупроводники. Диэлектрики. Их зонные диаграммы. Объяснение электропроводности.
Модуль2 Физика атомного ядра
14.Свойства атомных ядер. Состав и статические характеристики ядер.
15.Модели атомных ядер. Капельная модель. Модель ядерного ферми газа. Оболочечная модель.
16.Свойства ядерных сил и нуклон-нуклонное взаимодействие. Дейтрон и его характеристики.
17.Радиоактивность.альфа-распад, бета-распад.
18.Гамма-излучение возбужденных ядер и его характеристики. Эффект Мёссбауэра (ядерный гамма-резонанс)..
19.Ядерные реакции. Сечение и выход ядерной реакции. Реакции деления тяжелых ядер. Состав продуктов деления ядра и энергия деления..
20. Цепные ядерные реакции деления.Формула 4-х сомножителей.
21. Термоядерные реакции. Термоядерный взрыв.
22.Взаимодействие ядерного излучения с веществом.Прохождение заряженных частиц через вещество.
23.Прохождение гамма-квантов через вещество.
24. Прохождение нейтронов через вещество.
25.Источники частиц. Источники заряженных частиц. Ускорители. Источники γ-квантов. Источники нейтронов.
26.Методы регистрации частиц. Детекторы их типы и характеристики. Трековые детекторы. Ядерные фотоэмульсии. Пузырьковые камеры. Камера Вильсона.
27.Электронные детекторы. Счетчики
заряженных частиц и
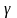 -квантов.
Гамма спектрометры и нейтронные
детекторы.
-квантов.
Гамма спектрометры и нейтронные
детекторы.
28.Ядерные реакторы. Классификация.Устройство. Работа. Управление. Аварии.
29. Дозиметрия. Флюенс.Экспозиционная доза.Поглощенная доза. Эквивалентная доза.
30.Действие ионизирующих излучений на структуру вещества. Радиационные дефекты. Химическое действие излучений.
31.Классификация
защит. Защита от внешних потоков
 -частиц
и
-частиц
и
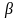 -частиц .Защита от
-излучения.
Защита от нейтронного излучения.
Радиационная защита от внутреннего
облучения.
-частиц .Защита от
-излучения.
Защита от нейтронного излучения.
Радиационная защита от внутреннего
облучения.
Модуль 3 Физика частиц
32.Частицы. Элементарные частицы и их классификация. Лептоны. Мезоны. Адроны.
33.Кварки и их характеристики. Кварковая модель адронов.
34.Эксперименты в области высоких энергий. Глубоконеупругое рассеяние электронов и нейтрино на протонах. Аннигиляция е-е+ в адроны, двух и трехструйные события.
35.Электромагнитное взаимодействие. Гамма-квант.
36.Сильное взаимодействие. Глюоны.
37.Слабое взаимодействие. Вионы (Векторные бозоны).
38. Объединение взаимодействий. Бегущие константы связи. График зависимости констант от энергии.
39.Гравитационное взаимодействие. Гравитон.
40.Большие машины физики. Большой адронный коллайдер в ЦЕРНЕ.
41.Современные астрофизические представления. Космология. Вселенная, её характеристики, образование и эволюция.
42. Галактики. Звезды, их классификация и эволюция. Белые карлики. Красные гиганты. нейтронные звезды. Черные дыры.
43. Ядерная астрофизика. Водородный и углеродный циклы. Ядерный нуклеосинтез.
44. Первичные и вторичные космические лучи.
1) Атомная физика- раздел физики, в котором изучают строение и свойства атомов и процессы с их участием.
Атом – наименьшая частица химического элемента, способная самостоятельно существовать и проявлять его свойства. Атом состоит из ядра и электронов. Электрический заряд ядра положительный равный отрицательному заряду электронов, следовательно, атом электрически нейтрален.
Строение атома было открыто Э.Резерфордом в 1911г. в опытах по рассеянию альфа-частиц на золотой пластинке. Очень малая часть альфа-частиц (дважды ионизированные атомы гелия) летящие с громадной скоростью рассеивались под большими углами, и даже назад, налетая на положительно заряженный массивный силовой центр внутри атома. Так возникла планетарная модель атома: в центре ядро вокруг него движутся электроны.
Формула Резерфорда для дифференциального сечения рассеяния
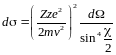
где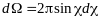 - элемент телесного угла «кулёк»).
- элемент телесного угла «кулёк»).
Дифференциальное
сечение рассеяния
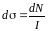 =
= число
частиц падающих на кольцо /плотность
потока частиц
число
частиц падающих на кольцо /плотность
потока частиц
2) Полуклассическая модель атома водорода предложенная Н.Бором основа на трех постулатах:
1.Постулат
стационарных состояний: электрон в
атоме находится в состояниях в которых
он не излучает. спектр энергий атома
дискретный.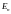 где
где
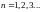 главное квантовое число.
главное квантовое число.
2.Условие частот:
электрон в атоме, переходя из одного
стационарного состояния
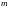 в другое состояние
в другое состояние
 ,
излучает (или поглощает) квант
электромагнитной энергии
,
излучает (или поглощает) квант
электромагнитной энергии
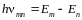
3.Правило квантования орбит: момент импульса электрона в стационарном состоянии при движении по орбите квантован
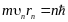
Кулоновская сила, действующая между электроном и ядром атома водорода (протоном) равна центростремительной силе
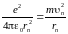
Радиус первой боровской орбиты электрона в атоме водорода
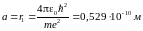
Уровни энергии электрона в атоме водорода
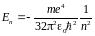
3)
Сериальная формула Бальмера-Ридберга для спектров излучения атома водорода
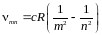 ;
где
;
где
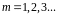
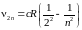 -серия Бальмера
(видимый свет).
-серия Бальмера
(видимый свет).
-нумерует серию, -нумерует линию в данной серии
4) Квантовая (волновая механика) - теория описывающая движение микрочастиц (молекул, атомов, ядер) и их систем.
Корпускулярно-волновой дуализм- всеобщее и универсальное свойство материи: любой волне соответствует частица и любой частице соответствует волна.
Энергия частицы
 ,где
,где
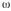 -
частота волны, импульс частицы
-
частота волны, импульс частицы
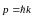 где
где
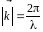 -волновой вектор, длина волны вероятности
де Бройля
-волновой вектор, длина волны вероятности
де Бройля
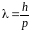 .
.
В квантовой механике нет понятия «траектория частицы» вследствие соотношения неопределенности Гейзенберга:
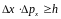 ,
,
 ,
,
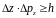 .
.
Т.е.
невозможно одновременно локализовать
микрочастицу и фиксировать её импульс
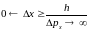
Комплексная
волновая функция
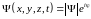 описывает состояние квантовой системы
в пространстве и времени.
описывает состояние квантовой системы
в пространстве и времени.
Вероятность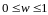 обнаружить частицу в объеме
обнаружить частицу в объеме
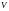 определяется по формуле
определяется по формуле
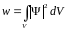
Условие
нормировки
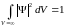 .
.
5) Уравнения Шредингера
Временно’е
уравнение Шредингера описывает эволюцию
квантовой системы
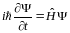
Где
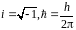
Стационарное
уравнение Шредингера описывает поведение
частицы находящейся в заданном силовом
поле
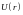
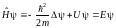
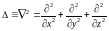 - оператор Лапласа
- оператор Лапласа
6)
Движение свободной
частицы вдоль оси х
с импульсом
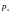
Уравнение
Шредингера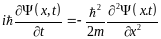 .
.
Его решение
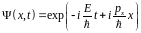 ,
энергия частицы
,
энергия частицы
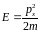 .
Спектр энергии непрерывен, (волновая
функция осциллирует), вероятность
нахождения частицы в любой точке оси
единица.
.
Спектр энергии непрерывен, (волновая
функция осциллирует), вероятность
нахождения частицы в любой точке оси
единица.
7)Движение
свободной частицы с энергией
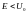 через одномерный потенциальный
прямоугольный барьер конечной ширины
через одномерный потенциальный
прямоугольный барьер конечной ширины
 и высоты
и высоты
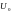 .
.
Уравнения Шредингера
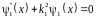 ,
,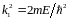
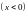 область 1 до барьера
область 1 до барьера
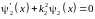 ,
,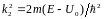
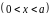 область 2 барьер
область 2 барьер
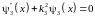 ,
,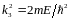
 область3 после барьера
область3 после барьера
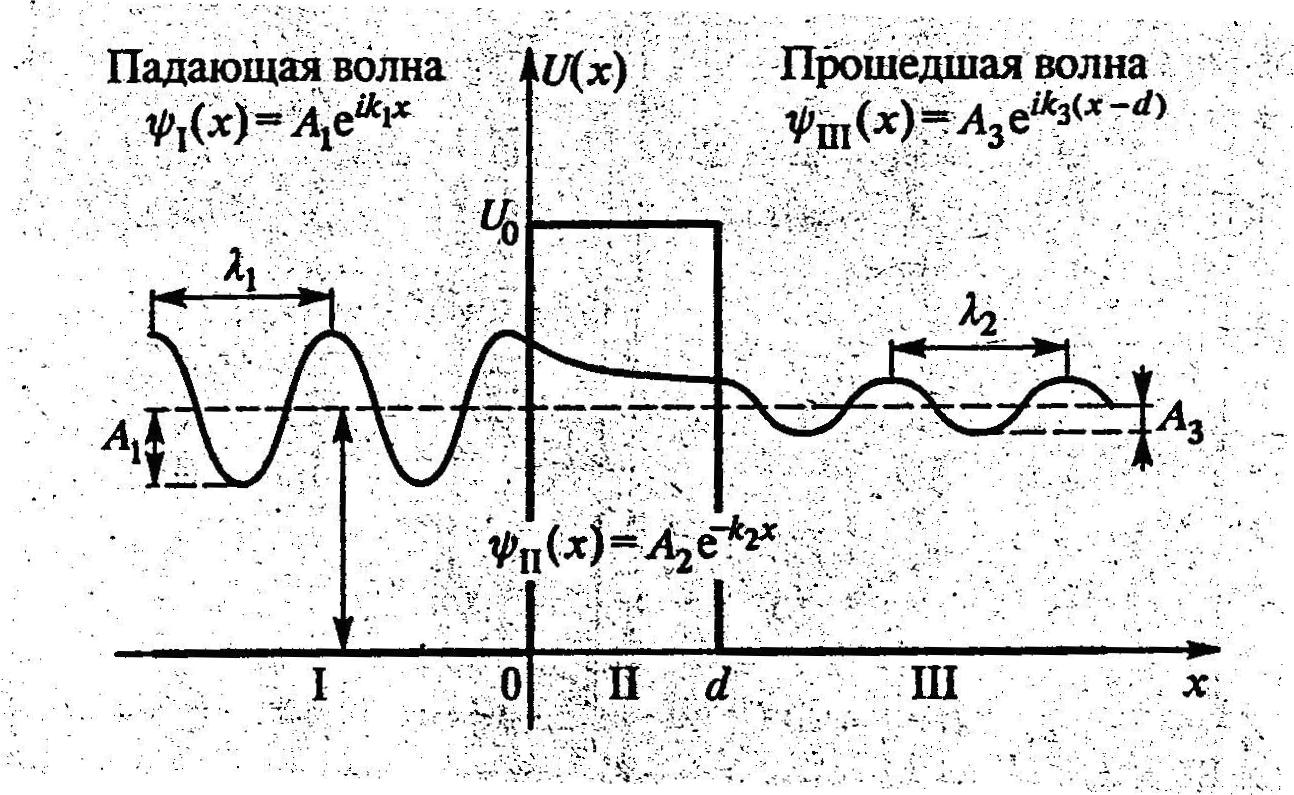
При падении на
барьер волновая функция осциллирует, частично отражается,
частично проходит внутрь барьера. Внутри
барьера волновая функция ослабляется
по экспоненте
осциллирует, частично отражается,
частично проходит внутрь барьера. Внутри
барьера волновая функция ослабляется
по экспоненте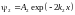 .
При выходе из барьера снова осциллирует
.
При выходе из барьера снова осциллирует
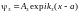 .
Таким образом, существует неравная нулю
вероятность прохождения потенциального
барьера. Она характеризуется коэффициентом
прозрачности прямоугольного барьера
.
Таким образом, существует неравная нулю
вероятность прохождения потенциального
барьера. Она характеризуется коэффициентом
прозрачности прямоугольного барьера
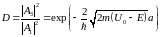
8) Уровни энергии соответствуют формуле бора
Волновая функция зависит от трех квантовых чисел
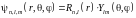
где
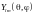 -сферические
гармоники
-сферические
гармоники
9) Принцип Паули: В каждом квантовом состоянии может находится только один электрон.
Состояние электрона в атоме полностью определяется четыремя квантовыми числами
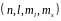
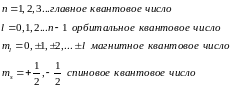
Квантовое состояние-это любое возможное состояние в котором может находится квантовая система.
Заполнение квантовых
состояний электронами происходит в
соответствие с принципом минимума
энергии и принципом Паули. При этом
электроны заполняют низшие энергетические
состояния группируясь в электронные
оболочки(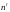 )
от ядра наружу. Число электронов в
оболочках
)
от ядра наружу. Число электронов в
оболочках
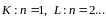
равно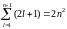 .
Оболочки состоят из подоболочек:
.
Оболочки состоят из подоболочек:
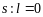 ;
;
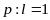 …
…
Так объясняется периодическая система химических элементов Д.И.Менделеева.
10)
Молекула –наименьшая частица вещества обладающая его свойствами и состоящая из атомов соединенных химическими связями.
Образование
молекулы водорода. В первом приближении
можно считать ядра атомов неподвижными
и рассматмимиривать только движение
двух электронов. Если спины электронов
антипараллельны то спин молекулы
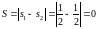 если параллельны то
если параллельны то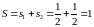 Энергия взаимодействия двух электронов
Энергия взаимодействия двух электронов
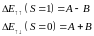
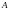 -электростатическая
энергия взаимодействия
-электростатическая
энергия взаимодействия
 -обменная
энергия (обмен электронами между
состояниями)
-обменная
энергия (обмен электронами между
состояниями)
Два атома водорода с антипараллельными спинами притягиваются образуют гомополярную молекулу водорода.
Два атома водорода с параллельными спинами отталкиваются. График потенциальной энергии взаимодействия атомов водорода в зависимости от расстояния между электронами приведен на рис .6
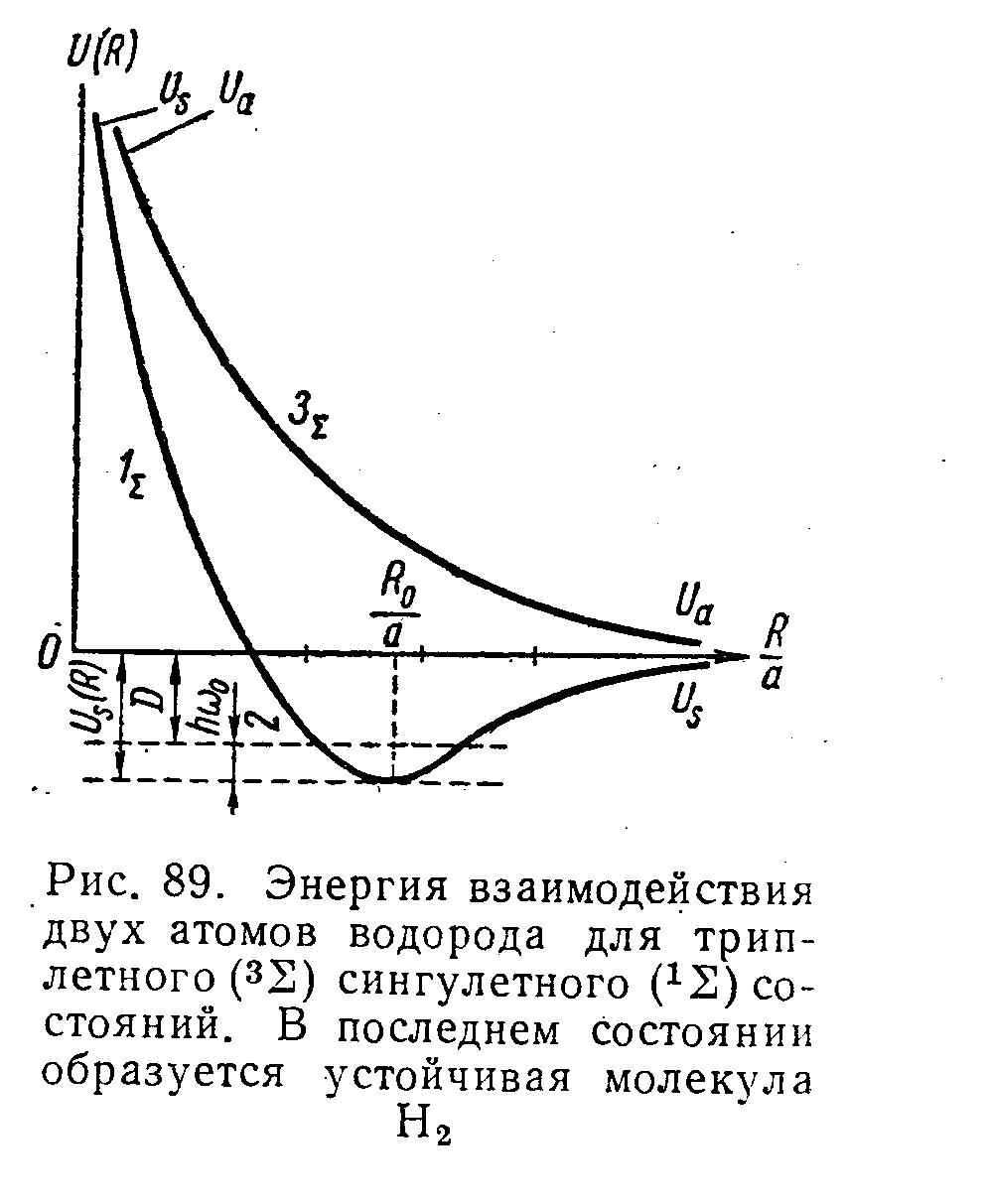
Рис6 Энергия взаимодействия двух атомов водорода для триплетного и синглетного состояний. В синглетном состоянии образуется устойчивая молекула водорода (нижняя кривая)
