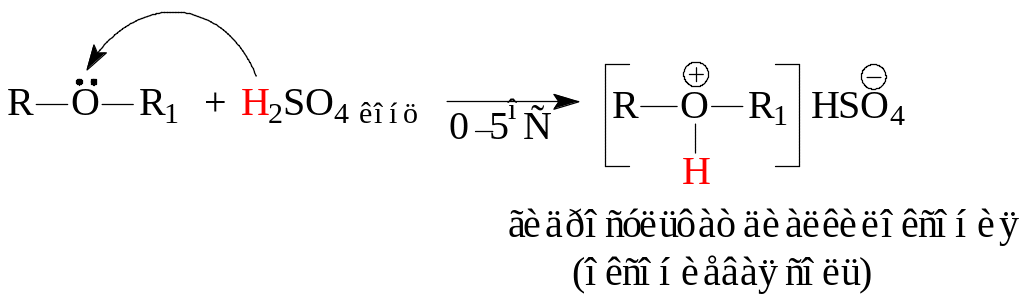- •Я. М. Каток, о. Я. Толкач органическая химия задачи и упражнения
- •Предисловие
- •1. Классификация и номенклатура органических соединений
- •Углеводороды и углеводородные радикалы (перечислены в порядке возрастания старшинства)
- •Примеры названий органических соединений
- •Примеры названий органических соединений
- •Индивидуальные задания Задача 1
- •Задача 2
- •2. Химическая связь
- •Индивидуальные задания Задача 3
- •Задача 4
- •3. Химическая реакция
- •Индивидуальные задания Задача 5
- •Задача 6
- •4. Алканы
- •Номенклатура
- •Примеры названий алканов по рациональной номенклатуре
- •Индивидуальные задания Задача 7
- •Задача 8
- •5. Непредельные углеводороды Номенклатура
- •Примеры названий непредельных соединений по рациональной номенклатуре
- •Примеры названий непредельных соединений
- •Индивидуальные задания Задача 9
- •Задача 10
- •Задача 11
- •Задача 12
- •Задача 13
- •Задача 14
- •Задача 15
- •Задача 16
- •6. Арены Номенклатура и изомерия замещенных бензола
- •Индивидуальные задания Задача 17
- •Задача 18
- •Задача 19
- •7. Галогенопроизводные углеводородов Номенклатура
- •Индивидуальные задания Задача 20
- •Задача 21
- •8. Спирты, фенолы, простые эфиры Классификация и номенклатура
- •Индивидуальные задания Задача 22
- •Задача 23
- •Задача 24
- •9. Альдегиды и кетоны Классификация и номенклатура
- •Индивидуальные задания Задача 25
- •Задача 26
- •10. Карбоновые кислоты и их производные Классификация и номенклатура
- •Примеры названий функциональных производных карбоновых кислот
- •Индивидуальные задания Задача 27
- •Задача 28
- •Задача 29
- •Задача 30
- •11. Углеводы
- •Номенклатура
- •Индивидуальные задания Задача 31
- •Задача 32
- •12. Нитросоединения Классификация и номенклатура
- •Индивидуальные задания Задача 33
- •13. Амины, аминокислоты и пептиды Классификация и номенклатура
- •Индивидуальные задания Задача 34
- •Задача 35
- •Задача 36
- •Задача 37
- •Задача 38
- •Литература
- •Оглавление
- •Органическая химия Задачи и упражнения
- •220006. Минск, Свердлова, 13а.
- •Пример решения задачи 1
- •Решение
- •Пример решения задачи 2
- •Решение
- •Пример решения задачи 3
- •Пример решения задачи 4
- •Решение
- •Пример решения задачи 5
- •Пример решения задачи 6
- •Пример решения задачи 7
- •Способы получения алканов
- •Решение
- •Пример решения задачи 8
- •Основные химические свойства алканов
- •Пример решения задачи 9
- •Способы получения алкенов
- •Решение
- •Пример решения задачи 10
- •Химические свойства алкенов
- •Решение
- •Пример решения задачи 11
- •Пример решения задачи 12
- •Химические свойства алкадиенов
- •Решение
- •Пример решения задачи 18
- •Способы получения аренов
- •Решение
- •Пример решения задачи 19
- •Пример решения задачи 20
- •Химические свойства галогенопроизводных углеводородов
- •Кислотно-основные свойства спиртов и фенолов
- •Реакции, иллюстрирующие кислотные свойства спиртов и фенолов
- •Решение
- •Пример решения задачи 23
- •Основные химические свойства спиртов, фенолов и простых эфиров
- •Решение
- •Пример решения задачи 24
- •Способы получения спиртов
- •Способы получения фенолов
- •Химические свойства карбонильных соединений
- •Решение
- •Пример решения задачи 26
- •Пример решения задачи 27
- •Решение
- •Пример решения задачи 28
- •Способы получения карбоновых кислот
- •Решение
- •Пример решения задачи 29
- •Пример решения задачи 30
- •Пример решения задачи 31
- •Моносахариды (монозы), классификация
- •Химические свойства моносахаридов
- •Решение
- •Пример решения задачи 32
- •Химические свойства дисахаридов
- •Решение
- •Пример решения задачи 34
- •Решение
- •Пример решения задачи 35 Основные химические свойства аминов
- •Химические свойства аминокислот
- •Качественные реакции на аминокислоты
- •Решение
- •Пример решения задачи 36 Решение
- •Пример решения задачи 37
- •Пример решения задачи 38
- •Решение
Кислотно-основные свойства спиртов и фенолов
Согласно протолитической теории БренстедаЛоури, кислотами являются вещества, способные отдавать протон (Н+), доноры протона. Основания это вещества, способные присоединять протон, акцепторы протона. Кислотно-основное взаимодействие двух молекул заключается в переносе протона от кислоты к основанию с образованием сопряженного основания и сопряженной кислоты. Чем сильнее кислота или основание, тем слабее сопряженные им основание и кислота. И наоборот. В рамках теории БренстедаЛоури любую кислотно-основную реакцию можно описать следующим уравнением:

Гидроксилпроизводные углеводородов (спирты и фенолы) содержат группу ОН, которая может являться как донором, так и акцептором протона.
Кислотные свойства гидроксилпроизводного, т. е. легкость разрыва связи ОН, будут определяться полярностью и энергией диссоциации этой связи. Чем выше полярность связи ОН и чем ниже ее энергия диссоциации, тем легче идет разрыв связи, тем выше кислотность.
Электроноакцепторные заместители (ЭА), связанные с ОН-группой, повышают полярность связи ОН, снижают энергию ее диссоциации и в целом повышают кислотность соединения. Электронодонорные заместители (ЭД), наоборот, снижают полярность, увеличивают энергию диссоциации связи ОН и снижают кислотные свойства соединения.
Основные свойства гидроксилсодержащих соединений обусловлены наличием неподеленной электронной пары на атоме кислорода. Чем выше электронная плотность на атоме кислорода, тем легче присоединяется протон, тем выше основность соединения. Поэтому электронодонорные заместители, увеличивающие электронную плотность на кислороде, повышают основные свойства соединения, а электроноакцепторные понижают.
Исходя из вышесказанного, представим ряд кислотно-основных свойств гидроксилпроизводных:
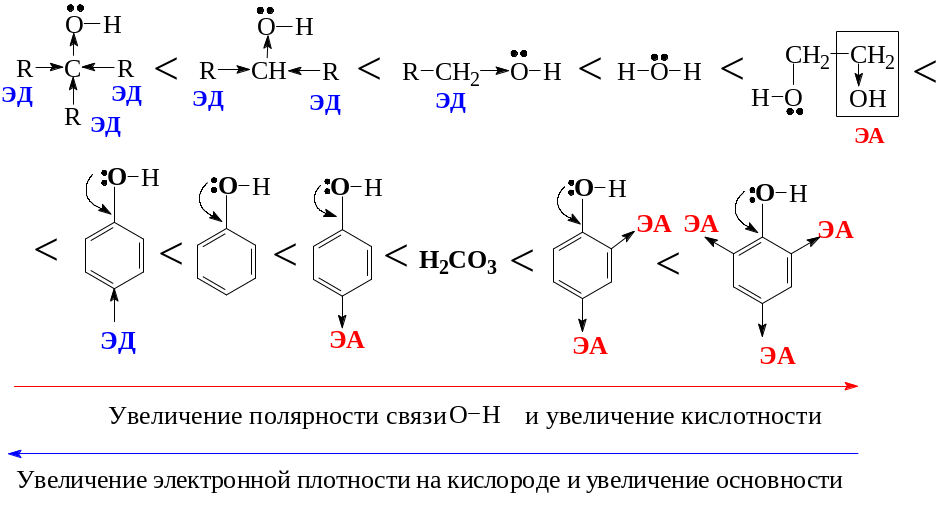
Реакции, иллюстрирующие кислотные свойства спиртов и фенолов
Спирты являются более слабыми кислотами, чем вода, и обнаружить их кислотность в водных растворах невозможно, рН водного раствора спиртов равно 7. Подтвердить кислотность спиртов можно только в реакциях с активными металлами или очень сильными основаниями в отсутствие воды:

Реакции с активными металлами и их амидами являются качественными на ОН-группу, так как сопровождаются бурным выделением газов.
У многоатомных спиртов кислотность по сравнению с одноатомными возрастает, особенно в случае вицинальных диолов и полиолов. В отличие от одноатомных спиртов, они могут проявлять кислотные свойства не только в реакциях с активными металлами и сильными основаниями, но и в реакциях с гидроксидами тяжелых металлов. В частности, с медь(II)-гидроксидом в щелочной среде вицинальные многоатомные спирты образуют растворимую в воде комплексную соль, окрашенную в темно-синий цвет. Это качественная реакция на вицинальную диольную группу:
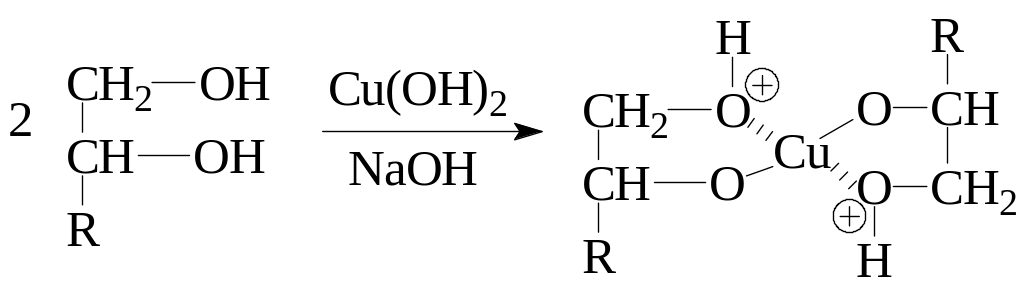
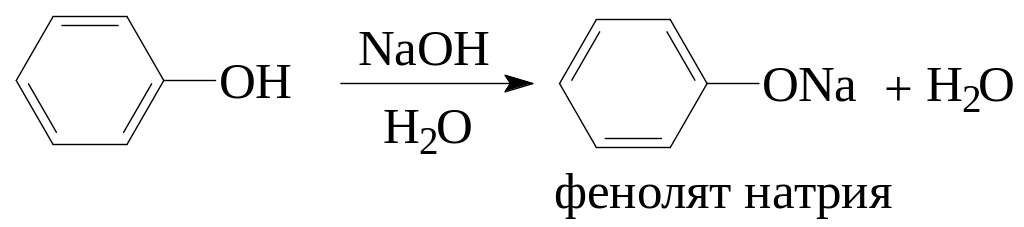
Фенолы. Благодаря наличию в молекулах фенолов +М-эффекта, электронная плотность на атоме кислорода понижается, полярность связи ОН увеличивается и снижается энергия ее диссоциации. Поэтому фенолы, в отличие от спиртов, являются достаточно сильными кислотами и способны образовывать соли даже с водными растворами щелочей:
 .
.
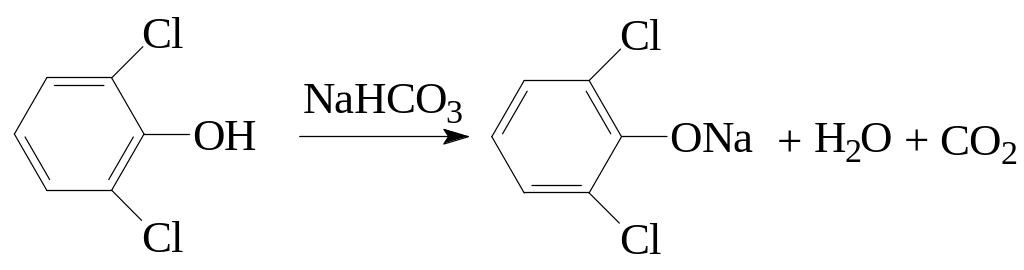
При наличии в бензольном кольце двух и более электроноакцепторных заместителей кислотность фенольного гидроксила увеличивается настолько, что становятся возможными реакции с солями угольной кислоты:
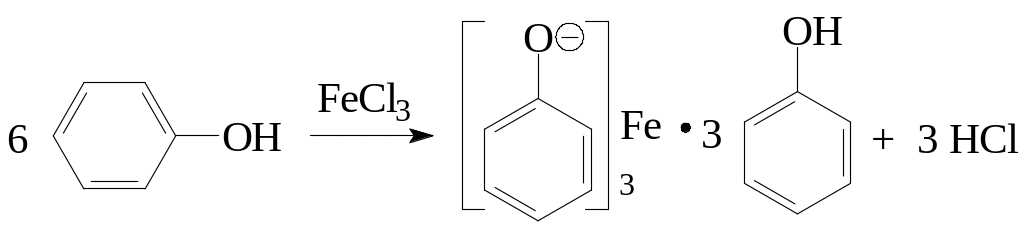
Кислотные свойства фенолов проявляются также в реакции с железо(III)-хлоридом. При взаимодействии с ионами Fe3+ образуется комплексная соль фенола, окрашенная в интесивный фиолетовый цвет. Поэтому реакция фенолов с FeCl3 является качественной и используется для обнаружения фенольного гидроксила.
Основность это способность присоединять протон или кислоты Льюиса. В ряду гидроксилпроизводных наиболее выраженными основными свойствами обладают третичные спирты. Однако вследствие высокой электроотрицательности атома кислорода и, соответственно, низкой поляризуемости его электронов спирты могут реагировать при охлаждении только с сильными минеральными кислотами с образованием оксониевых солей. Основными свойствами обладают и диалкиловые эфиры, которые тоже образуют оксониевые соли с концентрированными кислотами. Растворение в холодных концентрированных кислотах с образованием однофазной системы (оксониевых солей) является качественной реакцией на спирты и диалкиловые эфиры. У фенолов вследствие сопряжения неподеленной электронной пары кислорода с бензольным кольцом (+М-эффект) основные свойства выражены очень слабо. Поэтому фенолы оксониевых солей не образуют и не присоединяют кислоты Льюиса.