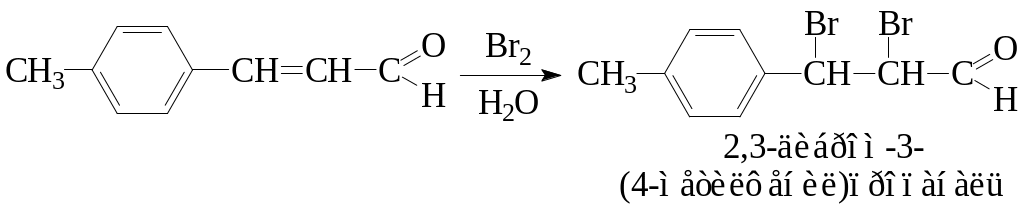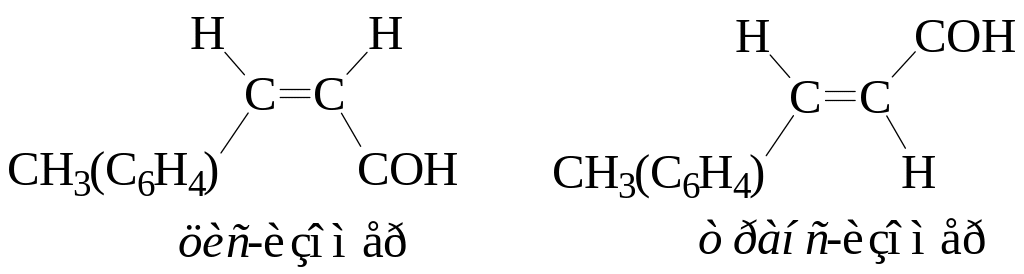- •Я. М. Каток, о. Я. Толкач органическая химия задачи и упражнения
- •Предисловие
- •1. Классификация и номенклатура органических соединений
- •Углеводороды и углеводородные радикалы (перечислены в порядке возрастания старшинства)
- •Примеры названий органических соединений
- •Примеры названий органических соединений
- •Индивидуальные задания Задача 1
- •Задача 2
- •2. Химическая связь
- •Индивидуальные задания Задача 3
- •Задача 4
- •3. Химическая реакция
- •Индивидуальные задания Задача 5
- •Задача 6
- •4. Алканы
- •Номенклатура
- •Примеры названий алканов по рациональной номенклатуре
- •Индивидуальные задания Задача 7
- •Задача 8
- •5. Непредельные углеводороды Номенклатура
- •Примеры названий непредельных соединений по рациональной номенклатуре
- •Примеры названий непредельных соединений
- •Индивидуальные задания Задача 9
- •Задача 10
- •Задача 11
- •Задача 12
- •Задача 13
- •Задача 14
- •Задача 15
- •Задача 16
- •6. Арены Номенклатура и изомерия замещенных бензола
- •Индивидуальные задания Задача 17
- •Задача 18
- •Задача 19
- •7. Галогенопроизводные углеводородов Номенклатура
- •Индивидуальные задания Задача 20
- •Задача 21
- •8. Спирты, фенолы, простые эфиры Классификация и номенклатура
- •Индивидуальные задания Задача 22
- •Задача 23
- •Задача 24
- •9. Альдегиды и кетоны Классификация и номенклатура
- •Индивидуальные задания Задача 25
- •Задача 26
- •10. Карбоновые кислоты и их производные Классификация и номенклатура
- •Примеры названий функциональных производных карбоновых кислот
- •Индивидуальные задания Задача 27
- •Задача 28
- •Задача 29
- •Задача 30
- •11. Углеводы
- •Номенклатура
- •Индивидуальные задания Задача 31
- •Задача 32
- •12. Нитросоединения Классификация и номенклатура
- •Индивидуальные задания Задача 33
- •13. Амины, аминокислоты и пептиды Классификация и номенклатура
- •Индивидуальные задания Задача 34
- •Задача 35
- •Задача 36
- •Задача 37
- •Задача 38
- •Литература
- •Оглавление
- •Органическая химия Задачи и упражнения
- •220006. Минск, Свердлова, 13а.
- •Пример решения задачи 1
- •Решение
- •Пример решения задачи 2
- •Решение
- •Пример решения задачи 3
- •Пример решения задачи 4
- •Решение
- •Пример решения задачи 5
- •Пример решения задачи 6
- •Пример решения задачи 7
- •Способы получения алканов
- •Решение
- •Пример решения задачи 8
- •Основные химические свойства алканов
- •Пример решения задачи 9
- •Способы получения алкенов
- •Решение
- •Пример решения задачи 10
- •Химические свойства алкенов
- •Решение
- •Пример решения задачи 11
- •Пример решения задачи 12
- •Химические свойства алкадиенов
- •Решение
- •Пример решения задачи 18
- •Способы получения аренов
- •Решение
- •Пример решения задачи 19
- •Пример решения задачи 20
- •Химические свойства галогенопроизводных углеводородов
- •Кислотно-основные свойства спиртов и фенолов
- •Реакции, иллюстрирующие кислотные свойства спиртов и фенолов
- •Решение
- •Пример решения задачи 23
- •Основные химические свойства спиртов, фенолов и простых эфиров
- •Решение
- •Пример решения задачи 24
- •Способы получения спиртов
- •Способы получения фенолов
- •Химические свойства карбонильных соединений
- •Решение
- •Пример решения задачи 26
- •Пример решения задачи 27
- •Решение
- •Пример решения задачи 28
- •Способы получения карбоновых кислот
- •Решение
- •Пример решения задачи 29
- •Пример решения задачи 30
- •Пример решения задачи 31
- •Моносахариды (монозы), классификация
- •Химические свойства моносахаридов
- •Решение
- •Пример решения задачи 32
- •Химические свойства дисахаридов
- •Решение
- •Пример решения задачи 34
- •Решение
- •Пример решения задачи 35 Основные химические свойства аминов
- •Химические свойства аминокислот
- •Качественные реакции на аминокислоты
- •Решение
- •Пример решения задачи 36 Решение
- •Пример решения задачи 37
- •Пример решения задачи 38
- •Решение
Задача 30
Установите строение соединения с молекулярной формулой А, которое соответствует приведенному в табл. 48 описанию. Обоснуйте выбор структурной формулы, сделав вывод по каждому из пунктов описания свойств. Назовите установленное вещество, напишите все упомянутые в условии уравнения реакций.
Таблица 48
Вариант |
Молекулярная формула соединения А |
Описание свойств соединения А |
1 |
С4Н4О4 |
а) выделяет СО2 при взаимодействии с NaHCO3; б) обесцвечивает бромную воду и реактив Вагнера; в) может существовать в виде цис-транс-изомеров, один из которых легко, а другой трудно растворим в воде; г) при нагревании до 200 С образуется соединение состава С4Н2О3, которое не обладает кислотными свойствами и реагирует с водой |
2 |
С8Н10О |
а) дает цветную реакцию с FеCl3; б) алкилируется метилбромидом в щелочной среде; в) при окислении продукта алкилирования образуется 4-метоксибензойная кислота |
3 |
С8Н8О3 |
а) реагирует с NaHCO3 с выделением газа; б) образует сложные эфиры как с карбоновыми кислотами, так и со спиртами; в) не дает цветную реакцию с FеCl3; г) при жестком окислении превращается в 1,2-бензолдикарбоновую кислоту |
4 |
С4Н6О4 |
а) проявляет кислотные свойства; б) с этанолом (в присутствии Н2SO4) образует производное состава С8Н14О4; в) при нагревании выделяет СО2 с образованием нового соединения С3Н6О2, которое также обладает кислотными свойствами |
5 |
С5Н10О2 |
а) имеет рН 4; б) реагирует с NaHCO3 с выделением газа; в) с фосфор-пентахлоридом образует вещество состава С5Н9OCl; г) при cплавлении со щелочью его натриевой соли образуется 2-метилпропан |
6 |
C8H6O3 |
а) реагирует с карбонатами с выделением газа; б) дает реакцию «серебряного зеркала»; в) с этанолом в кислой среде образует соединение состава С14Н20О4; г) при окислении хромовой смесью образует 1,4-бензолдикарбоновую кислоту |
Продолжение табл. 48
Вариант |
Молекулярная формула соединения А |
Описание свойств соединения А |
7 |
С8Н8О2 |
а) образует оксим и гидразон; б) дает положительную иодоформную реакцию; в) дает цветную реакцию с FеCl3; г) функциональные группы в искомом соединении имеют согласованную ориентацию в SE-реакциях; д) не способно к образованию внутримолекулярной водородной связи |
8 |
С3Н4О3 |
а) не дает реакцию «серебряного зеркала»; б) дает положительную иодоформную реакцию; в) образует оксим, гидразон, хлорангидрид; г) в реакции с натрий-гидрокарбонатом выделяет газ |
9 |
C8H8O3 |
а) выделяет СО2 при взаимодействии с карбонатами; б) с этанолом образует вещество состава С9Н10О3; в) при нагревании с концентрированной НI образует салициловую кислоту |
10 |
С6Н12О3 |
а) образует соль с СаСО3; б) при взаимодействии с РСl5 образует вещество состава C6H10Cl2; в) при нагревании с серной кислотой образует соединение, обладающее кислотными свойствами, состава С6Н10О2; г) соединение С6Н10О2 дает бурый осадок с реактивом Вагнера, а при окислении хромовой смесью образует метилэтилкетон и щавелевую кислоту |
11 |
С4Н6О6 |
а) реагирует с NaHCO3 с выделением газа; б) вступает в реакцию этерификации с метанолом с образованием соединения состава С6Н10О6; в) в сильно щелочной среде образует комплекс темно-синего цвета с Сu(OH)2 |
12 |
C8H6O4 |
а) не растворяется в воде, но растворяется в растворах NaOH и NaHCO3; б) при интенсивном нагревании образует соединение состава C8H4O3, которое не проявляет кислотные свойства; в) вещество C8H4O3 легче, чем искомое, вступает в реакции ацилирования с этанолом и метиламином |
Продолжение табл. 48
Вариант |
Молекулярная формула соединения А |
Описание свойств соединения А |
13 |
С9Н12О |
а) реагирует с металлическим натрием с выделением газа; б) при нагревании с водоотнимающим средством образует соединение состава С9Н10, которое обесцвечивает бромную воду, а при окислении KMnO4 + H2SO4 образует 1,4-бензолдикарбоновую кислоту; в) при дегидрировании (Cu, 630 C) образует кетон |
14 |
С3Н8О2 |
а) выделяет водород при взаимодействии с металлическим натрием; б) при взаимодействии с избытком РСl5 образует соединение состава C3H7СlO; в) при нагревании с концентрированной НI образует иодметан и вещество состава С2H6O2, которое растворяет Сu(OH)2 с образованием комплекса темно-синего цвета |
15 |
C8H8O3 |
а) способно к образованию внутримолекулярной водородной связи; б) дает фиолетовое окрашивание при добавлении раствора FeCl3; в) обесцвечивает бромную воду с образованием светлого осадка; г) при кислотном гидролизе образует метанол и вещество состава C7H6O3, которое при добавлении раствора NaHCO3 выделяет углекислый газ |
16 |
С6Н12О2 |
а) образует кристаллический осадок с натрий-гидросульфитом; б) реагирует с металлическим натрием без нагревания; в) при нагревании с Cu(ОН)2 образует красный осадок Cu2О; г) может быть получено реакцией альдольной конденсации пропаналя |
17 |
С6Н14О2 |
а) молекула имеет симметричное строение; б) выделяет водород при взаимодействии с металлическим натрием; в) не образует комплекс темно-синего цвета с Сu(OH)2; г) при дегидратации образует алкадиен состава С6Н10, который при окислении KMnO4 в кислой среде образует 2 моль СО2 и 1 моль бутандиона |
Продолжение табл. 48
Вариант |
Молекулярная формула соединения А |
Описание свойств соединения А |
18 |
С4Н8О2 |
а) реагирует с металлическим натрием при комнатной температуре с выделением газа; б) при взаимодействии с PCl5 образует соединение состава С4Н7Cl3; в) дает положительную реакцию «серебряного зеркала»; г) окисление хромовой смесью приводит к образованию янтарной кислоты |
19 |
С9Н8О2 |
а) сгорает с выделением сажи; б) с реактивом Вагнера образует бурый осадок MnO2; в) существует в виде цис-транс-изомеров; г) реагирует с натрий-гидрокарбонатом с выделением газа |
20 |
С5Н8О3 |
а) выделяет СО2 при взаимодействии с NaНСО3; б) с метанолом в кислой среде образует соединение состава С6Н10О3; в) присоединяет молекулу HCN в щелочной среде; г) образует желтый осадок иодоформа при взаимо- действии с I2 + NaOH; д) имеет неразветвленный углеродный скелет |
21 |
С5Н8О2 |
а) не проявляет кислотные свойства; б) обесцвечивает бромную воду; в) при гидролизе в водном растворе щелочи образует два органических продукта, один из которых метанол; г) легко вступает в реакцию полимеризации с образованием полимера, который используется для изготовления органического стекла |
22 |
С7Н8О2 |
а) хорошо растворяется в NaOH; б) ацилируется уксусным ангидридом в щелочной среде; в) обесцвечивает бромную воду с образованием соединения состава С7Н5Br3О2; г) при нагревании с концентрированной HI образуется иодметан и вещество, которое с раствором FeCl3 дает цветную реакцию |
Продолжение табл. 48
Вариант |
Молекулярная формула соединения А |
Описание свойств соединения А |
23 |
C9H8O |
а) обесцвечивает бромную воду; б) с NaHSO3 образует кристаллический осадок; в) дает реакцию «серебряного зеркала»; г) при окислении KMnO4 в кислой среде образует бензолдикарбоновую кислоту с согласованной ориентацией в SE-реакциях |
24 |
С10Н12О2 |
а) не проявляет кислотные свойства; б) при гидролизе в кислой среде образует два органических соединения, одно из которых при взаимодействии с NaHCO3 выделяет углекислый газ; в) искомое вещество может быть получено ацилированием фенолята натрия хлорангидридом кислоты с разветвленным углеродным скелетом |
25 |
С6Н14О |
а) растворяется в холодной концентрированной H2SO4 с образованием оксониевой соли; б) не взаимодействует с металлическим натрием при комнатной температуре, но при нагревании претерпевает расщепление с образованием двух органических продуктов; в) может быть получено по реакции Вильямсона из трет-бутилата натрия и алкилиодида |
26 |
С6Н12О3 (2 изомера) |
а) образуют соли с СаСО3; б) в реакции с РCl5 образуют соединения состава С6Н10Cl2О; в) в результате внутримолекулярной дегидратации обоих изомеров получается одно и то же соединение состава С6Н10О2, которое образует бурый осадок при взаимодействии с реактивом Вагнера; г) вещество С6Н10О2 при жестком окислении хромовой смесью образует ацетон и малоновую кислоту |
27 |
С9Н8О3 |
а) выделяет СО2 при взаимодействии с карбонатами; б) при гидролизе образует уксусную кислоту и соединение состава С7Н6О3, которое дает фиолетовое окрашивание с FeCl3 и образует осадок с бромной водой; в) искомое вещество широко используется в медицине |
Окончание табл. 48
Вариант |
Молекулярная формула соединения А |
Описание свойств соединения А |
28 |
С3Н6О3 |
а) с C6H5NHNH2 образует фенилгидразон; б) в щелочной среде присоединяет HCN; в) дает реакцию «серебряного зеркала»; г) растворяет Cu(OH)2 с образованием раствора темно-синего цвета |
29 |
С8Н6О4 |
а) не растворяется в воде, но растворяется в растворах NaOH и NaHCO3; б) с этанолом образует соединение состава С12Н14О4; в) вступает в реакцию поликонденсации с этандиолом с образованием полимера, который используется в производстве синтетического волокна лавсан |
30 |
С5H10О |
а) с гидроксиламином образует оксим; б) не восстанавливает Сu(OH)2; в) присоединяет водород с образованием спирта, который при нагревании с водоотнимающим средством дает углеводород С5Н10; г) вещество С5Н10 при жестком окислении образует смесь этановой и пропановой кислот |
Пример решения и оформления задачи на установление строения неизвестного вещества.
Установить строение соединения состава С10Н10О, которое: а) обесцвечивает бромную воду и реактив Вагнера; б) может cуществовать в виде цис-транс-изомеров; в) образует осадок с NaHSO3; г) при нагревании восстанавливает Cu(OH)2 до Cu2O; д) при окислении хромовой смесью образует терефталевую кислоту.
Экспериментальные данные |
Выводы о строении |
С10Н10О т. е. СnH2n10O |
сильно ненасыщенное кислородсодержащее соединение (возможно содержит бензольное кольцо) |
обесцвечивает бромную воду и реактив Вагнера |
содержит алифатические кратные связи |
Экспериментальные данные |
Выводы о строении |
может существовать в виде цис-транс-изомеров |
содержит не концевую двойную связь |
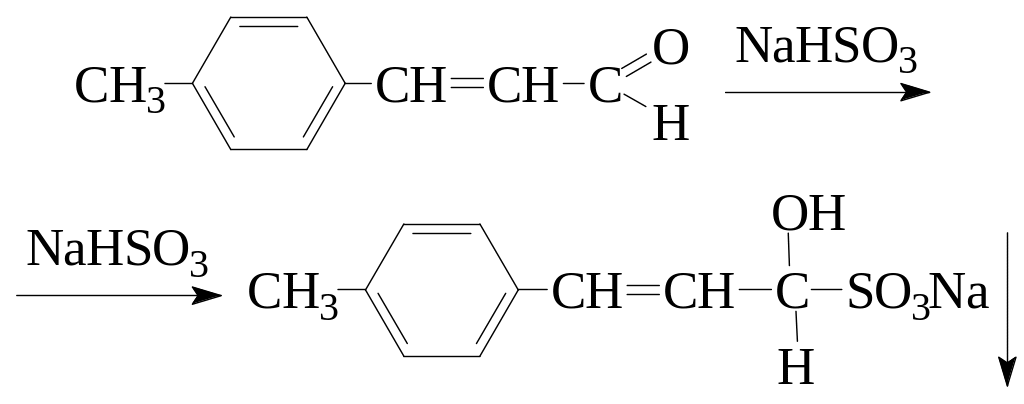
образует осадок с NaHSO3 |
является альдегидом или метилкетоном |
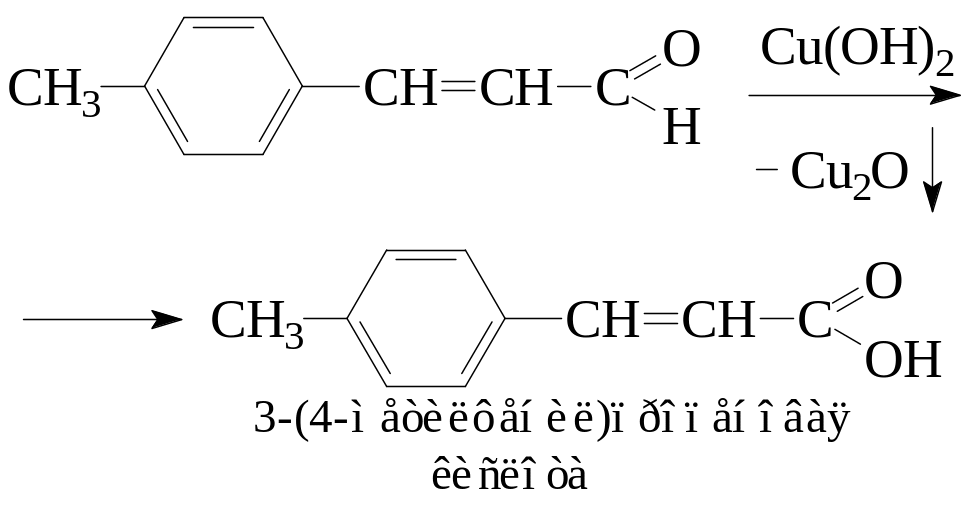
при нагревании восстанавливает Cu(OH)2 до Cu2O |
содержит альдегидную группу, не связанную с бензольным кольцом |
при окислении хромовой смесью образует терефталевую кислоту |
содержит две боковые цепи, находящиеся по отношению друг к другу в пара-положении |
На основании выводов о строении устанавливаем, что искомое соединение имеет следующую структурную формулу:
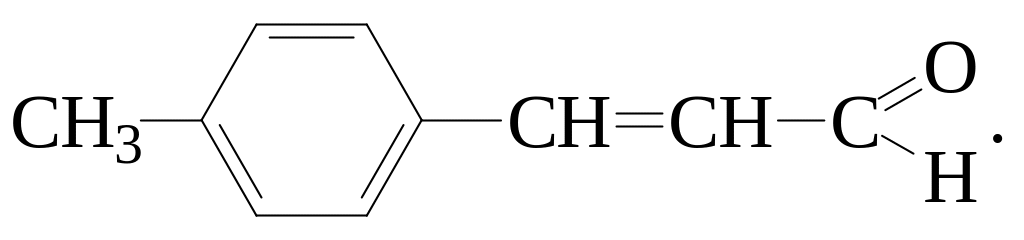
3-(4-метилфенил)пропеналь
(пара-метилкоричный альдегид)
Уравнения реакций, подтверждающие строение искомого соединения: