
- •Техника безопасности при работе в химической лаборатории
- •Физические константы органических веществ
- •Лабораторная работа Определение температуры кипения и показателя преломления неизвестного вещества
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1) Определение температуры плавления с применением прибора Сиволобова.
- •Лабораторная работа Определение температуры плавления неизвестного вещества с применением прибора Сиволобова
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1.1. Исследование физических свойств вещества
- •1.2. Проба на свечение пламени
- •1.3. Проба Бельштейна на галоген
- •1.4. Открытие кратной связи
- •1.5. Открытие бензольного кольца
- •1.6. Открытие боковой цепи в бензольном кольце
- •1.7. Открытие галогена в алифатической цепи
- •Аналитическая задача
- •Качественный анализ неизвестного вещества
- •Задача 1
- •1. Исследование физических свойств вещества
- •2. Качественные реакции
- •2.1.Открытие карбоксильной группы
- •2.2. Открытие фенолов.
- •2.3. Открытие карбонильной группы (открытие альдегидов и кетонов).
- •2.4. Открытие спиртов.
- •2.5. Открытие сложного эфира.
- •Идентификация индивидуальных веществ
- •1. Идентификация кислот
- •3. Идентификация альдегидов и кетонов.
- •4. Идентификация спиртов.
- •Аналитическая задача
- •Идентификация неизвестного вещества (образец)
- •Дата Подпись преподавателя Задача 2
- •1.1. Предварительные испытания
- •1.2. Качественные реакции
- •1.2.1. Открытие углеводов реакцией Молиша
- •1.2.2. Открытие моносахаридов реакцией с калий-гидроксидом
- •1.2.3. Открытие альдоз и кетоз реакцией Троммера
- •1.2.4. Открытие кетоз реакцией Селиванова
- •1.3. Идентификация моно- и дисахаридов
- •1.3.1. Фруктоза
- •1.3.2. Ксилоза
- •1.3.3. Глюкоза
- •1.3.4. Мальтоза (солодовый сахар)
- •1.3.5. Сахароза (свекловичный, тростниковый сахар)
- •1.4. Идентификация полисахаридов
- •1.4.1. Амилоза и амилопектин
- •1.4.2. Открытие целлюлозы
- •1.5. Идентификация производных сахаров
- •1.5.1. Сорбит
- •1.5.2. Глюкаровая кислота
- •Аналитическая задача по теме «Углеводы»
- •Дата Подпись преподавателя Задача 3
1. Исследование физических свойств вещества
1.1 Внешний вид вещества. Как видно из табл. 2.6, кроме фенола, все исследуемые эталонные вещества являются бесцветными жидкостями с характерным запахом (отметить в журнале). Фенол низкоплавкое кристаллическое вещество. Для неизвестного вещества в таблице 2.2 описывают его агрегатное состояние, цвет.
1.2 Определение растворимости. Растворимость неизвестного вещества определяют:
а) в воде (1);
б) в петролейном эфире (10);
в) в 5%-ном растворе едкого натра (6);
г) в 5%-ном растворе гидрокарбоната натрия (5).
Карбоновая кислота, спирты и ацетон (см. таблицу 2.7) хорошо растворимы в воде, фенол малорастворим, этилацетат практически нерастворим. В петролейном эфире растворимы все эталонные вещества, кроме этиленгликоля. Растворимость в воде и петролейном эфире изучают на примере этиленгликоля и этилацетата; в водном растворе NaOH фенол, в водном растворе NaHCO3 уксусную кислоту.
Затем исследуют растворимость неизвестного вещества, причем для растворимого в воде вещества не имеет смысла определять растворимость в других водных растворах (почему?).
В пробирку помещают несколько капель или кристалликов вещества, приливают при встряхивании 0,5 мл растворителя. Если вещество не растворяется при комнатной температуре, то добавляют еще растворителя и нагревают на водяной бане или в пламени горелки.
На основании растворимости с помощью таблицы 2.5 делают вывод о классах, к которым можно отнести неизвестное соединение.
1.3 Определение относительной плотности по сравнению с водой (>1 или <1) проводят для жидких, нерастворимых в воде неизвестных веществ.
2. Качественные реакции
2.1.Открытие карбоксильной группы
2.1.1. Реакция на кислотность среды. В пробирку помещают 23 капли уксусной кислоты (16) и 3 капли воды (1). Полученный раствор наносят с помощью стеклянной палочки на универсальную индикаторную бумажку (47) отмечают рН раствора. Записывают уравнение диссоциации кислоты в водном растворе.
Аналогично изучают растворимость неизвестного вещества. Для определения рН малорастворимых в воде веществ их раствор готовят, добавляя к смеси вещества (0,01 г) с водой по каплям этиловый спирт (20) и энергично встряхивая пробирку. Сравнивают полученное рН раствора с рН уксусной кислоты. Двухосновные и замещенные кислоты сильнее одноосновных кислот.
2.1.2. Реакция с гидрокарбонатам натрия является качественной на карбоксильную группу, внешний признак выделение пузырьков газа (какого?). Для этого опыта лучше использовать свежеприготовленный насыщенный водный раствор гидрокарбоната натрия: в пробирку вносят примерно 0,1 г NaHCO3 и 1 мл воды (1), смесь можно слегка подогреть на водяой бане.Затем добавляют несколько капель уксусной кислоты (16) или исследуемого вещества. При наличии карбоксильной группы наблюдается выделение углекислого газа.
Записывают наблюдаемый результат и уравнение реакции.
![]()
2.2. Открытие фенолов.
2.2.1. Реакция фенолов с хлоридом железа (III). В пробирке растворяют маленький кристаллик фенола (17) или неизвестного вещества (один кристаллик или одну каплю жидкости) в нескольких капелях спирта (20), затем добавляют 12 мл дистиллированной воды (1). При встряхивании добавляют 12 капли 1%-ного водного раствора FeCl3 (8). При наличии фенольного гидроксила появляется интенсивная окраска раствора. Отмечают цвет раствора, его интенсивность, записывают уравнение реакции.
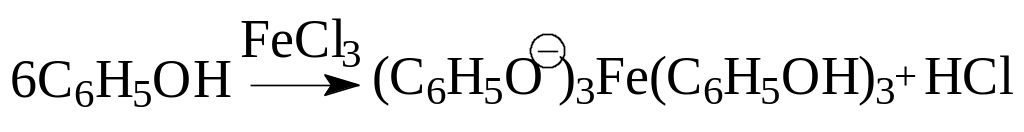
Большинство фенолов и фенолокислот дают с хлоридом железа интенсивное сине-фиолетовое окрашивание, реже красное или зеленое (см. табл 2.8). При этом появившаяся окраска может быстро исчезнуть за счет протекающей реакции окисления многоатомного фенола под действием хлорида железа. Проба считается отрицательной, если сохраняется желтый цвет хлорида железа.
2.2.2. Реакция с бромной водой. Готовят, как описано в опыте 2.3.1, раствор фенола (17) или неизвестного вещества в 12 мл воды (1), затем по каплям добавляют бромную воду (2) (опыт проводить в вытяжном шкафу!). При наличии фенола сначала наблюдается обесцвечивание бромной воды, а при дальнейшем прибавлении реагента образование мути и выпадение белого или окрашенного осадка. Записывают уравнение реакции, указывают цвет образующегося продукта.
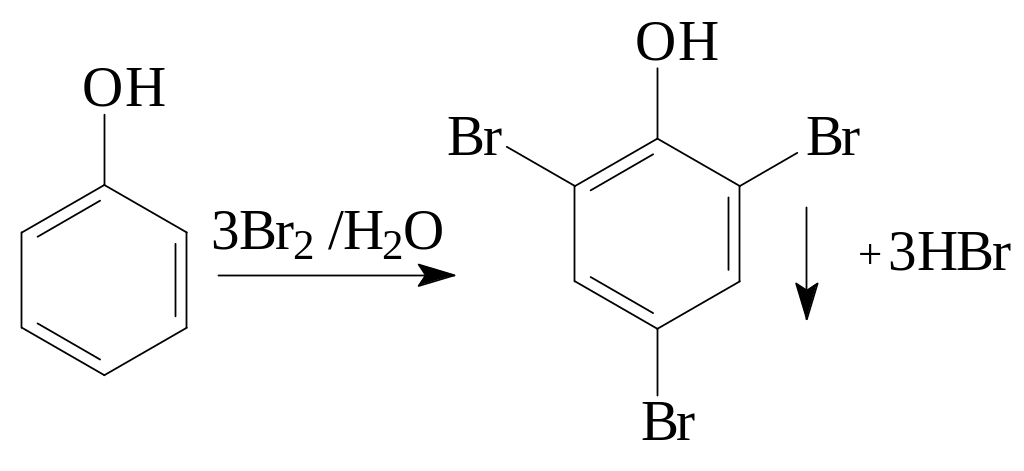
Положительные пробы в опытах с хлоридом железа и с бромной водой доказывают наличие в исследуемом веществе фенольного гидроксила.
