
- •Техника безопасности при работе в химической лаборатории
- •Физические константы органических веществ
- •Лабораторная работа Определение температуры кипения и показателя преломления неизвестного вещества
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1) Определение температуры плавления с применением прибора Сиволобова.
- •Лабораторная работа Определение температуры плавления неизвестного вещества с применением прибора Сиволобова
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1.1. Исследование физических свойств вещества
- •1.2. Проба на свечение пламени
- •1.3. Проба Бельштейна на галоген
- •1.4. Открытие кратной связи
- •1.5. Открытие бензольного кольца
- •1.6. Открытие боковой цепи в бензольном кольце
- •1.7. Открытие галогена в алифатической цепи
- •Аналитическая задача
- •Качественный анализ неизвестного вещества
- •Задача 1
- •1. Исследование физических свойств вещества
- •2. Качественные реакции
- •2.1.Открытие карбоксильной группы
- •2.2. Открытие фенолов.
- •2.3. Открытие карбонильной группы (открытие альдегидов и кетонов).
- •2.4. Открытие спиртов.
- •2.5. Открытие сложного эфира.
- •Идентификация индивидуальных веществ
- •1. Идентификация кислот
- •3. Идентификация альдегидов и кетонов.
- •4. Идентификация спиртов.
- •Аналитическая задача
- •Идентификация неизвестного вещества (образец)
- •Дата Подпись преподавателя Задача 2
- •1.1. Предварительные испытания
- •1.2. Качественные реакции
- •1.2.1. Открытие углеводов реакцией Молиша
- •1.2.2. Открытие моносахаридов реакцией с калий-гидроксидом
- •1.2.3. Открытие альдоз и кетоз реакцией Троммера
- •1.2.4. Открытие кетоз реакцией Селиванова
- •1.3. Идентификация моно- и дисахаридов
- •1.3.1. Фруктоза
- •1.3.2. Ксилоза
- •1.3.3. Глюкоза
- •1.3.4. Мальтоза (солодовый сахар)
- •1.3.5. Сахароза (свекловичный, тростниковый сахар)
- •1.4. Идентификация полисахаридов
- •1.4.1. Амилоза и амилопектин
- •1.4.2. Открытие целлюлозы
- •1.5. Идентификация производных сахаров
- •1.5.1. Сорбит
- •1.5.2. Глюкаровая кислота
- •Аналитическая задача по теме «Углеводы»
- •Дата Подпись преподавателя Задача 3
1.1. Предварительные испытания
Моно- и дисахариды представляют собой белые кристаллические вещества, сладкие на вкус, растворимые в воде и нерастворимые в диэтиловом эфире и углеводородах (гексане, петролейном эфире и др.) (см. табл. П.1.10).
Полисахариды это аморфные вещества, иногда со слабо- выраженным кристаллическим строением, без вкуса и запаха, нерастворимы (отдельные представители малорастворимы) в воде и органических растворителях. Например, целлюлоза не растворяется в воде; компоненты крахмала: амилоза растворима в горячей воде, но не образует клейстера (геля); амилопектин не растворяется в холодной воде, а в горячей образует клейстер (табл. 1).
Таблица 1
Свойства полисахаридов
Полисахарид |
Растворимость в воде |
Реакция с иодом |
Амилоза |
Хорошо растворима в горячей воде, не образу-ет клейстера |
Синее окрашивание |
Амилопектин |
В холодной воде не раст-ворим, в горячей воде образует клейстер |
Сине-фиолетовое (красно-ватое) окрашивание, которое при нагревании исчезает, но снова появляется при охлаждении |
Целлюлоза |
Не растворима в холодной и горячей воде |
Не дает окрашивания |
3.1.1. Внешний вид вещества. Охарактеризовать внешний вид полученного вещества: кристаллы, аморфная масса, цвет, запах.
3.1.2. Растворимость. Исследование растворимости вещества в воде: в пробирку с 1 мл воды добавляют несколько крупинок вещества и смесь встряхивают. Если вещество сразу не растворяется, то пробирку нагревают на водяной бане.
На основании сравнения полученных результатов с данными табл. 1 и П.1.10. можно сделать предварительное заключение о классе неизвестного углевода: хорошо растворимые в воде вещества могут относиться к моно-, дисахаридам и их производным; не растворимые в холодной воде углеводы являются полисахаридами.
1.2. Качественные реакции
1.2.1. Открытие углеводов реакцией Молиша
Эту реакцию дают все углеводы, причем олиго- и полисахариды в условиях реакции сначала гидролизуются до моносахаридов. Моносахариды под действием концентрированной H2SO4 расщепля-ются до фурфурола или гидроксиметилфурфурола, которые при взаимодействии с -нафтолом образуют окрашенные продукты кон-денсации: наблюдается появление красно-фиолетового кольца на границе раздела фаз. Образование окрашенных продуктов конденса-ции свидетельствует о наличии углеводов.
Эта реакция очень чувствительная, наблюдается при концентрации альдоз 0,01%.
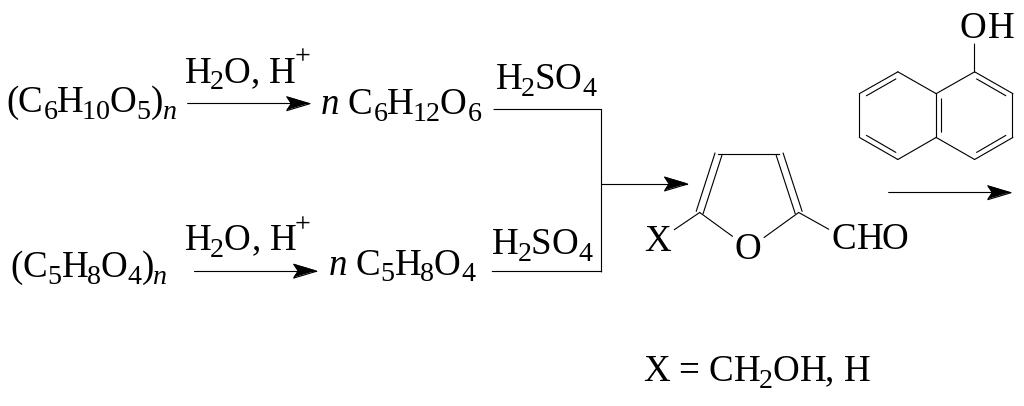

Реактивы: 10%-ный спиртовой раствор -нафтола; серная кислота.
В пробирку с 1 мл воды помещают несколько крупинок (~0,01 г) исследуемого вещества (или используют 1 мл раствора, полученного в опыте 1.1.2), встряхивают и добавляют 12 капли 10%-ного спиртового раствора -нафтола. Потом, наклонив пробирку, осторожно по стенке приливают с помощью пипетки 1 мл концентрированной серной кислоты так, чтобы она опустилась на дно. При наличии углеводов на границе слоев быстро образуется красно-фиолетовое кольцо. В отсутствие углеводов жидкость может позеленеть или пожелтеть, но фиолетовое кольцо не образуется.
