
- •Техника безопасности при работе в химической лаборатории
- •Физические константы органических веществ
- •Лабораторная работа Определение температуры кипения и показателя преломления неизвестного вещества
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1) Определение температуры плавления с применением прибора Сиволобова.
- •Лабораторная работа Определение температуры плавления неизвестного вещества с применением прибора Сиволобова
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1.1. Исследование физических свойств вещества
- •1.2. Проба на свечение пламени
- •1.3. Проба Бельштейна на галоген
- •1.4. Открытие кратной связи
- •1.5. Открытие бензольного кольца
- •1.6. Открытие боковой цепи в бензольном кольце
- •1.7. Открытие галогена в алифатической цепи
- •Аналитическая задача
- •Качественный анализ неизвестного вещества
- •Задача 1
- •1. Исследование физических свойств вещества
- •2. Качественные реакции
- •2.1.Открытие карбоксильной группы
- •2.2. Открытие фенолов.
- •2.3. Открытие карбонильной группы (открытие альдегидов и кетонов).
- •2.4. Открытие спиртов.
- •2.5. Открытие сложного эфира.
- •Идентификация индивидуальных веществ
- •1. Идентификация кислот
- •3. Идентификация альдегидов и кетонов.
- •4. Идентификация спиртов.
- •Аналитическая задача
- •Идентификация неизвестного вещества (образец)
- •Дата Подпись преподавателя Задача 2
- •1.1. Предварительные испытания
- •1.2. Качественные реакции
- •1.2.1. Открытие углеводов реакцией Молиша
- •1.2.2. Открытие моносахаридов реакцией с калий-гидроксидом
- •1.2.3. Открытие альдоз и кетоз реакцией Троммера
- •1.2.4. Открытие кетоз реакцией Селиванова
- •1.3. Идентификация моно- и дисахаридов
- •1.3.1. Фруктоза
- •1.3.2. Ксилоза
- •1.3.3. Глюкоза
- •1.3.4. Мальтоза (солодовый сахар)
- •1.3.5. Сахароза (свекловичный, тростниковый сахар)
- •1.4. Идентификация полисахаридов
- •1.4.1. Амилоза и амилопектин
- •1.4.2. Открытие целлюлозы
- •1.5. Идентификация производных сахаров
- •1.5.1. Сорбит
- •1.5.2. Глюкаровая кислота
- •Аналитическая задача по теме «Углеводы»
- •Дата Подпись преподавателя Задача 3
3. Идентификация альдегидов и кетонов.
Формальдегид (муравьиный альдегид, метаналь) представляет собой бесцветный газ с резким запахом Ткип. 19С), поэтому обычно используют формалин 40%-ный водный раствор формальдегида. Отличить формальдегид от других альдегидов можно с помощью реакции с фуксинсернистой кислотой (см. 2.3.5), так как окрашенный продукт взаимодействия формальдегида при добавлении нескольких капель 20%-но Н2SO4 (30) не изменяет окраски. С другими альдегидами в этих условиях продукт обесцвечивается.
Уксусный альдегид, ацетон, метилэтилкетон. В этих веществах имеется СН3СО-группировку, что позволяет их идентифицировать йодоформной пробой (опыт 2.3.4). Этаналь также восстанавливает гидроксид меди (II) (опыт 2.3.1), а кетоны различают по физическим константам.
Пропионовый и масляный альдегиды (бутаналь) открываются реакциями на алдегидную группу, в отличие от этаналя не дают иодоформной пробы(опыт 2.3.4), идентифцируют с помощью физических констант.
Трихлоруксусный альдегид (хлораль) содержит атомы хлора, поэтому его идентифцируют с помощью пробы Бейльштейна (опыт 1.3).
Бензальдегид в отличие от алифатических альдегидов не восстанавливает гидроксид меди (II), но дает другие реакции альдегидов (опыт 2.3). Бензальдегид, как и другие ароматические альдегиды, имеет характерный запах и легко окисляется кислородом воздуха, что позволяет идентифицировать эти соединения. 1 каплю альдегида наносят на предметное стекло и оставляют на 12 ч, в течение которых появляются белые кристаллы бензойной кислоты. Окончательно идентифицировать бензальдегид можно по физическим константам.
Циклогексанон дает положительную реакцию с гидроксиламином (опыт 2.3.1) и отрицательную иодоформную пробу, окончательно его идентифицируют по физическим свойствам.
4. Идентификация спиртов.
Метанол (метиловый или древесный спирт, карбинол) очень сильный яд, поэтому при работе с ним требуется соблюдать повышенные меры безопасности. Метанол открывают по способности окисляется до формальдегида, восставливая при этом оксид меди (II) до Cu. В пробирку помещают 23 капли спирта. Медную проволоку (41), скрученную в спираль, дважды нагревают докрасна в пламени горелки и затем быстро опускают в спирт. Черная поверхность спирали превращается в золотистую (почему?). Образующийся при этом формальдегид открывают качественными реакциями на альдегидгную группу (опыт 2.3).
Этанол (этиловый спирт) как и метанол окисляется оксидом меди (II) в условиях предыдущего опыта до уксусного альдегида. Последний в отличие от формальдегида дает йодоформную пробу (опыт 2.3.4).
Пропан-2-ол (изопропиловый спирт) открывают иодоформной пробой, (опыт 2.3.4), однако реакцию проводят при нагревании (60°С), чтобы произошло первоначальное окисление спирта до пропанона, который является метилкетоном.
2-Метилпропан-2-ол (третбутиловый спирт) как третичный спирт легко замещает гидроксильную группу на галоген при действии HHal. К 1 мл концентрированной соляной кислоты добавляют 5 капель спирта, пробирку хорошо встряхивают, наблюдая за изменениями в течение двух минут. Образующийся хлоралкан не растворим в водном растворе кислоты, поэтому наблюдается помутнение раствора. Первичные и вторичные спирты в этих условиях не реагируют.
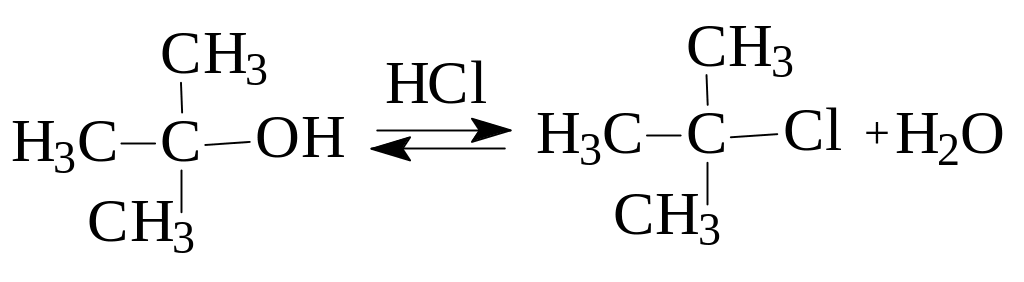
Этан-1,2-диол (этиленгликоль), пропан-1,2,3-триол (глицерин) как многоатомные спирты открывают с помощью реакции с гидроксидом меди (II) (опыт 2.4.1). Кроме того, глицерин в результате внутримолекулярной дегидратации превращается в акролеина, который затем идентифицируют качественными реакциями на альдегидную группу (опыты 2.4).
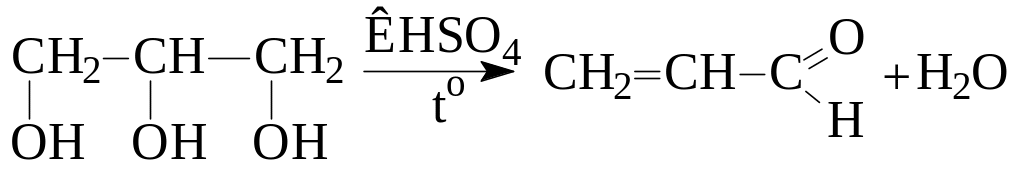
В сухую пробирку помещают 35 кристаллов гидросульфата калия КHSO4 (44) и 1 каплю глицерина. Смесь осторожно нагревают на пламени горелки. Наблюдается побурение жидкости в пробирке и появление очень характерного едкого запаха акролеина, который знаком благодаря тому, что образуется в процессе жарения при подгорании жира, который представляет собой сложнвый эфир глицеринаи и высших жирных кислот. Образующийся акролеин обнаруживают по покраснению бумажки, смоченной фуксинсернистой кислотой (48) и внесенной в пробирку с веществом.
Другие спирты идентифицируют по физическим константам.
5. Идентификация сложных эфиров. Сложные эфиры алифатических спиртов представляют собой жидкости с характерным приятным фруктовым запахом, открывают реакцией с гидроксидом натрия (опыт 2.5), идентифицируют по физическим свойствам.
