
- •Техника безопасности при работе в химической лаборатории
- •Физические константы органических веществ
- •Лабораторная работа Определение температуры кипения и показателя преломления неизвестного вещества
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1) Определение температуры плавления с применением прибора Сиволобова.
- •Лабораторная работа Определение температуры плавления неизвестного вещества с применением прибора Сиволобова
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1.1. Исследование физических свойств вещества
- •1.2. Проба на свечение пламени
- •1.3. Проба Бельштейна на галоген
- •1.4. Открытие кратной связи
- •1.5. Открытие бензольного кольца
- •1.6. Открытие боковой цепи в бензольном кольце
- •1.7. Открытие галогена в алифатической цепи
- •Аналитическая задача
- •Качественный анализ неизвестного вещества
- •Задача 1
- •1. Исследование физических свойств вещества
- •2. Качественные реакции
- •2.1.Открытие карбоксильной группы
- •2.2. Открытие фенолов.
- •2.3. Открытие карбонильной группы (открытие альдегидов и кетонов).
- •2.4. Открытие спиртов.
- •2.5. Открытие сложного эфира.
- •Идентификация индивидуальных веществ
- •1. Идентификация кислот
- •3. Идентификация альдегидов и кетонов.
- •4. Идентификация спиртов.
- •Аналитическая задача
- •Идентификация неизвестного вещества (образец)
- •Дата Подпись преподавателя Задача 2
- •1.1. Предварительные испытания
- •1.2. Качественные реакции
- •1.2.1. Открытие углеводов реакцией Молиша
- •1.2.2. Открытие моносахаридов реакцией с калий-гидроксидом
- •1.2.3. Открытие альдоз и кетоз реакцией Троммера
- •1.2.4. Открытие кетоз реакцией Селиванова
- •1.3. Идентификация моно- и дисахаридов
- •1.3.1. Фруктоза
- •1.3.2. Ксилоза
- •1.3.3. Глюкоза
- •1.3.4. Мальтоза (солодовый сахар)
- •1.3.5. Сахароза (свекловичный, тростниковый сахар)
- •1.4. Идентификация полисахаридов
- •1.4.1. Амилоза и амилопектин
- •1.4.2. Открытие целлюлозы
- •1.5. Идентификация производных сахаров
- •1.5.1. Сорбит
- •1.5.2. Глюкаровая кислота
- •Аналитическая задача по теме «Углеводы»
- •Дата Подпись преподавателя Задача 3
2.3. Открытие карбонильной группы (открытие альдегидов и кетонов).
2.3.1. Реакция с гидроксиламином солянокислым. В пробирку помещают одну каплю 0,2%-ного спиртового раствора метилового оранжевого (50), 23 капли ацетона (18) или неизвестного вещества. Для кристаллического малорастворимого в воде неизвестного вещества, сначала готовят его (0,05 г) раствор в небольшом количестве спирта (20).Отмечают рН среды. В нейтральной среде индикатор имеет оранжевый цвет, в кислой красный, в щелочной желтый. В двух последних случаях доводят рН до нейтральной добавлением соответственно 1%-ного раствора гидроксида натрия или соляной кислоты.
Затем к полученной смеси добавляют 0,5 мл 3%-ного раствора НОNН2HCl (28), при отсутствии изменений нагревают на водяной бане, отмечая изменение цвета индикатора. Возможно выпадение кристаллов оксима карбонильного соединения.
Покраснение индикатора свидетельствует о положительной реакции на альдегид или кетон (почему?). Записывают уравнение реакции.
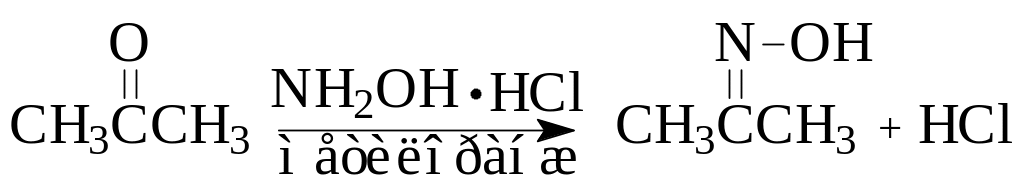
2.3.2. Реакция окисления альдегидов гидроксидом меди (II). В пробирку помещают 10 капель 5%-ного NаОН (6) и добавляют 12 капли 5%-ного раствора CuSO4 (7). К выпавшему осадку гидроксида меди прибавляют 23 капли неизвестного вещества и раствор встряхивают. Затем медленно нагревают в пламени горелки только верхнюю часть пробирки до начала кипения. Если вещество содержит альдегидную группу, то происходит изменение цвета осадка: вначале образуется гидроксид меди (I) желтого цвета, который при нагревании превращается в оксид меди (I) красного цвета.
![]()

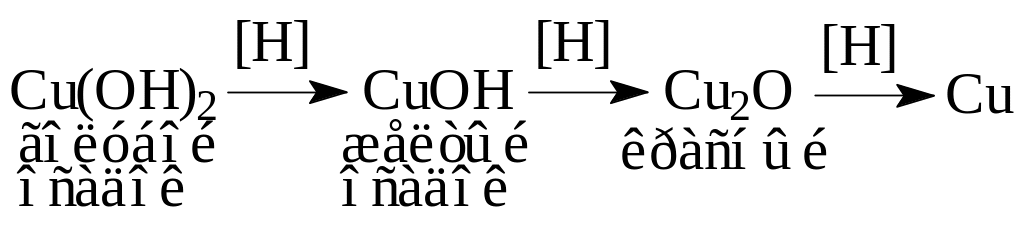
Кетоны эту реакцию не дают. Уравнение реакции записывают на примере окисления уксусного альдегида.
2.3.3. Открытие альдегидов и метилкетонов реакцией с гидросульфитом (бисульфитом) натрия. На предметное стекло помещают 1 каплю насыщенного раствора NaHSO3 (25), добавляют 1 каплю ацетона (18) или неизвестного вещества, смесь перемешивают стеклянной палочкой. При образовании гидросульфитного производного карбонильного соединения выпадает кристаллический осадок. Записывают уравнение реакции, отмечают внешний вид кристаллов.
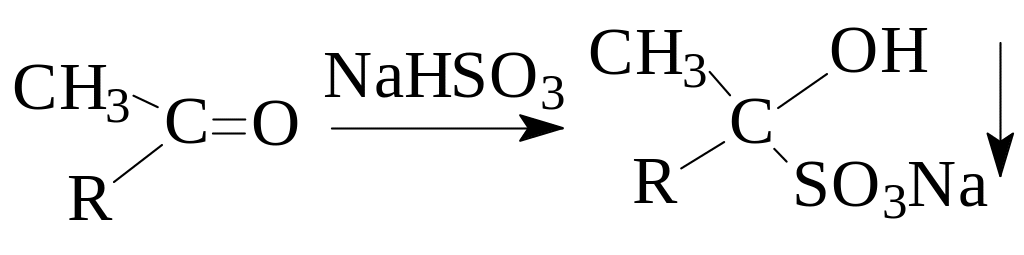
Образование кристаллического осадка свидетельствует о наличии альдегида или метилкетона..
2.3.4. Открытие метилкетонов и уксусного альдегида иодоформной пробой. К 5 каплям 2%-ного раствора йода в растворе иодида калия (9) добавляют 5%-ный NаОН (6) почти до обесцвечивания желтой окраски иода. Затем прибавляют 12 капли ацетона или неизвестного вещества. При наличии метилкетонной группировки выпадает желтый осадок или образуется муть, отмечается с характерным стойким «больничным»запахом йодоформа. Записывают уравнение реакции.

Уксусный альдегид (R=H), поскольку содержит метилкарбонильную группировку, также дает эту реакцию.
При нагревании иодоформную пробу дают метилкарбинолы СН3СH(ОН)R.
2.3.5. Открытие альдегидов и ацетона реакцией с фуксинсернистой кислотой. В пробирку помещают 0,5 мл бесцветного раствора фуксинсернистой кислоты (48), 1 каплю ацетона (18) или неизвестного вещества (кристаллик твердого вещества) и полученную смесь хорошо встряхивают. При наличии альдегидной группы раствор постепенно окрашивается в малиново-красный цвет. Эту реакцию дают все альдегиды, а также диметилкетон (ацетон).
