
- •Визначення залежності швидкості хімічних реакцій від різних умов
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •4.1. Вплив температури на швидкість реакції.
- •4.2. Вплив поверхні зіткнення на швидкість хімічної реакції.
- •4.3. Вплив каталізатора на швидкість хімічної реакції,
- •4.4. Вплив інгібітору на швидкість хімічної реакції.
- •5. Вимоги до звіту
- •6. Техніка безпеки
- •7. Контрольні питання
- •8. Література
- •Вивчення моделі проточного трубчастого реактора
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади і посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Вивчення моделі реактору ідеального змішування
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •2.Хімічні реактиви, прилади, посуд
- •3.Опис лабораторної установки
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів
- •Одержання нафтопродуктів прямою перегонкою нафти
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •Визначення густини пікнометром
- •Визначення в 'язкості
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи.
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Дослідження корозії металів
- •1. Теоретичні основи
- •Показники корозії металів
- •2. Хімічні реактиви та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •Отримання їдкого натрію (NаOh) і хлору електрохімічним методом
- •1.Теоретичні основи
- •2.Хімічні реактиви, прилади та посуд
- •3.Опис лабораторної установки
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів
- •Одержання сульфату амонію
- •1.Теоретичні основи
- •2.Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4.Послідовність виконання роботи
- •5.Опрацювання результатів
- •2. Хімічні реактиви, прилади та посуд
- •3. Послідовність виконання роботи
- •3.1 Визначення твердості води
- •3.2 Визначення хлоридів
- •3.3 Визначення масової концентрації двовалентного і тривалентного заліза
- •3.4 Визначення масової концентрації міді
- •3.5 Визначення масової концентрації хрому
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Одержання і дослідження конденсаційних смол (новолочна смола)
- •Теоретичні основи
- •2. Хімічні реактиви та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
- •5. Опрацювання результатів
- •6. Вимоги до звіту
- •7. Техніка безпеки
- •8. Контрольні питання
- •9. Література
- •Очищення хімічних реагентів ( реактивів) методом прямої перегонки
- •1. Теоретичні основи
- •2. Хімічні реактиви, прилади та посуд
- •3. Опис лабораторної установки
- •4. Послідовність виконання роботи
2. Хімічні реактиви та посуд
Реактиви:
фенол - 50мл;
формальдегід (формалін) - 50мл;
концентрована сірчана кислота - 20мл;
концентрована соляна кислота - 20мл;
щавлева кислота - 20г;
гліцерин- 100 мл.
Прилади та посуд:
колба кругла тришийкова;
зворотний холодильник-1 шт.;
пробірки - 3 шт.;
колба, V200 - 2 шт.;
мішалка;
водяна баня;
фарфорова чашка -1 шт.;
капіляри - 2 шт.;
термометр - 1 шт.:
сушильна шафа (180-200°С);
електрична плита;
ваги технічні - 1 шт.
3. Опис лабораторної установки
Лабораторна установка (рисунок 12.1) складається з тришийкової кругло донної колби 1, яка нагрівається на водяній бані 5, в ній перемішується мішалкою 4 суміш фенолу, формальдегіду і каталізатора. Зворотний холодильник 2 вставлений в середню шийку колби, термометр З для контролю температурного режиму вставлений через пробку 7 в бокову шийку колби. Підігрів ведеться на електричній плиті 6.
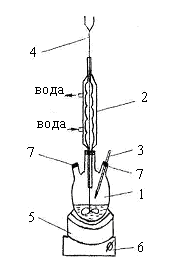
1 - кругло донна тришийкова колба; 2 - зворотний холодильник; 3 - термометр;
4 - мішалка; 5 - водяна баня; 6 - електрична плита; 7 - пробка.
Рисунок 12.1 - Лабораторна установка
Лабораторний прилад для визначення температури розм'якшення і плавлення (рисунок 12.2) складається з колби 1, в яку заливається гліцерин. Пробірка 2 вставляється в колбу. Термометр 3 на пробці вставляється в пробірку. До нього прикріплюються два капіляри 4 з смолою.
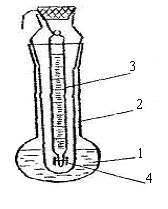
- колба з гліцерином; 2 - пробірка; 3 - термометр; 4 - капіляри.
Рисунок 12.2 - Прилад для визначення температури розм'якшення і плавлення
4. Послідовність виконання роботи
Суміш фенолу і формальдегіду (формалін - водяний розчин формальдегіду) і необхідну кількість каталізатора поміщають в круглодонну тришийкову колбу 1. В середню шийку колби вставляють на пробці зворотний холодильник 2. В один бічний отвір поміщають термометр 3, другий закривають пробкою 7. Через внутрішню трубку холодильника опускають мішалку 4. Реакційну суміш нагрівають на водяній бані 5 в колбі при температурі 90-95°С, доки утворюваний водяний шар не перестане змінюватися в об'ємі. Для контролю за ходом реакції з бічного отвору колби беруть пробу реакційної суміші, охолоджуючи її в пробірці (струшуванням) до 15-20°С. Каламуть в пробірці вказує на кінець реакції. Необхідно звернути увагу на інтенсивність протікання реакції взаємодії фенолу з формальдегідом. Після 20-40 хв нагрівання рідина в колбі може закипіти. В цьому випадку необхідно призупинити нагрівання і зняти колбу з бані 5. Реакція продовжується деякий час без подальшого нагрівання (за рахунок теплоти конденсації). Далі колбу знову занурюють в гарячу водяну баню і продовжують нагрівання, доки суміш не розділиться на два шари. Після цього суміш перестають нагрівати і дають відстоятися водяному шару, який потім зливають, а смолу переливають в фарфорову чашку і сушать, спочатку на водяній бані, а потім на піщаній при температурі 170-200°С.
Після закінчення сушіння смолу зважують і визначають її вихід за відношенням до взятих реагентів (фарфорова чашка, в якій відбувається сушіння, повинна бути попередньо зважена).
Новолочні смоли можуть бути одержані в різних молярних відношеннях фенолу і формальдегіду з різними каталізаторами.
Для визначення температури розм'якшення і плавлення існують різні методи. В лабораторній роботі будемо використовувати метод визначення температури розм'якшення і плавлення в капілярі. Для цього використовуємо прилад, зображений на рис. 7.2. У колбу 1 наливають гліцерин, в її верхній отвір вставляють пробірку, в яку через пробку вводять термометр 3 d=6-8 мм з шкалою 0-200°С. Тонко подрібнену смолу в кількості 0,01 г поміщають в капіляри з тонкого скла висотою 10-15 мм з внутрішнім діаметром 1,5 мм із запаяним кінцем. Смолу набирають так, щоб після старанного ущільнення одержати стовпчик висотою 3-4 мм. Ущільнення ведуть за допомогою двадцятикратного вільного падіння капіляра з смолою в 0,5 м скляній трубці.
Два капіляри прикріплюють до термометра за допомогою тонкої гумової нитки. Капіляри розміщують так, щоб стовпчики смоли знаходилися на рівні ртутної кульки термометра. Термометр з капілярами встановлюють в приладі так, щоб кулька термометра була нижче рівня рідини в колбі.
Потім прилад нагрівають, але так, щоб перші 10-15 хв температура піднімалася зі швидкістю 5 градусів на хв, а потім (після 40°С) нагрівання повинно відбуватися зі швидкістю 1 градус на хв.
Коли окремі частинки порошкоподібної смоли почнуть спікатися, відмічають цей момент як температуру розм'якшення смоли.
Далі продовжують нагрівання і відмічають температуру, при якій смола починає втрачати свій порошкоподібний стан. Ця точка відповідає температурі плавлення смоли.
Визначення повторюють декілька разів (2-3), для розрахунків беруть середній із одержаних результатів. Різниця між отриманими значеннями не повинна перевищувати 1 °С.
