
- •Лекція 5
- •5.1. Основні означення
- •5.2. Закон гесса
- •5.3.Розрахунок теплових ефектів
- •5.3.1. Розрахунок теплових ефектів хемічних реакцій за теплом утворення сполук
- •Наприклад, отримання при 25 ºС Al2(sо4)3 з кристалічного Аl2о3 (т) і ґазу sо3 за реакцією:
- •5.3.2. Тепловий ефект утворення сполуки певного аґреґатного стану (тепло аґреґатного стану)
- •5.3.3. Тепловий ефект утворення сполуки у розчині (тепло розчинення)
- •5.3.4. Тепло розведення розчину
- •5.3.5. Тепло взаємодії кислоти та основи
- •5.3.6. Розрахунок теплового ефекту хемічних реакцій за теплом згоряння
- •Лекція 6
- •6.1.Означення другого начала термодинаміки
- •6.2. Рівняння другого начала термодинаміки
- •6.3. Коефіцієнти ефективности термодинамічних циклів
- •6.3.1.Прямий цикл
- •6.3.2. Зворотній цикл
- •6.4. Цикл карно
- •6.4.1. Прямий цикл Карно
- •6.4.2. Зворотній цикл Карно
- •6.5. Математичні вирази другого начала термодинаміки
- •Термодинамічний процес (незамкнутий цикл)
- •7.1.Означення характеристичних функцій і термодинамічних потенціалів
- •7.2. Ентропія, внутрішня енергія і ентальпія як характеристичні функції
- •7.3. Ізохорно-ізотермний потенціал гельмгольца
- •7.4. Ізобарно-ізотермний потенціал ґіббса
- •7.5.Десять вислідів з попередньої частини лекції
- •7.6. Рівняння гельмгольца
- •7.7. Рівняння ґіббса
- •7.8.Рівняння ґіббса-гельмгольца
- •Лекція 8
- •8.1. Залежність характеристичних функцій та ентропії від тиску. Фуґітивність
- •Стандартний стан
- •8.2. Хемічний потенціал
- •8.3.Хемічний потенціал ідеального ґазу
- •8.4.Хемічний потенціал реального ґазу
- •Лекція 9
- •9.1. Активність реальних ґазів і розчинів
- •9.1.1. Активність реального ґазу
- •9.1.2. Активність компонентів розчину
- •9.2. Хемічна рівновага
- •9.2.2. Рівняння рівноваги для суміші ідеальних ґазів і константа рівноваги
- •9.2.3. Рівняння рівноваги для ідеального розчину і константа рівноваги
- •9.2.4.Рівняння рівноваги для суміші реальних ґазів і константа рівноваги
- •9.2.5. Рівняння рівноваги для неідеальних розчинів і константа рівноваги
- •9.2.6. Закон діяння мас Ґульдберґа-Воґе
- •9.3.Рівняння ізотерми і напрямок хемічної реакції
- •Для ідеального розчину
- •Для суміші реальних ґазів
- •9.4.Стандартний потенціал ґіббса хемічної реакції Введемо поняття стандартного потенціалу Ґіббса і знайдемо його зв’язок з константами рівноваги хемічної реакції:
- •Для суміші ідеальних ґазів
- •Для ідеального розчину
- •Для неідеального розчину
- •9.5. Константа рівноваги і стандартний потенціал ґіббса хемічної реакції
- •9.6.Константа рівноваги і способи вираження складу реакційної суміші
- •9.7.Вплив тиску на рівновагу хемічної реакції. Принцип зміщення рівноваги ле шательє-брауна
- •Приклади
- •Гетерогенна хемічна рівновага
- •9.9.Залежність константи рівноваги від температури. Рівняння ізобари та ізохори хемічної реакції
- •Рекомендована література
- •Використані джерела інформації
Приклади рівнянь для констант рівноваги:
Приклад 1. С(т)+СО2(г)=2СО(г), вважаючи ґазову фазу сумішшю ідеальних ґазів; активність чистого вуглецю приймаємо сталою а(с)≈1:
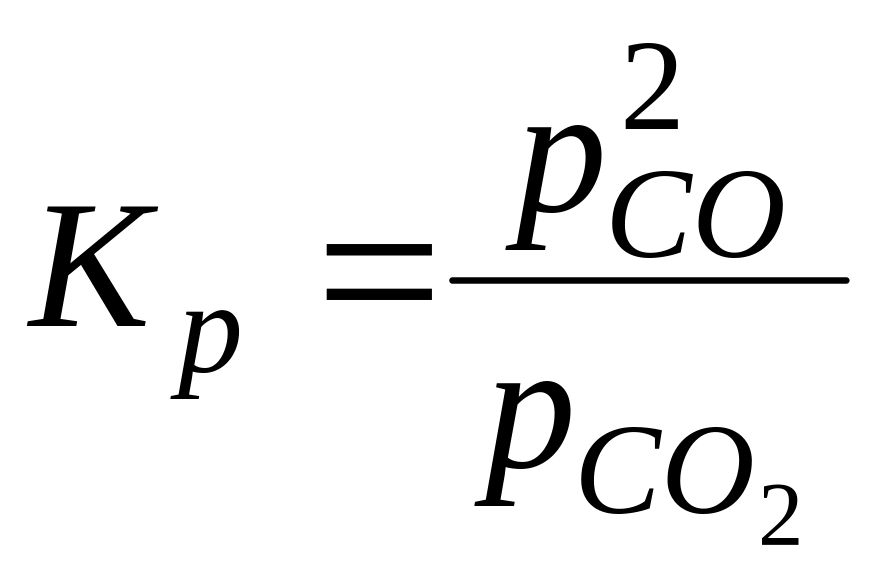 . (9.109)
. (9.109)
Приклад 2. FeO(р)+H2(г)=Fe(р)+H2O(г), вважаючи ґазову фазу сумішшю ідеальних ґазів; FeO погано розчинний в Fe; активність а(Fe)=1:
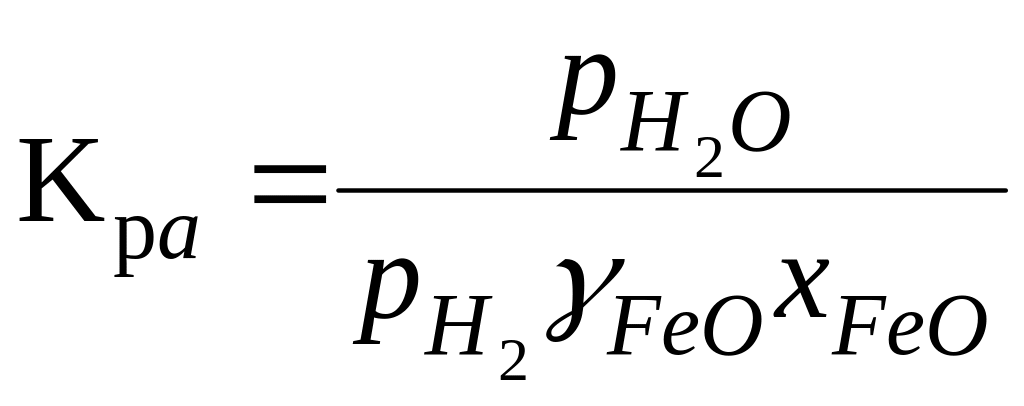 , (9.110)
, (9.110)
де
![]() – коефіцієнт активности оксиду феруму
(ІІ) в Fe;
– коефіцієнт активности оксиду феруму
(ІІ) в Fe;
![]() – молярна
частка оксиду феруму (ІІ) в Fe(р).
– молярна
частка оксиду феруму (ІІ) в Fe(р).
9.9.Залежність константи рівноваги від температури. Рівняння ізобари та ізохори хемічної реакції
Рівняння ізотерми хемічної реакції в суміші ідеальних ґазів:
![]() . (9.111)
. (9.111)
Згідно рівняння Ґіббса-Гельмгольца
![]() , (9.112)
, (9.112)
де
ΔН – тепловий ефект хемічної реакції
при Т,р=const,
отримаємо з (9.111), взявши похідну по dT,
і вважаючи :![]() :
:
![]() (9.113)
(9.113)
Підставляючи (9.111) і (9.113) у (9.112) при р=const, отримаємо рівняння вант-Гоффа ізобари хемічної реакції:
 . (9.114)
. (9.114)
Аналогічно при V=const отримаємо рівняння вант-Гоффа ізохори хемічної реакції:
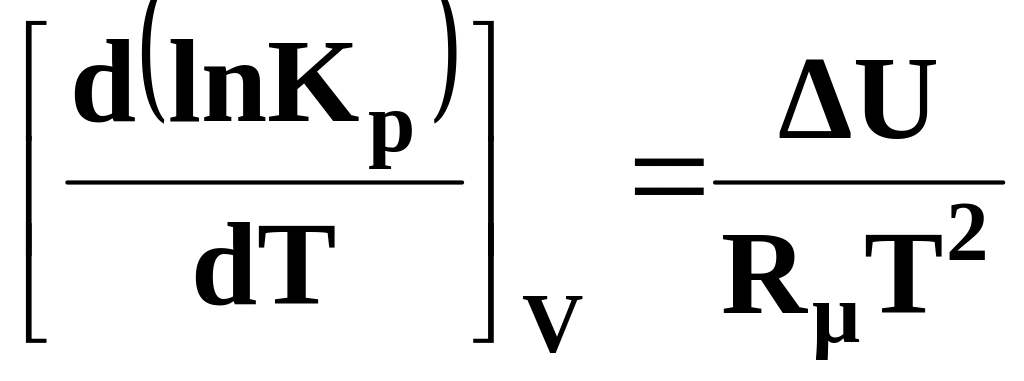 .
(9.115)
.
(9.115)
Якщо реакція протікає у суміші реальних ґазів, то заміна в рівнянні ізобари Кр на Кf при р=const, приведе до рівняння:
 .
(9.116)
.
(9.116)
.Якщо реакція протікає в ідеальному розчині при V=const, то
 .
(9.117)
.
(9.117)
Якщо реакція протікає в неідеальному розчині при V=const, то в рівнянні ізохори (9.117) необхідно Кс замінити на Ка:
 .
(9.118)
.
(9.118)
Рівняння (9.114) (9.115)-(9.118) дозволяють передбачити і дати якісну і кількісну оцінку залежності константи рівноваги від температури:
якщо ΔН>0 (ендотермічна реакція), то температурний коефіцієнт
![]() >0.
(9.119)
>0.
(9.119)
Це означає, що із зростанням температури, Кр ендотермічної реакції завжди зростає і рівновага зсувається вправо.
якщо ΔН<0, то
<0. (9.120)
Це означає, що із зростанням температури, Кр екзотермічної реакції зсувається вліво.
якщо ΔН=0, то Кр не залежить від Т.
