
- •Лекція 5
- •5.1. Основні означення
- •5.2. Закон гесса
- •5.3.Розрахунок теплових ефектів
- •5.3.1. Розрахунок теплових ефектів хемічних реакцій за теплом утворення сполук
- •Наприклад, отримання при 25 ºС Al2(sо4)3 з кристалічного Аl2о3 (т) і ґазу sо3 за реакцією:
- •5.3.2. Тепловий ефект утворення сполуки певного аґреґатного стану (тепло аґреґатного стану)
- •5.3.3. Тепловий ефект утворення сполуки у розчині (тепло розчинення)
- •5.3.4. Тепло розведення розчину
- •5.3.5. Тепло взаємодії кислоти та основи
- •5.3.6. Розрахунок теплового ефекту хемічних реакцій за теплом згоряння
- •Лекція 6
- •6.1.Означення другого начала термодинаміки
- •6.2. Рівняння другого начала термодинаміки
- •6.3. Коефіцієнти ефективности термодинамічних циклів
- •6.3.1.Прямий цикл
- •6.3.2. Зворотній цикл
- •6.4. Цикл карно
- •6.4.1. Прямий цикл Карно
- •6.4.2. Зворотній цикл Карно
- •6.5. Математичні вирази другого начала термодинаміки
- •Термодинамічний процес (незамкнутий цикл)
- •7.1.Означення характеристичних функцій і термодинамічних потенціалів
- •7.2. Ентропія, внутрішня енергія і ентальпія як характеристичні функції
- •7.3. Ізохорно-ізотермний потенціал гельмгольца
- •7.4. Ізобарно-ізотермний потенціал ґіббса
- •7.5.Десять вислідів з попередньої частини лекції
- •7.6. Рівняння гельмгольца
- •7.7. Рівняння ґіббса
- •7.8.Рівняння ґіббса-гельмгольца
- •Лекція 8
- •8.1. Залежність характеристичних функцій та ентропії від тиску. Фуґітивність
- •Стандартний стан
- •8.2. Хемічний потенціал
- •8.3.Хемічний потенціал ідеального ґазу
- •8.4.Хемічний потенціал реального ґазу
- •Лекція 9
- •9.1. Активність реальних ґазів і розчинів
- •9.1.1. Активність реального ґазу
- •9.1.2. Активність компонентів розчину
- •9.2. Хемічна рівновага
- •9.2.2. Рівняння рівноваги для суміші ідеальних ґазів і константа рівноваги
- •9.2.3. Рівняння рівноваги для ідеального розчину і константа рівноваги
- •9.2.4.Рівняння рівноваги для суміші реальних ґазів і константа рівноваги
- •9.2.5. Рівняння рівноваги для неідеальних розчинів і константа рівноваги
- •9.2.6. Закон діяння мас Ґульдберґа-Воґе
- •9.3.Рівняння ізотерми і напрямок хемічної реакції
- •Для ідеального розчину
- •Для суміші реальних ґазів
- •9.4.Стандартний потенціал ґіббса хемічної реакції Введемо поняття стандартного потенціалу Ґіббса і знайдемо його зв’язок з константами рівноваги хемічної реакції:
- •Для суміші ідеальних ґазів
- •Для ідеального розчину
- •Для неідеального розчину
- •9.5. Константа рівноваги і стандартний потенціал ґіббса хемічної реакції
- •9.6.Константа рівноваги і способи вираження складу реакційної суміші
- •9.7.Вплив тиску на рівновагу хемічної реакції. Принцип зміщення рівноваги ле шательє-брауна
- •Приклади
- •Гетерогенна хемічна рівновага
- •9.9.Залежність константи рівноваги від температури. Рівняння ізобари та ізохори хемічної реакції
- •Рекомендована література
- •Використані джерела інформації
Так при T=const для ідеального ґазу (або суміші ідеальних ґазів) відомі співвідношення:
для ідеального ґазу
![]() ;
(8.3)
;
(8.3)
 ;
(8.4)
;
(8.4)
![]() ;
(8.5)
;
(8.5)
 ;
(8.6)
;
(8.6)
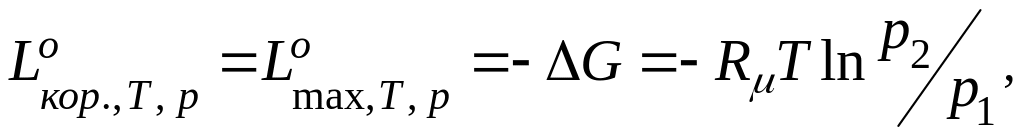 (8.7)
(8.7)
де S, G – ентропія та ізобарно-ізотермний потенціал одного моля ідеального ґазу відповідно;
∆S, ∆G – зміна ентропії та ізобарно-ізотермного потенціалу одного моля ідеального ґазу відповідно при зміні тиску;
![]() ,
KG
– сума
членів, які при T=const
зберігають сталі значення для певного
ґазу і його кількости, які чисельно
дорівнюють
,
KG
– сума
членів, які при T=const
зберігають сталі значення для певного
ґазу і його кількости, які чисельно
дорівнюють
![]() ,
KG=G
для 1 моля, р=1 атм при даній температурі
T=const.
,
KG=G
для 1 моля, р=1 атм при даній температурі
T=const.
![]() -
корисна робота в оборотньому процесі.
-
корисна робота в оборотньому процесі.
для і-го компоненту суміші ідеальних ґазів
![]() ;
(8.8)
;
(8.8)
 ;
(8.9)
;
(8.9)
![]() ;
(8.10)
;
(8.10)
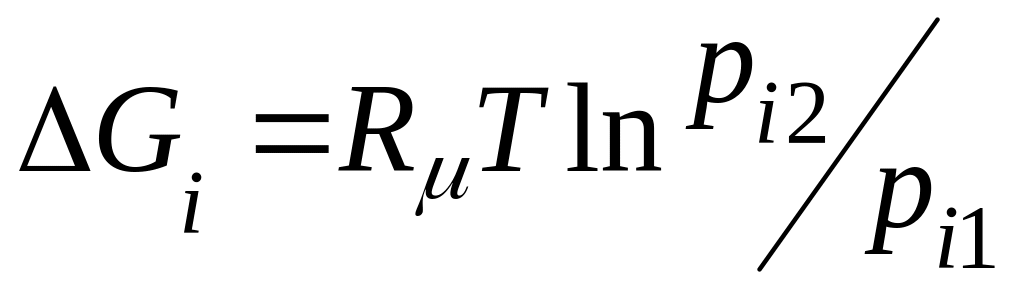 ;
(8.11)
;
(8.11)
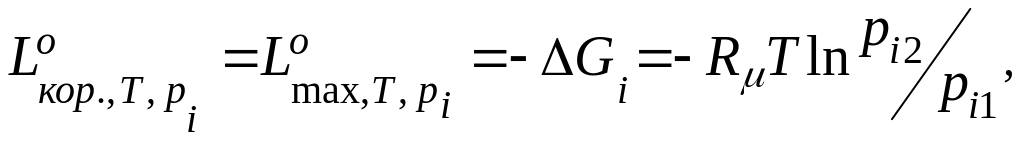 (8.12)
(8.12)
де pi – парціальний тиск і-го компоненту у суміші ідеальних ґазів;
Si – ентропія і-го компоненту у суміші ідеальних ґазів;
Gi – парціальний ізобарно-ізотермний потенціал.
При T=const при підстановці фуґітивности f (fі) замість тиску р (рі) у рівняння (8.3)-(8.12) отримаємо для реального ґазу (або суміші реальних ґазів) такі співвідношення:
для реального ґазу
![]() ;
(8.13)
;
(8.13)
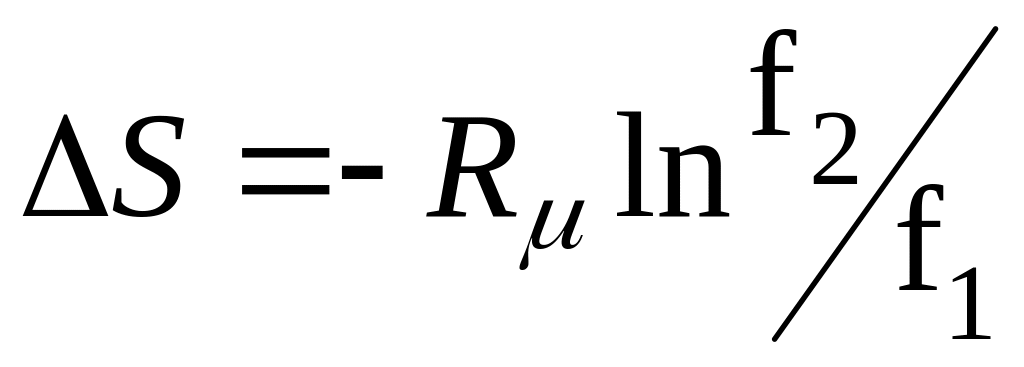 ;
(8.14)
;
(8.14)
![]() ;
(8.15)
;
(8.15)
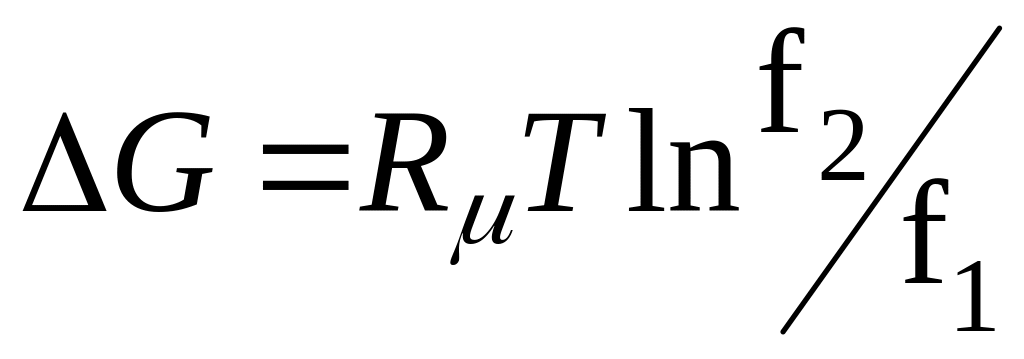 ;
(8.16)
;
(8.16)
 (8.17)
(8.17)
для і-го компоненту суміші реальних ґазів
![]() ;
(8.18)
;
(8.18)
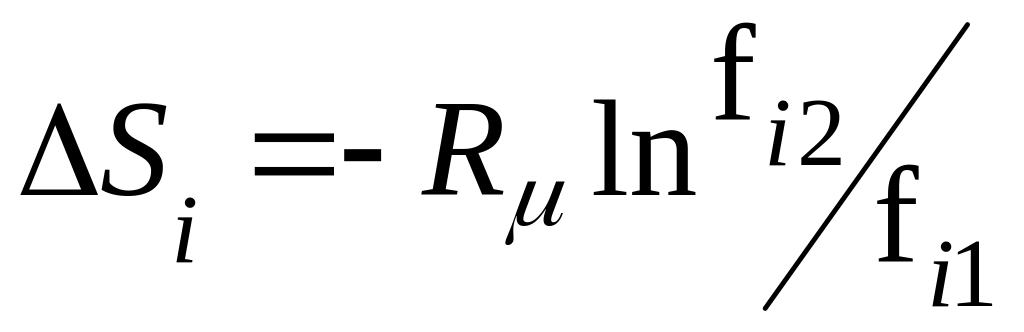 ;
(8.19)
;
(8.19)
![]() ;
(8.20)
;
(8.20)
 ;
(8.21)
;
(8.21)
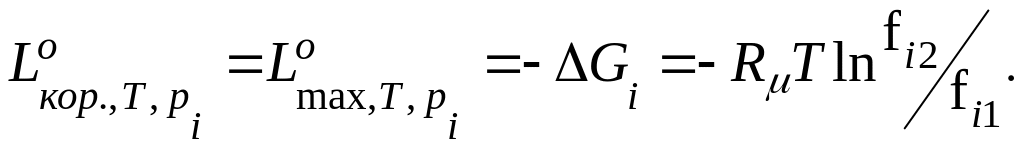 (8.22)
(8.22)
Стандартний стан
Стандартним (нормальним, нормалізованим, уявним, зведеним, приведеним) станом називають такий гіпотетичний стан реального ґазу, якби він при стандартній температурі (То=298,15К) і стандартному абсолютному тиску ро=1 атм мав властивости ідеального ґазу, тобто його властивости можна було б розрахувати за рівняннями ідеального ґазу.
Це стосується і стандартного стану і-го компоненту реальної ґазової суміші.
Якщо fо(або
 )
і Gi
(
)
і Gi
( )
– функції стандартного стану, то:
)
– функції стандартного стану, то:
