
- •2. Стереохимия амк
- •4. Синтез жк
- •5. Ферм-ты,их отличие от химических катализаторов
- •6. Какими путями при обмене амк обр-ется аммиак, роль глутамина и аспарагина в обмене в-в. Дезаминирование амк
- •2. Мажорные-минорные осн, пуриновые-пиримидиновые
- •3. Общ хар. Сахаров, тригалозный сахар
- •Трегалоза (-d-глюкопиранозил-(11)--d-глюкопиранозид) – невосстанавливающий резервный дисахарид грибов и насекомых.
- •5. Оксидоредуктазы
- •6. Бэта окисление жирн кислот.
- •1 Таутомерные превращения азот.Оснований
- •2 Гликозиды написать формулу метил-альфа-d-глюкозогликозид
- •3 Написать формулу кардиолипина и написать их хар-ку
- •4 Кинетика фер-тативных процессов ур-ние михаэлис-Мэнтен
- •6 Цикл глюкоза в лактат и сколько нужно и затрачено атф
- •1.МРнк строение и роль
- •3.Арахидоновая кисл и её произв(пг)
- •4.Изомеразы.Общая хар-ка,примеры реакций
- •5.Как влияет концентрац......(константа мих-мэнтоса)
- •6.Дых цепь
- •6 Биосинтез белка
- •2. Общая хар-ристика лигаз
- •3. Биосинтез рнк
- •5. Изоф-ты, функции
- •6. Цикл пировиноградной к-ты
- •3. Таутомерия глюкозы и что такое мутаротация
- •6. Рилизинг-факторы (либерины)
- •1. Факторы, влияющие на скорость ферм. Реакции
- •2. Биосинтез триглицерина и глицеролфосфолипидов биосинтез триглицеридов
- •3. Стр. Нуклеотида
- •5. Горм. Гипофиза
- •Вазопрессин и окситоцин
- •Меланоцитстимулирующие гормоны (мсг, меланотропины)
- •Адренокортикотропный гормон (актг, кортикотропин)
- •Соматотропный гормон (стг, гормон роста, соматотропин)
- •Лактотропный гормон (пролактин, лютеотропный гормон)
- •Тиреотропный гормон (ттг, тиротропин)
- •Гонадотропные гормоны (гонадотррпины)
- •Липотропные гормоны (лтг, липотропины)
- •1 Отличия и сходста днк и рнк
- •2 Произв. Моносахаридов: кислоты, гликозиды, аминосахара
- •3 Роль тиреоидных гормонов
- •4 Оксиредуктазы
- •2 Гормоны поджелудочной железы...Функции ....Строение...
- •Глюкагон
- •3 Гетерогликаны
- •4 Классы ф-тов
- •5 Аллостерическая активность ф-тов.
- •14 Билет
- •3 Горомны гипоталамусса, их природа и ролль...
- •4 Специфичность ф-тов
- •3) Хим. Природа связей, стабилизирующих первичную и вторичную стр-ру белков и нуклеиновых к-т
- •4) Гомогликаны (строение, функции)
- •5) Пиридоксин, его роль в регуляции белкового обмена, переаминирование(механизм р-ии и роль в метаболизме)
- •2. Гормоны,как производные амк, гормональный цикл
- •4. Лигазы(ферм-ты),их функции.
- •5. Гормональная регуляция акт-сти ф-та с пом вторичных посредников.
- •6. Пентозофосфатный путь(пфп) окисления ув
- •Основные р-ции моносахаридов, продукты р-ций и их св-ва
- •2. Пептиды
- •1. Структурная организация фермента
- •Активный центр ферментов.
- •2. Регуляторные центры
- •4. Общая классификация витаминов
- •5. Гликогенез и его роль Синтез гликогена (гликогенез)
- •1)Гликофосфолипиды
- •2) Однокомпонентные и двухкомпонентные ф-ты
- •4)Гликозиды, к-ты,моносахара,как производные монасахаридов
- •5)Мембрано-опосредованное вз-действие гормонов
- •6)Катаболизм амк
- •1. Стеролы и стероиды
- •2. Лактоза и ее св-ва
- •Роль тРнк
- •1.Макроэргические соединения
- •2.Гидролазы, роль
- •3.Арахидоновая кислота и ее роль в метаболизме и произв
- •5.Ингибирование, виды. Константа Михаэлиса и зависимость
- •6.Свободное окисление, его роль в антиоксидантном механизме
1 Таутомерные превращения азот.Оснований
Одним
из важных св-в своб АО (содержащих
оксигруппы)
явл возм-сть их сущ-ния в 2 таутомерных
формах, явление таутомерии заключается
в том, что вещество определенного состава
и молекулярного веса существует в виде
равновесной смеси двух или нескольких
изомеров, легко переходящих друг в
друга. в частности лактим- и лактамной
формах, в завис от знач рН среды: при рН
7,0 они представл в лактамной форме, при
снижении велич рН – в лактимной форме.
Таутомерные превращ можно представить
на примере урацила.
 Оказалось, что в сост природных НК все
оксипроиз-водные пуринов
и пиримидинов
находятся в лактамной форме.
Оказалось, что в сост природных НК все
оксипроиз-водные пуринов
и пиримидинов
находятся в лактамной форме.
2 Гликозиды написать формулу метил-альфа-d-глюкозогликозид
ГЛИКОЗИДЫ, соед., в к-рых остаток циклич. формы моно- или олигосахарида (гликозильный, или УГный, остаток) связан с др. орг. остатком (агликоном) через гетероатом; соотв. различают О-, N-, S-гликозиды и др. Связь м/у гликозильным остатком и агликоном наз. гликозидной.
При
обр-нии гликозидов возникает новый
асимметрич. гликозидный центр. Его
конфигурацию обознач![]() или
или![]() в завис от того, совпадает она или нет
с конфиг-ей того углерод атома
моносахарида,
к-рый определяет принадлежность
последнего к D- или L-ряду. Напр., в изомерных
метил-О-глюкопиранозидах конфигурация
в завис от того, совпадает она или нет
с конфиг-ей того углерод атома
моносахарида,
к-рый определяет принадлежность
последнего к D- или L-ряду. Напр., в изомерных
метил-О-глюкопиранозидах конфигурация![]() отражается ф-лой I, конфигурация
отражается ф-лой I, конфигурация![]() -ф-лой
II:
-ф-лой
II:

По размеру цикла УГ остатка гликозиды делят на фуранозиды (5-членные), пиранозиды (6-) и септанозиды. (7-); по числу моносахаридных остатков в УГной части мол-лы - на моноозиды, биозиды, триозиды и олигозиды (соотв. производные моно-, ди-, три- и олигосахаридов).
Присоед-ие гликозильного остатка к агликону (гликозилирование) повышает гидрофильность соед-ия, что играет важную роль в метаболизме. Мн. УГные остатки, особенно олигосахаридные, выполняют ф-ции специфич. маркеров пов-стей кл и биополимеров, обусл-ющих их узнавание др. кл.
К О-гликозидам в широком смысле слова относ не только гликозиды с неУГными агликонами, но и внутр. ангидриды сахаров (внутр. гликозиды), олиго- и полисахариды. О-Гликозиды- малолетучие кристаллич. или аморфные в-ва. Гликозиды низших спиртов легко раств. в воде, спиртах, не раств. в малополярных орг. р-рителях. Соед. с полярными агликонами (напр., гликозиды полиолов) раств. в воде, соед. с крупными гидрофобными агликонами не раств. в воде и малополярных р-рителях. Для олигозидов с большими малополярными агликонами хар-рны пенообразующие св-ва.
Гликозиды
не облад хим. св-вами восст-ющих Сахаров,
обусл-ными карбонильной группой, не
подвержены мутаротации.
Они легко ацилируются ангидридами
и галоген-ангидридами к-т в пиридине
с обр-нием сложных
эфиров,
алкилируются типичными алкилирующими
агентами в сильнощелочных средах, обр-ют
циклич. ацетали
и кетали
при конденсации
с карбонильными соед., окисляются
периодатами с расщеплением связей С—С,
подвергаются к-тному гидролизу,
алкоголизу,
формолизу с расщеплением гликозидной
связи. Скорость гидролиза
в Наиб. степени зависит от размера цикла:
фуранозиды гидролизуются на два порядка
быстрее пиранозидов. Механизм гидролиза
м. б. представлен след. схемой (знак ~
означает, что мол-ла
гликозида может им![]() или
или![]() конфигурацию):
конфигурацию):

Скор ф-тативного гидролиза, к-рый осущ-тся под дейст гликозидгидролаз, зависит от стр-ры агликона.
Гликозиды
с алифатич. и алициклич. агликонами
устойчивы к действию р-ров щелочей,
с ароматич. и нек-рыми гетероциклич.
агликонами
- неустойчивы. Так, щелочное
расщепление![]() D-глюкопиранозидов
с ароматич. агликоном
дает 1,6-ангидроглюкозу (левоглюкозан),
что явл препаративным методом синтеза
последней.
D-глюкопиранозидов
с ароматич. агликоном
дает 1,6-ангидроглюкозу (левоглюкозан),
что явл препаративным методом синтеза
последней.
К прир. О-гликозидам относятся сапонины, гликозиды сердечные, флавоноидные коф-ты (напр., рутин), гликолипиды, гликопротеины, нек-рые антибиотики.
Хим.
св-ва N-гликозидов сильно зависят от
хар-ра заместителей при атоме
N. Алифатич. и ароматич. N-Гликозиды,
содержащие при N атом
водорода,
подвергаются мутаротации
(подобно восстанавливающим сахарам)
вследствие таутомерного превращения
в форму шиффовых
оснований,
напр.:
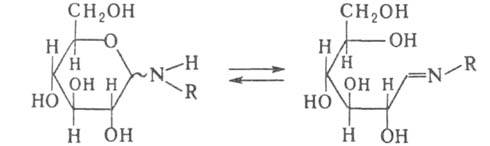
Они легко подвергаются к-тному и щелочному гидролизу.
N-Гликозиламиды, в т.ч. N-гликозилмочевины, и соед., в к-рых гликозидный атом N включен в амидную стр-ру, не склонны к мутаротации и по устойчивости к гидролизу сходны с О-гликозидами. Алифатич. и ароматич. гликозиды, в к-рых гликозидный атом N обладает достаточно высокой основностью, подвергаются перегруппировке в 1-амино-1-дезоксикетозы (Амадори перегруппировка).
Алифатич. и ароматич. N-гликозиды получают конденсацией восстанавливающих Сахаров с аминами; N-гликозиламиды и гликопептиды - восстановлением гликозилазидов с послед. N-ацилированием; нуклеозиды и их стр-рные аналоги-N-гликозилированием азотсодержащих гетероциклич. соединений ацилгликозилгалогенидами и их аналогами.
К прир. N-гликозидам относятся нуклеозиды, нуклеотиды, нуклеиновые к-ты, гликопротеины, нек-рые смешанные биополимеры, в к-рых гликозидная связь соединяет УГные и пептидные цепи через амидный атом N остатка аспарагина. Многие N-гликозиды и стр-рные аналоги нуклеозидов, являясь антиметаболитами нуклеозидов, обнаруживают высокую физиол. активность и используются в кач-ве лек. препаратов, напр. фторафур, цитарабин.
Для S-гликозидов хар-рны специфич. св-ва, связанные с возм-стью окислит.-восстановит. р-ций по атому S. К ним относятся гидрогенолиз над никелем Ренея, окислит. расщепление галогенами, окисление до сульфонов, обр-ние из S-гликозидов гликозилгалогенидов. Гидролиз S-гликозидов в отличие от гидролиза О-гликозидов может протекать в мягких условиях в присут. солей Hg и Cd, что позволяет вести селективную р-цию, не затрагивая О-гликозидные связи мол-лы. S-Гликозиды, аналогично ароматич. О-гликозидам, получают конденсацией тиолятов щелочных металлов с ацилгликозилгалогенидами. Специфич. методы - конденсация ацилгликозилгалогенидов с тиомочевиной с послед. гидролизом тиурониевой соли и частичный гидролиз диалкилдитиоацеталей Сахаров, катализируемый солями Hg.
