
- •2. Стереохимия амк
- •4. Синтез жк
- •5. Ферм-ты,их отличие от химических катализаторов
- •6. Какими путями при обмене амк обр-ется аммиак, роль глутамина и аспарагина в обмене в-в. Дезаминирование амк
- •2. Мажорные-минорные осн, пуриновые-пиримидиновые
- •3. Общ хар. Сахаров, тригалозный сахар
- •Трегалоза (-d-глюкопиранозил-(11)--d-глюкопиранозид) – невосстанавливающий резервный дисахарид грибов и насекомых.
- •5. Оксидоредуктазы
- •6. Бэта окисление жирн кислот.
- •1 Таутомерные превращения азот.Оснований
- •2 Гликозиды написать формулу метил-альфа-d-глюкозогликозид
- •3 Написать формулу кардиолипина и написать их хар-ку
- •4 Кинетика фер-тативных процессов ур-ние михаэлис-Мэнтен
- •6 Цикл глюкоза в лактат и сколько нужно и затрачено атф
- •1.МРнк строение и роль
- •3.Арахидоновая кисл и её произв(пг)
- •4.Изомеразы.Общая хар-ка,примеры реакций
- •5.Как влияет концентрац......(константа мих-мэнтоса)
- •6.Дых цепь
- •6 Биосинтез белка
- •2. Общая хар-ристика лигаз
- •3. Биосинтез рнк
- •5. Изоф-ты, функции
- •6. Цикл пировиноградной к-ты
- •3. Таутомерия глюкозы и что такое мутаротация
- •6. Рилизинг-факторы (либерины)
- •1. Факторы, влияющие на скорость ферм. Реакции
- •2. Биосинтез триглицерина и глицеролфосфолипидов биосинтез триглицеридов
- •3. Стр. Нуклеотида
- •5. Горм. Гипофиза
- •Вазопрессин и окситоцин
- •Меланоцитстимулирующие гормоны (мсг, меланотропины)
- •Адренокортикотропный гормон (актг, кортикотропин)
- •Соматотропный гормон (стг, гормон роста, соматотропин)
- •Лактотропный гормон (пролактин, лютеотропный гормон)
- •Тиреотропный гормон (ттг, тиротропин)
- •Гонадотропные гормоны (гонадотррпины)
- •Липотропные гормоны (лтг, липотропины)
- •1 Отличия и сходста днк и рнк
- •2 Произв. Моносахаридов: кислоты, гликозиды, аминосахара
- •3 Роль тиреоидных гормонов
- •4 Оксиредуктазы
- •2 Гормоны поджелудочной железы...Функции ....Строение...
- •Глюкагон
- •3 Гетерогликаны
- •4 Классы ф-тов
- •5 Аллостерическая активность ф-тов.
- •14 Билет
- •3 Горомны гипоталамусса, их природа и ролль...
- •4 Специфичность ф-тов
- •3) Хим. Природа связей, стабилизирующих первичную и вторичную стр-ру белков и нуклеиновых к-т
- •4) Гомогликаны (строение, функции)
- •5) Пиридоксин, его роль в регуляции белкового обмена, переаминирование(механизм р-ии и роль в метаболизме)
- •2. Гормоны,как производные амк, гормональный цикл
- •4. Лигазы(ферм-ты),их функции.
- •5. Гормональная регуляция акт-сти ф-та с пом вторичных посредников.
- •6. Пентозофосфатный путь(пфп) окисления ув
- •Основные р-ции моносахаридов, продукты р-ций и их св-ва
- •2. Пептиды
- •1. Структурная организация фермента
- •Активный центр ферментов.
- •2. Регуляторные центры
- •4. Общая классификация витаминов
- •5. Гликогенез и его роль Синтез гликогена (гликогенез)
- •1)Гликофосфолипиды
- •2) Однокомпонентные и двухкомпонентные ф-ты
- •4)Гликозиды, к-ты,моносахара,как производные монасахаридов
- •5)Мембрано-опосредованное вз-действие гормонов
- •6)Катаболизм амк
- •1. Стеролы и стероиды
- •2. Лактоза и ее св-ва
- •Роль тРнк
- •1.Макроэргические соединения
- •2.Гидролазы, роль
- •3.Арахидоновая кислота и ее роль в метаболизме и произв
- •5.Ингибирование, виды. Константа Михаэлиса и зависимость
- •6.Свободное окисление, его роль в антиоксидантном механизме
Билет 2
Вит- А ( ретинол)
Известны 3 вит гр А: А1, А2 и цис-форма вит А1 (неовит А). С хим т.зр. ретинол предст собой циклич непредельный одноат спирт, сост из 6-членного кольца (β-ионон), двух остатков изопрена и первичной спиртовой группы.

Вит А2 отлич от вит А1 наличием дополнит двойной связи в кольце β-ионона. Все 3 формы вит гр А сущ-ют в виде стереоизомеров, однако только нек-рые из них обладают био акт-тью. Вит гр А хорошо раств в жирах и жирораст-лях: бензоле, хлороформе, эфире, ацетоне и др. В орг-ме они легко окис-ся при участии специфич ф-тов с обр-нием соотв-ующих цис- и транс-альдегидов - ретиненов (ретинали), т.е. альдегидов вит-а А; могут откладываться в печени в форме более устойч сложных эфиров с уксусной или пальмитиновой к-той.
Хар-рными симптомами недостат-сти вит-а А у ч-ка и жив явл-ся торможение роста, снижение массы тела, общее истощение орг-ма, специфич пораж кожи, слизистых оболочек и глаз. Прежде всего пораж эпителий кожи, кожа усиленно шелушится, становится сухой. В результ нач-ся вторичные гнойные и гнилостные процессы. При авит-озе А пораж также эпителий слиз оболочки всего пищ-ного тракта, мочепол и дых аппаратов. Глазное яблоко не омывается слезной жид-тью, к-рая облад бактерицидным св-вом. Этот комплекс поражений обозначают термином «кератомаляция»; она развив оч быстро, иногда в теч нескольких часов. Распад и размягчение роговицы связаны с развитием гнойного процесса, поскольку гнилостные микроорг-мы при отсутствии слезной жидкости быстро развиваются на поверхности роговицы.
К наиболее ранним и специфическим симптомам авит-оза А (гиповит-оза А) относится куриная, или ночная, слепота. Она выражается в потере остроты зрения, точнее, способности различать предметы в сумерках, хотя больные днем видят нормально.
Хар-рны проявл гипер-вит-оза А: воспаление глаз, гиперкератоз, выпадение волос, общее истощение орг-ма. При этом, как правило, отмечаются потеря аппетита, головные боли, диспепсические явления (тошнота, рвота), бессонница. Гипервит-оз может развиться и у детей в результ приема больших кол-в рыбьего жира и препаратов вит-а А.
Биологическая роль. Вит- А оказывает влияние на барьерную функцию кожи, слизистых оболочек, проницаемость кл-ых мембран и биосинтез их компонентов, в частности определенных гликопротеинов. Действие вит-а А в этих случаях связывают с его вероятной причастностью к синтезу белка. Сущ-ет предположение, что благодаря наличию двойных связей в мол-ле вит- А может участвовать в ОВР, поскольку он способен образовывать перекиси, к-рые в свою очередь повышают скорость окисления других соединений.
В проц светоощущения большую роль играет хромолипопротеин – сложный белок родопсин, явл-ся осн светочувствительным пигментом сетчатки, в частности палочек. Установлено, что родопсин сост из липопротеина опсина и простети-ческой группы, представленной альдегидом вит-а A1(ретиналь); связь м/у ними осущ-тся через альдегидную гр вит-а и свобод ε-NH2-группу лизина мол-лы белка с обр-нием шиффова основания. На свету родопсин расщепляется на белок опсин и ретиналь; последний подвергается серии конформационных изм-ний и превращ в транс-форму. С этими превращ связана трансформация энергии свет лучей в зрительное возбуждение В темноте происх обратный проц – синтез родопсина, требующий наличия актив формы альдегида – 11-цис-ретиналя, к-рый может синтез-ся из цис-ретинола, или транс-ретиналя, или транс-формы вит-а А при участии 2 специфич ф-тов – дегидрогеназы и изомеразы.
Распр-ние в природе и суточная потреб. Вит- А широко распр-н. Наиболее богаты этим вит-ом печень круп рог скота и свиней, яичный желток, цельное молоко, масло, сметана, сливки. Особенно много свободного вит-а А в жирах печени морс окуня, трески; красно-мякотные овощи (морковь, томаты, перец и др.), в к-рых вит- А сод-тся в виде провит-ов – каротинов.
Суточная потребность для взрослого человека составляет в среднем 2,7 мг вит-а А или от 2 до 5 мг β-каротина. У человека основным органом, в к-ром частично откладывается про запас вит- А, явл печень. В норме в ней содержится около 20 мг этого вит-а на 100 г ткани.
2. Стереохимия амк
Важнейшим св-вом АМК, освобожд-ся в проц гидролиза природных белков в условиях, исключающих рацемизацию, явл их оптическая акт-ть. Будучи раст-ными в воде (или в НСl), они способны вращать плоскость поляризованного луча (исключ сост глицин). Это св-во связано с наличием в мол-ле всех природных АМК (за ислюч глицина) в α-положении асимметрич атома С. Величины удельного вращения вправо или влево явл колич-ной хар-кой оптич акт-сти, и для больш-ва АМК сост от 10 до 30°. Примерно половина АМК белков оказалась правовращающей, их обозначают знаком «+» (Ала, Иле, Глу, Лиз и др.), а чуть меньше половины - левовращ (Фен, Трп, Лей и др.), их обознач знаком «–». Все эти АМКы принадлежат к L-ряду, а величина и знак оптич вращения зависят от природы радикалов АМК и значения рН раствора, в к-ром измеряют оптическое вращение.
Стереохимию
АМК
принято оценивать не по оптич
вращению,
а исходя из абсолютной конфигурации
всех 4 замещающих групп, располож вокруг
асимметрич
атома
углерода
в вершинах модели тетраэдра. Абсолютную
конфигурацию АМК
принято соотносить стереохим с соед-м,
произвольно взятым для сравнения, а
именно с глицериновым
альдегидом,
также содержащим асимметрич
атом
С.
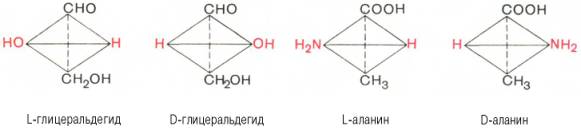
Все
АМКы,
обр-щиеся при гидролизе
природ белков
в усл, исключающих рацемизацию,
принадлежит к L-ряду. Т.об., природные
АМКы
им простр-ное располож, аналогичное
конфигур L-глицеринового альдегида.
Символы L и D означ принадлеж данной АМКы
по своей стереохим
конфигур
к L- или D-ряду, а «+» или «–» указ на
направл изменения плоскости поляризации
светового луча. Среди белковых АМК
имеются 2 АМКы
(треонин
и изолейцин),
к-рые содерж по 2 асимметр
атома
С. след в лаб-рии возможно получить 4
стереоизомерные формы этих АМК
. Для треонина
известны все 4 изомера.
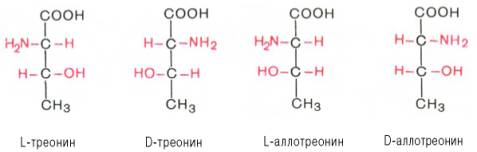
Как отмечалось, в белковой мол-ле D-АМКы не обнаружены , однако в живой природе они широко распространены.
Так, D-изомеры глутаминовой к-ты, аланина, валина, фенилаланина, лейцина и ряда других открыты в клеточной стенке бактерий; в составе нек-рых антибиотиков, в частности актиномицинов, бацитрацина, грамицидинов А и S, содержатся АМКы D-конфигурации.
3. РАЦЕМАТЫ, сост из эквимол. кол-в энантиомеров и не облад оптич. акт-тью. Сущ-ют в виде мол. соед-ний (истин Р.) и рацемич. смесей кристаллич. энантиомер (конгломерата, т. е. простой смеси кристаллов право- и левовращающего антиподов) или смешанных кристаллов, обр-нных обоими энантиомерами. Физ. св-ва (т-ра плавления, плотность, р-римость и др.) истинных рацематов отличны от св-в индивид-х энантиомеров. Обр-ние ист рацематов обусл водородн связями, индукционным или дисперсионным вз-действием.
Рацематы обр-ся при любом хим. синтезе, приводящем к хиральным мол-лам, если исход компоненты р-ции были оптически неактивны и синтез проводился в отсутствие асимметризующих воздействий. Это обусл тем, что переходные сост при обр-нии энантиомеров энергетически эквивалентны. При наличии асимметризующих факторов переходные состояния диастереомерны, их энергия различна, поэтому возможно обр-ние предпочтительно одного из двух энантиомеров конечного продукта.
Пары
диастереомеров, различающиеся
конфигурацией одного из неск. асимметрич.
атомов,
наз. эпимерами,
напр.:
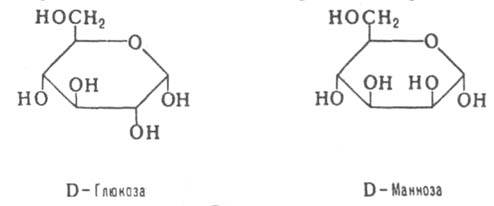
оптич антиподы -
в-ва, хар-щиеся противополож по знаку и
одинаковыми по величине вращениями
плоскости поляризации
света при идентичности всех других физ.
и хим. св-в. Необход и достаточная причина
возникновения оптич. антиподов - отнесение
мол-лы
и одной из след, точечных групп симметрии
Сn,
Dn,
Т, O, I. Чаще всего речь идет об асимметрич.
атоме
углерода,
т.е. об атоме,
связанном с 4 разными заместителями,
напр.:

