- •2.3. Получение фторорганических соединений
- •2.3.1. Общие методы получения фторорганических соединений
- •2.3.2. Синтез лекарственных средств
- •2.4. Диазотирование и диазореакции
- •2.4.1. Диазотирование ароматических аминов
- •2.4.2. Строение солей диазония, реакционная способность
- •2.4.3. Реакция азосочетания
- •2.4.4. Восстановление диазосоединений
- •2.4.5. Реакции диазосоединений с выделением азота
- •2.4.6. Техника безопасности, экология
- •2.5. Методы восстановления кратных связей
- •2.5.1. Методы восстановления, реагенты и катализаторы
- •2.5.2. Восстановление кратных с-с связей
- •2.5.3. Восстановление кратных c-n связей
- •2.5.4. Восстановление кетонов, альдегидов
- •2.5.5. Восстановление сложных эфиров
- •2.5.6. Восстановление азосоединений и солей диазония
- •2.5.7. Восстановление нитрозогрупп
- •2.5.8. Восстановление нитрогрупп
- •2.5.9. Техника безопасности, экология
- •2.6. ОкислениЕ и дегидрированиЕ
- •2.6.1. Реакции окисления
- •При синтезе никотиновой кислоты (витамина рр) окисление азотной кислотой не приводит к желаемому результату. Приходится использовать более сильный окислитель – перманганат калия:
- •2.6.2. Дегидрирование
- •Следует отметить интересный метод ароматизации дигидропиразола, приведенный на схеме:
- •2.6.3. Техника безопасности, экология
- •2.7. Реакции конденсации и гетероциклизации
- •2.7.1. Реакции конденсации
- •2.7.2. Реакции гетероциклизации
- •2.7.3. Синтез лекарственных препаратов
- •2.8. Основные концепции комбинаторной химии
- •Твердофазный синтез
- •2.8.2. Метод параллельных синтезов
При синтезе никотиновой кислоты (витамина рр) окисление азотной кислотой не приводит к желаемому результату. Приходится использовать более сильный окислитель – перманганат калия:
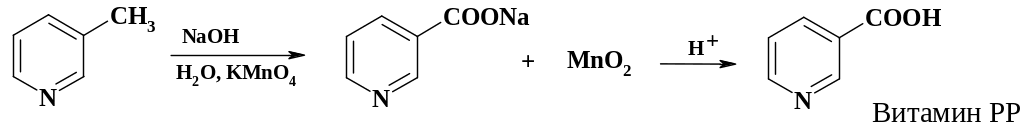
Процесс окисления ведут в эмалированном аппарате. Перманганат добавляют порциями с помощью шнекового питателя в раствор -пиколина в щелочи. Выпавший осадок диоксида марганца отфильтровывают, при подкислении фильтрата выделяется никотиновая кислота.
Окисление бензольного кольца в бензимидазоле используется при синтезе препарата этимизол. Это лекарственное средство стимулирует дыхательный и двигательный центры продолговатого мозга (аналептик), обладает противовоспалительным, противоаллергическим действием, снимает чувство тревоги. Этимизол индуцирует выработку адренокортикотропного гормона (АКТГ), ингибирует фосфодиэстеразу, способствует накоплению внутриклеточного ц-АМФ, усиливает гликогенолиз, активирует метаболитические процессы в ЦНС. Полный синтез приведен на схеме:
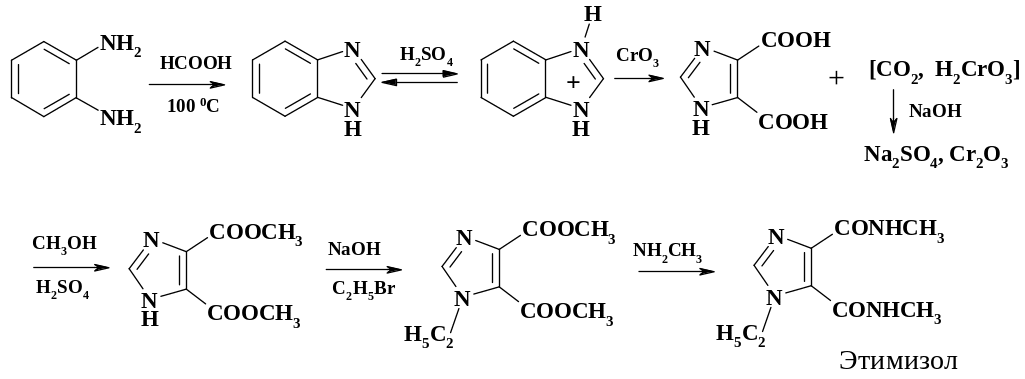
Окисление бензимидазола проводят хромовым ангидридом или бихроматом натрия в 70 % серной кислоте при 85 – 90 oС. Как и в случае нитронафталина, окислению подвергается цикл, несодержащий электроноакцепторный заместитель. В условиях проведения процесса имидазольный цикл протонирован, а положительный заряд делокализован между двумя равноценными атомами азота, окисляется бензольный цикл. После окончания процесса реакционную массу выливают на охлажденную воду, выпавший осадок 4,5-имидазолдикарбоновой кислоты отфильтровывают. Следует отметить, что окисление солями хрома является экологически напряженным процессом, т. к. ионы шестивалентного хрома высокотоксичны, попадание их в сточные воды недопустимо и строго регламентируется. Поэтому фильтрат после отделения имидазолдикарбоновой кислоты подщелачивают, вводят слабый восстановитель, оксид трехвалентного хрома отфильтровывают.
В разделе 2.1.6. при описании получения хлораля из этилового спирта отмечалось использование хлора в качестве окислителя. В синтезе противовирусного препарата оксолин хлорирующие агенты также используются в качестве окислителей. Это лекарственное средство в виде мази применяют для лечения гриппа, вирусного ринита, герпеса и кератита.
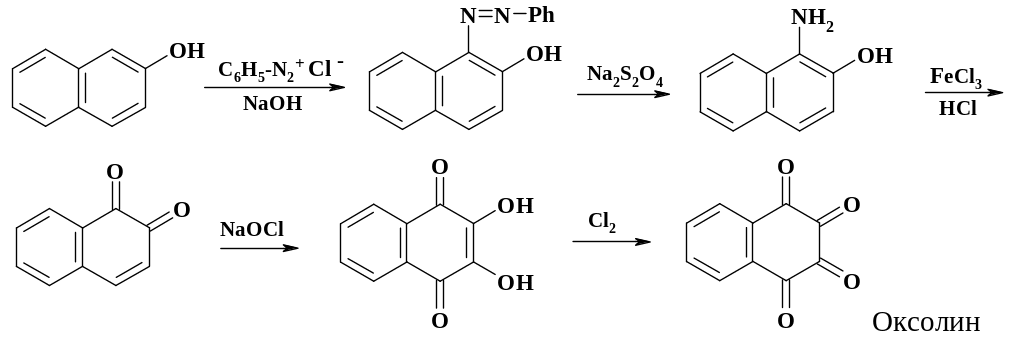
Окисление хлорным железом 1-амино-2-нафтола, который получают восстановлением азосоединения, синтезированного из 2-нафтола и фенилдиазоний хлорида, дает 1,2-нафтохинон. Отфильтрованную влажную пасту нафтохинона суспендируют в воде и медленно прибавляют раствор гипохлорита натрия. Полученный изонафтазарин переосаждают из щелочи соляной кислотой с добавлением для очистки акивированного угля. Дальнейшее окисление до 1,2,3,4-тетрагидро-1,2,3,4-тетраоксонафталина проводят хлором при температуре 40 oС. Использование других окислителей приводит к получению примеси фталевой кислоты.
При действии гипохлорита натрия и хлора хлорирования в цикл не наблюдается, т. к. в нафталиновом ядре уже имеются электроноакцепторные группы и отсутствует катализатор хлорирования.
2.6.2. Дегидрирование
Реакция дегидрирования является обратной процессу гидрирования. Она также идет по свободнорадикальному механизму, как правило, на поверхности катализатора (соли меди, хрома, металлические серебро, палладий или платина). Для отрыва двух атомов водорода необходимо не только применение катализатора, но и высокая температура, т. к. процесс является равновесным и эндотермическим. Субстрат дегидрирования сорбируется на поверхности катализатора, происходит разрыв С-Н, CN-H или CО-Н связей с образованием двойной связи C=C, C=O, C=N и выделением молекулы водорода. При гидрировании после окончания процесса объем реакционной массы уменьшается, и для смещения равновесия используют повышенное давление. В случае дегидрирования наоборот – объем реакционной массы увеличивается, для смещения равновесия необходимо понижать давление. Так степень конверсии этилбензола в стирол при давлении 0,1 МПа составляет 40 %, а при 0,01 МПа уже 80 %. Необязательно реакции проводить при пониженном давлении, к тому же результату приводит разбавление реагентов инертным газом, т. к. их парциальное давление уменьшается.
Наиболее многотоннажным производством, в котором используется эта реакция, является получение бутадиена-1,3 и изопрена. Дегидрирование осуществляют как в одностадийном, так и двустадийном варианте. Степень конверсии бутана составляет около 50 %. На схемах приведены условия синтеза бутадиена-1,3:
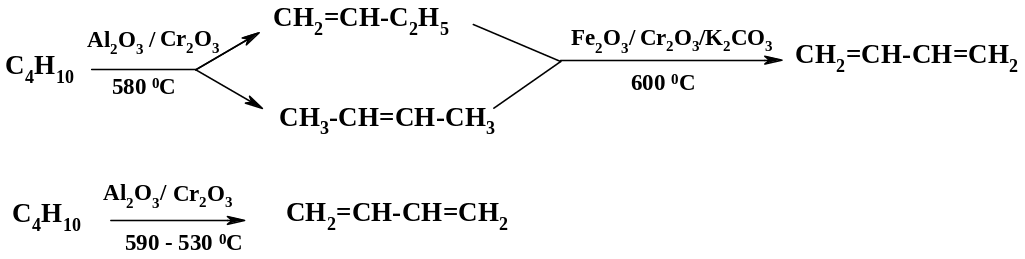
Технологическое оформление процесса довольно сложное (см. [2] к разделу 1.3). В случае одностадийного процесса энергозатраты ниже.
Стирол, метилстирол и дивинилбензол также получают дегидрированием соответствующих углеводородов. Для поддержания температуры и снижения парциального давления в пары этилбензола вводят перегретый пар.
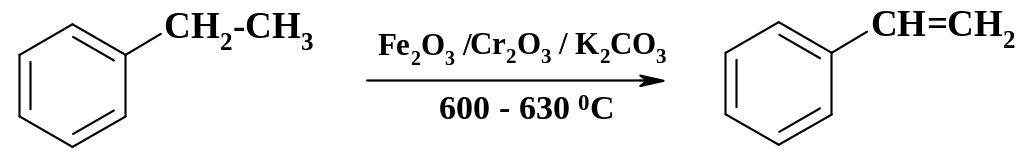
Формальдегид (водный раствор – формалин), его олигомеры и полимеры находят широкое применение в медицинской промышленности. По одному из способов формальдегид получают окислительным дегидрированием метанола на серебряном катализаторе. Серебро наносят на пемзу. Соотношение реакций окисления и дегидрирования составляет обычно 55 и 45 %.
![]()
Из напорного бака 90 % водный метанол поступает в испаритель. Через распределительное устройство подают воздух так, чтобы в 1 л паровоздушной смеси содержалось около 0,5 г метанола, что существенно выше пределов взрываемости. Процесс контролируется автоматически, т. к. несоблюдение концентрации метанола в паровоздушной смеси может привести к взрыву. Смесь поступает в перегреватель, а затем в контактный аппарат. После прохождения процесса полученная смесь поступает в подконтактный теплообменник, где она охлаждается до 100 – 130 oС, а затем на абсорбер. Пар, полученный в этом теплообменнике, идет на перегреватель. Получают 36 – 37 % формалин, содержащий, в зависимости от аппаратурного оформления абсорбции, от 1 до 10 % метанола. Выход формальдегида составляет от 85 до 90 %. Синтез формальдегида проводят также и в режиме реакции окисления без дегидрирования. В этом случае применяют железо-молибденовый катализатор [твердый раствор MoO3 в Fe2(MoO4)3]. Аналогично формальдегиду окислительным дегидрированием получают глиоксаль из этиленгликоля.
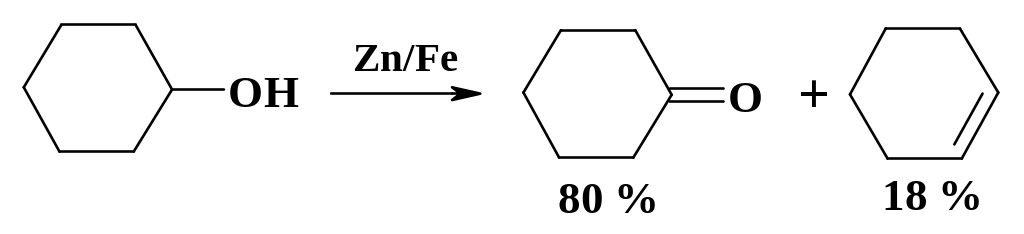
Еще одним продуктом, который используют при получении полимеров и лекарственных средств, является циклогексанон. По одному из методов его получают дегидрированием циклогексанола (см. раздел 2.5.2). Процесс ведут в трубчатом теплообменнике при температуре 430 – 450 oС, катализатором служит оцинкованное железо. Основным побочным продуктом является циклогексен. Чистый продукт получают ректификацией.
В производстве препарата папаверин (биологическое действие и полный синтез приведены в разделе 3.7, получение полупродуктов в разделе 2.3.4) на последней стадии используют реакцию дегидрирования:
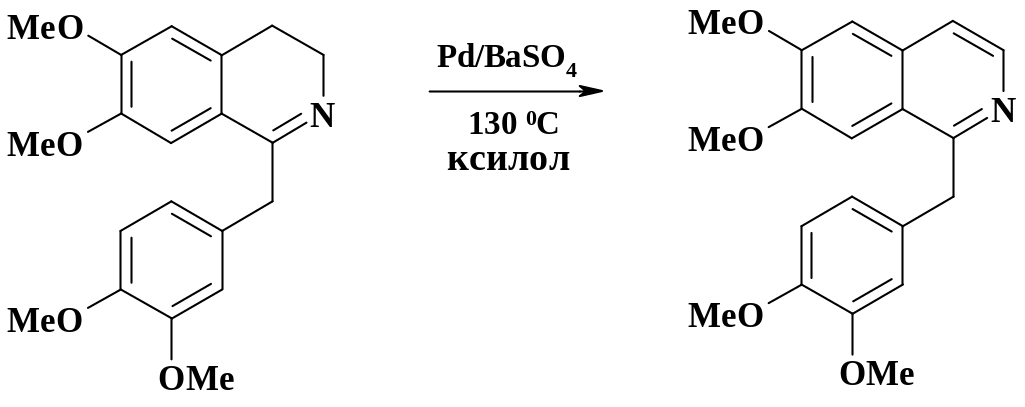
В качестве катализатора этой реакции применяют палладий, нанесенный на сульфат бария. Процесс вели при температуре 200 oС в очищенном тетралине. Недостатком этого метода являлось то, что папаверин приходилось очищать от примеси нафталина, который получался при дегидрировании тетралина. Тетралин был заменен на ксилол, при этом увеличилась чистота препарата.
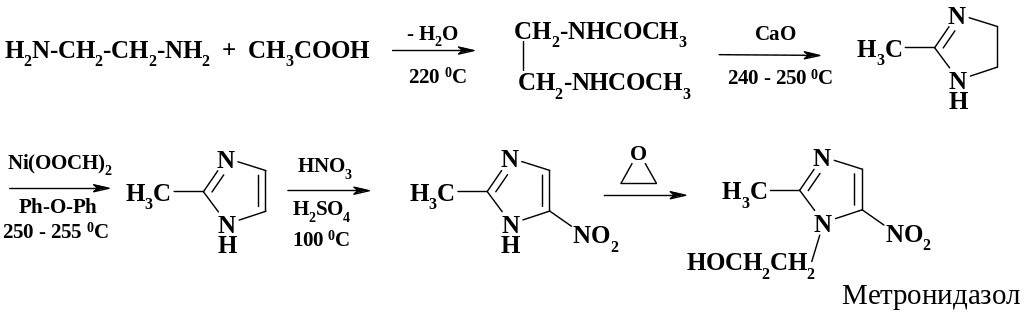
В производстве трихопола (метронидазола) (биологическое действие препарата рассмотрено в разделе 2.3.1) при получении 2-метилимидазола проводят дегидрирование с использованием катализатора – формиата никеля. Реакцию ведут при температуре 250 oС в дифенилоксиде. Полный синтез препарата приведен на схеме: