
- •Нормы белка в питании
- •Критерии полноценности пищевых белков
- •Внешний обмен белков
- •Переваривание в желудке
- •Функции соляной кислоты:
- •Переваривание в кишечнике
- •Преобразования сложных белков
- •Всасывание аминокислот
- •Процессы гниения белков в кишечнике
- •Внутриклеточный обмен аминокислот
- •Дезаминирование
- •1. Окислительное.
- •Трансаминирование (переаминирование).
- •Декарбоксилирование
- •Пути обезвреживания биогенных аминов
- •Пути образования и обезвреживания аммиака
- •Нарушение детоксикации аммиака приводит к накоплению его в организме и возникает гипераммониемия
- •Синтез амидов
- •Интегральная схема
- •Аммониогенез
- •Синтез креатина
- •1) В почках:
- •Понятие клиренса
- •3,5 Ммоль/л
- •Кетогенные и гликогенные аминокислоты
Лекции по теме «Обмен белков» (доцент Жаворонок Т.В.)
Белковый обмен занимает ведущее место среди превращений веществ в клетке. Это обусловлено важными функциями белков.
Белки находятся в организме в состоянии динамического равновесия. Период полураспада белков в организме ~ 80 дней (печень, сыворотка ~ 10 дней). Белки содержат 16% азота (α-аминогруппы и гетероциклы в аминокислотах), а углеводы и липиды содержат доли процентов азота. Количество азота (белка) в веществе определяют с помощью коэффициента 6,25 (100/16), умножая на 6,25. В оценке белкового обмена организма используют понятие «азотистый баланс».
Азотистый баланс [г/сут] – количественная разница между введением азота с пищей и выведением его в виде конечных продуктов азотистого обмена:
а) положительный – азота выводится меньше, чем поступает с пищей (часть остаётся в организме и расходуется на биосинтез белков), наблюдается у детей;
б) отрицательный – азота выводится больше, чем поступает с пищей, наблюдается при голодании, белковой недостаточности, тяжёлых заболеваниях;
в) азотистое равновесие – поступает и выводится равное количество азота, характерно для здорового взрослого организма на полноценной диете.
Нормы белка в питании
Для достижения азотистого равновесия, сохранения здоровья человека и обеспечения работоспособности необходимо знать нормы белка в питании.
В XIX веке немецкий учёный Фойт научно обосновал необходимое человеку количество пищевых компонентов за сутки.
С учётом анкетных данных, статистических методов для суточной диеты (количественного и качественного состава пищи) были рекомендованы нормы:
белков – 120 г; углеводов – 500 г; жиров – 50 г.
При белковом голодании у человека в сутки распадается 23 г белка (выводится) → коэффициент изнашивания.
При поступлении 45 г белка (35-45 до 50 г) с пищей в сутки сначала наступает азотистое равновесие – физиологический минимум. Через некоторое время (полгода-год) снова развивается отрицательный азотистый баланс. Для предотвращения нужно есть 80-100-120 г в сутки (зависит от массы тела).
Качество белковой пищи. Из 20 АК 8 незаменимы (три, тре, лиз, вал, иле, лей, мет, фен), но необходимы все. У детей незаменимы ещё и арг, гис. Недифференцированный азот – совокупность заменимых АК, поступающих с пищей
Критерии полноценности пищевых белков
усвояемость белка – степень их гидролиза в ЖКТ;
наличие незаменимых аминокислот в составе белка пищи;
чем ближе состав АК принимаемого белка пищи к составу АК белков тела, тем выше его биологическая ценность. Она определяется по соответствию между содержанием незаменимых АК в белке и потребностью в них организма.
Существует международный условный образец белка, который содержит в своем составе около 32% незаменимых аминокислот.
Наиболее близок к нему белок молока матери и куриного яйца.
Спектр аминокислотного состава:
растительные
белки
мясо 20–25%
рыба 16–20%
творог до 15% (как правило)
сыр до 30%
молоко 3,5%
хлеб 7–10%
картофель 0,2%
горох 25%
соя до 35%
Внешний обмен белков
Внешний обмен белков – превращение белков в ЖКТ путём последовательного действия протеолитических ферментов. Это тотальный протеолиз малоспецифичными протеиназами, которые расщепляют пептидную связь около 1-й, 2-х или 3-х конкретных АК.
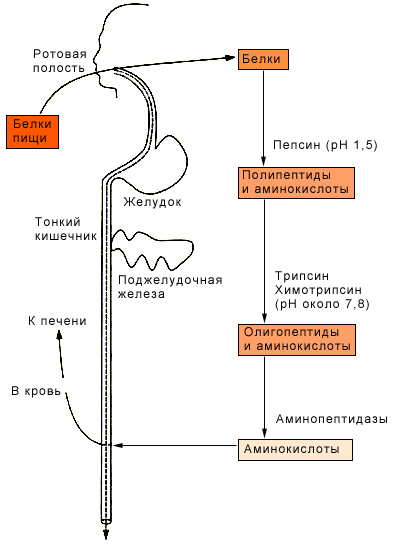
Рис. Переваривание белков в желудочно-кишечном тракте.
Переваривание в желудке
Переваривание белков начинается в желудке.
Желудочное пищеварение под контролем нервной и гуморальной регуляции. Гуморальные регуляторы: гастрин (стимулирует главные, обклад и добав клетки, вызывая секрецию) и гистамин (стимулирует выделение НСl).
Желудочный сок за счёт НСl имеет кислое значение рН 1–3 (1,5).
Функции соляной кислоты:
создаёт оптимальное значение рН;
переводит неактивный пепсиноген в активный пепсин;
вызывает денатурацию белка (частичный кислотный гидролиз);
оказывает бактерицидное действие;
влияет на всасывание железа.
НСl синтезируется в обкладочных клетках (за счёт энергии АТФ: Н+/K+-АТФаза).
кровь обкладочные клетки просвет желудка
Na+
Cl
–
NaHCO3
HCl
Cl–
H+
HCО3–
3333Щl




HCO3– транспортируют из крови в клетку анионные каналы в обмен на Cl–, который по хлоридным каналам идёт в просвет желудка. Н+ выкачивает Н+/K+-АТФаза в обмен на К+, который возвращается в желудок по каналам вместе с Cl–.
Главные (пепсиновые) клетки желёз продуцируют в желудочный сок пепсин (М.М. ~ 40000 Да) и гастриксин (оптимум рН=3, м.б. изофермент пепсина).
Чтобы не переваривать собственные клетки: 1) пищеварительные ферменты синтезируются в виде проферментов (неактивных форм), 2) добавочные (слизистые) клетки продуцируют слизистый углеводный секрет (муцины) - он защищает полость желудка от действия протеаз и HCl (переваривания изнутри).
Пепсиноген состоит из:
остаточный
полипептид
ингибитор пепсина
пепсин
HCl







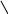


активный пепсин
аутокатализ аутокатализ
Пепсиноген может превратиться в пепсин при участии НСl, но медленно. Сам пепсин затем осуществляет автокатализ очень быстро.
Активация заключается в разрыве пептидной связи с удалением 42 АК и перестройке пространственной структуры оставшейся части молекулы со сближением аминокислотных остатков активного центра (называется – ковалентная химическая модификация путём частичного протеолиза).
Пепсин и гастриксин желудочного сока относят к эндопептидазам, они гидролизуют пептидные связи внутри белковых молекул:
пепсин → около ароматических аминокислот;
гастриксин → между дикарбоновыми аминокислотами.
Расщепляют белки до смеси полипептидов – альбумозы и пептоны.
У грудных детей в желудочном соке есть фермент реннин (химозин), близок пепсину, удаляет концевой гликопептид казеиногена молока, вызывая створаживание, что очень важно для гидролиза, т.к. жидкости в желудке не задерживаются. У детей в желудке рН = 3,5-4-5.
